Наличие большого выбора антибактериальных препаратов значительно расширяет возможности лечения, но одновременно требует от врача-клинициста глубоких знаний о свойствах антибиотиков, спектре действия, эффективности в отношении той или иной инфекции, побочных эффектах, возможном токсическом влиянии и взаимодействии с другими лексредствами.

Ошибка № 1
Антибиотики как средство лечения симптомов или профилактики бактериальной инфекции
По словам спикера, часто антибиотики назначаются на основании наличия симптомов, например, кашля или лихорадки, а не на основании диагностированной или предполагаемой бактериальной инфекции. Еще одна распространенная ситуация — когда врач выписывает антибиотики пациенту с ОРВИ в качестве профилактики присоединения бактериальной инфекции.
Дмитрий Рузанов:
Сегодня принята презумпция неназначения антибиотиков. Они отнюдь не являются безопасными препаратами. Без четких показаний, очевидных признаков бактериальной инфекции антибиотик может нанести больше вреда, чем принести пользы, и конкретному пациенту, и обществу в целом.
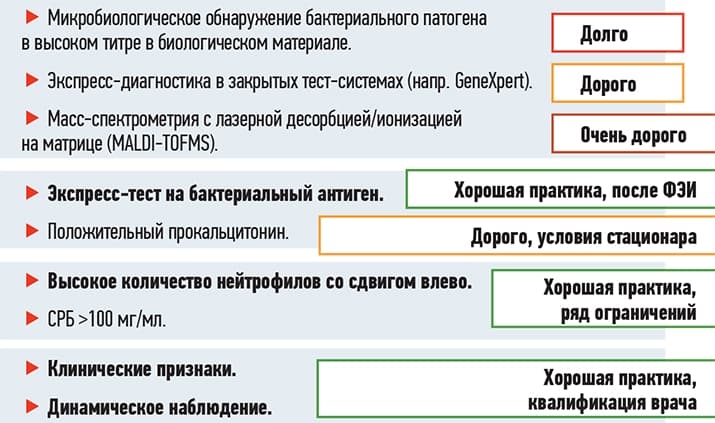
Существуют различные диагностические методы детекции бактериологического возбудителя (см. рис. 1). Часть из них длительны по времени (например, микробиологический посев), другие — точные, быстрые, но крайне дорогостоящие (масс-спектрометрия), некоторые тоже недешевы и используются в условиях стационара (прокальцитонин).
Рисунок 1. Диагностические критерии бактериальной инфекции.
Дмитрий Рузанов:
В большинстве случаев врачу приходится полагаться на свой опыт и мастерство при диагностике бактериальной инфекции. Это во многом определяется клиническими признаками и динамическим наблюдением за пациентом. Общий анализ крови имеет недостаточную специфичность и чувствительность в отношении диагностики бактериальной этиологии инфекции.
Среди недооцененных в амбулаторной практике, но при этом чувствительных и недорогих диагностических методов можно отметить определение С-реактивного белка: если показатель больше 100 мг/мл — с высокой вероятностью это бактериальная инфекция, требующая неотложного назначения антибиотика, а снижение СРБ скажет об эффективности антибиотика.
Как определить, нужен ли пациенту антибиотик? В первую очередь следует исключить те диагнозы, которые требуют их обязательного и неотложного приема: пневмонию, острый стрептококковый тонзиллит (ангину), острый гнойный средний отит, гнойный риносинусит. И это может каждый врач общей практики. Нужны стетоскоп, шпатель и отоскоп. Услышали бронхиальное дыхание или хрипы — сделайте обзорный снимок легких.
Исключив эти четыре патологии, можно продолжить динамическое наблюдение без антибиотика. Конечно, стоит учитывать и эпидемиологическую ситуацию, например, подъем заболеваемости гриппом, привит ли пациент, сведения о предшествующих назначениях антибиотика, наличие факторов риска антибиотикорезистентности.
Дмитрий Рузанов:
Важно обращать внимание и на факторы риска и коморбидность пациента. Чем она выше, тем больше вероятность бактериальной инфекции, тем выше риски устойчивости к стартовым антибиотикам. Возможна гипердиагностика «гнойности» выделений.
Например, ряд аллергических заболеваний могут давать характерный желтоватый цвет выделений слизи как из бронхиального дерева, так и из верхних дыхательных путей. К 5–7-му дню риновирусной инфекции слизь может окрашиваться омертвевшими клетками эпителия. И наоборот, иммунокомпрометированные сопутствующими заболеваниями пациенты могут иметь стертые клинические симптомы бактериальной инфекции, подострое начало и невысокую лихорадку.
Стадийность течения респираторной инфекции в целом характерна как для вирусной, так и для бактериальной. И здесь много заблуждений. Например, так называемое правило третьего дня, когда антибиотик назначают на 3-и сутки заболевания при сохранении повышенной температуры, нерационально. Почему? Потому что большинство вирусов (аденовирус, парагрипп, РСВ, метапневмовирус) сопровождаются лихорадкой в течение недели, их часто и называют семидневными. Снижаться температура начинает с 4–5-го дня и нормализуется к 7-му. В итоге — череда совпадений: на 3–4-й день назначаются антибиотики, а через день температура снижается. Но это не заслуга антибиотика, а естественное течение вирусной инфекции. Наиболее частый «трехдневный» вирус — риновирус, когда действительно к 3-му дню субфебрильная температура возвращается в норму и пациента чаще всего минует участь принимать антибиотик.
Дмитрий Рузанов:
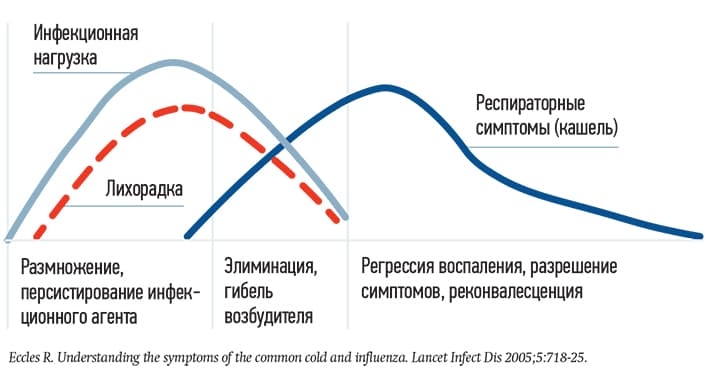
Еще одна частая причина избыточного использования антибиотика — когда кашель при вирусных инфекциях появляется через несколько дней после лихорадки и к 7-му дню усиливается, достигая своего пика, а температура обычно к этому времени уже нормализуется (см. рис. 2).
Часто именно в этот момент и начинают прием антибиотика или его замену («Пациенту стало хуже, у него нарастает кашель, инфекция прогрессирует…»). Вместе с тем, как правило, кашель самостоятельно начинает стихать и проходит в течение одной-двух недель. Такой кашель и называют постинфекционным.
Но в случае назначения в этот период антибиотика появляется ошибочное мнение, что сработал именно антибактериальный препарат. Поэтому стоит помнить об этапности развития респираторной инфекции. При сборе анамнеза важно понимать, в какой патогенетической фазе находится пациент, чтобы прогнозировать дальнейшее течение, выбрать лечение и исключить избыточное назначение антибиотиков, — уверен эксперт.
Рисунок 2. Патогенез и симптоматика ОРВИ.
Изменилось отношение и к профилактическому использованию антибиотиков на фоне вирусной инфекции («А вдруг пневмония присоединится?»). Исследования в области детекции некультивируемых микроорганизмов позволили открыть и говорить еще об одном органе нашего тела — микробиоме, в том числе респираторном. Да, нижние дыхательные пути далеко не стерильны, как нас когда-то учили! Они заселены микробами, грибами, вирусами, которые регулируют иммунитет и защищают от патогенных микроорганизмов. Соответственно, антибиотики способны нарушить это равновесие.
Другими словами, поясняет Дмитрий Рузанов, антибиотики способны повысить вероятность присоединения бактериальной инфекции, даже если ее не было.
Ошибка № 2
Назначение антибиотиков с избыточно широким спектром действия
Неверно полагать, что чем шире спектр действия у препарата, тем лучше. И другая крайность — когда назначаются антибиотики, у которых нет активности в отношении, например, респираторных патогенов.
«Нереспираторные» антибиотики:
- Фторхинолоны 2-го поколения
- Ко-тримоксазол
- Аминогликозиды
- Цефалоспорины 1-го поколения
- Эритромицин
Дмитрий Рузанов:
Существует широкий гипотетический спектр респираторных инфекций, которые могут быть у пациента. Но на практике для амбулаторной инфекции актуальны лишь несколько возбудителей: пневмококк, гемофильная палочка, моракселла, пиогенный стрептококк и микоплазма, совсем редко — стафилококк. Все остальное обычно удел госпитальных тяжелых инфекций. Соответственно, и антибиотики в этом случае понадобятся другие, а если они не сработают по причине резистентности, пациент погибнет. Поэтому мы и должны ограничить их широкое использование, не стрелять, как говорится, из пушки по воробьям.
Если проанализировать клинические руководства по лечению респираторных бактериальных инфекций — белорусские, российские, китайские, австралийские, европейские, — везде стартовым препаратом для антибиотикотерапии будет амоксициллин. Как при гнойном среднем отите, так и при бактериальном риносинусите или инфекции нижних дыхательных путей. И это обосновано и рационально. Цефалоспорины 1-го поколения или фторхинолоны 1–2-го поколения не имеют антипневомококковой активности. А, например, у левофлоксацина с его широчайшим спектром активности есть все шансы уничтожить микробиом, в том числе респираторный.
Все существующие современные рекомендации предлагают придерживаться ключевого принципа антибиотикотерапии — принципа минимальной достаточности. То есть уничтожить только наиболее вероятного возбудителя, не затрагивая микробиом. Важно учитывать бактерицидную активность препарата, его токсичность, биодоступность и концентрацию непосредственно в слизистой.
Ошибка № 3
Необоснованное назначение парентерального антибиотика для лечения нетяжелых инфекций или препарата с низкой биодоступностью
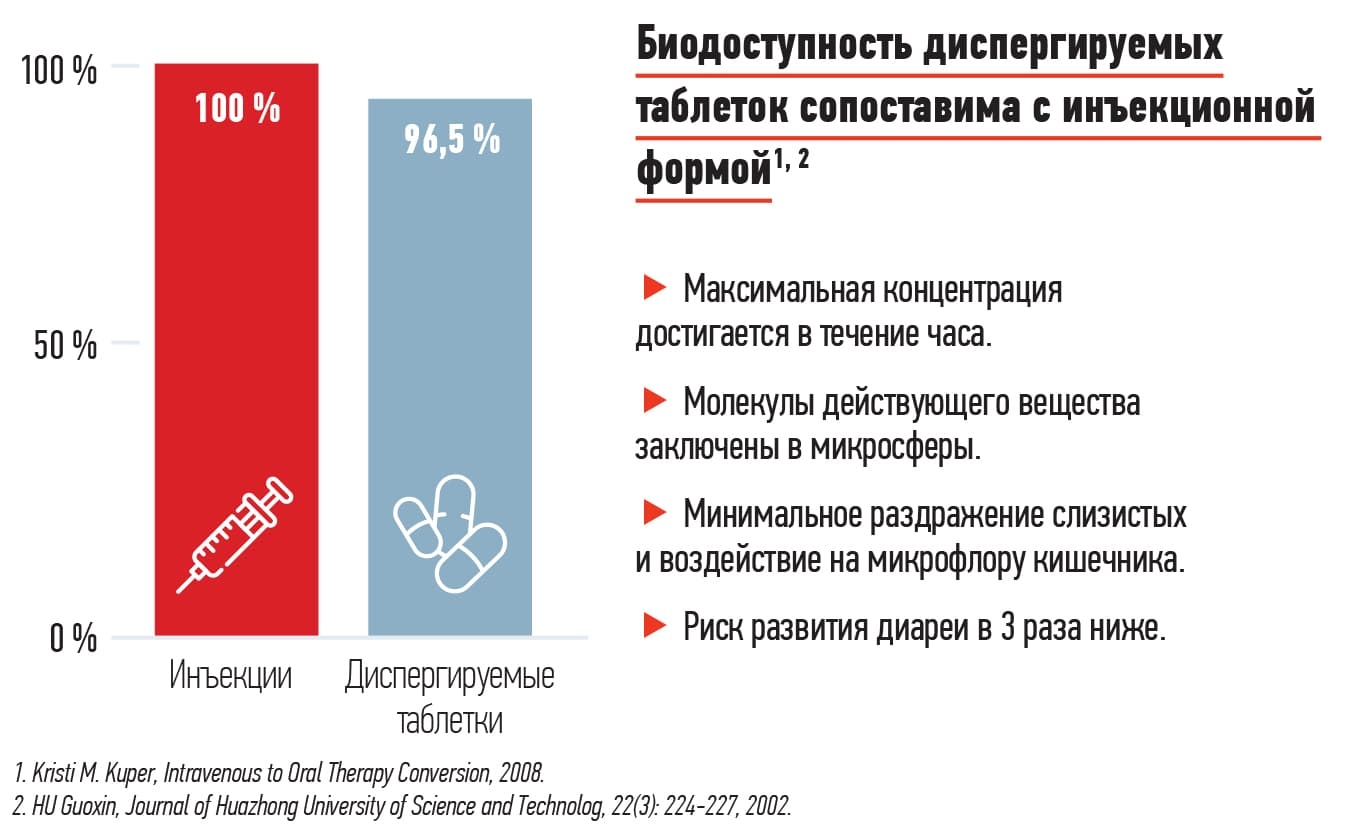
Целый ряд исследований показал, что нет никаких принципиальных отличий между назначением препарата с адекватной биодоступностью и внутривенных или внутримышечных лекарственных средств у пациента с нетяжелым течением инфекции. Тем более многие антибиотики сегодня имеют диспергируемые формы (см. рис. 3).
Рисунок 3. Биодоступность диспергируемых таблеток.
Дмитрий Рузанов:
Диспергируемые таблетированные антибиотики имеют близкую к 100 % биодоступность, создают низкую концентрацию в просвете кишечника, а значит меньше влияют на кишечную микрофлору.
Пример нерационального выбора антибиотика для лечения респираторной инфекции — пероральный ампициллин (см. рис. 4). Его биодоступность составляет не более 40 %, а при приеме с пищей — лишь 15–20 %. Вроде название созвучное, тоже аминопенициллин и спектр активности такой же, как и у амоксициллина, но тем не менее его не стоит применять в лечении респираторных инфекций из-за низкой биодоступности, подчеркнул специалист.
Рисунок 4. Нерациональный выбор антибиотика для лечения респираторной инфекции.
Ошибка № 4.
Погрешности в дозировании и кратности приема антибиотиков
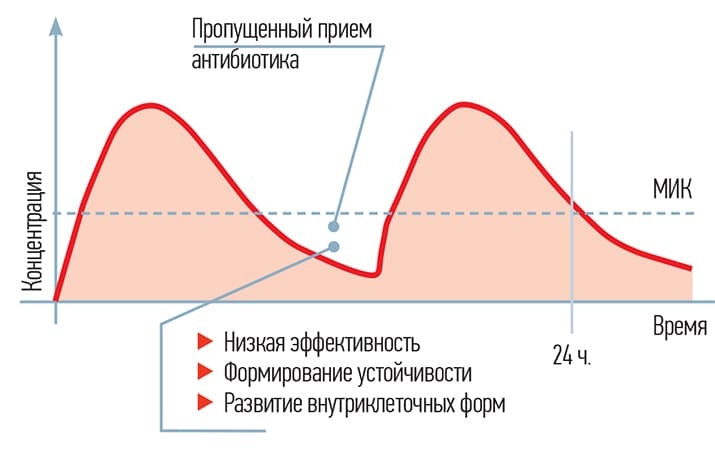
Следует также помнить о фармакокинетической кривой. Большую часть времени она должна быть выше минимальной ингибирующей концентрации. Что происходит, когда она снижается? В первую очередь, что наиболее нежелательно, формируется устойчивость, нет должной эффективности, некоторые возбудители «сохраняются» внутриклеточно.
Дмитрий Рузанов:
Назначая амоксициллин по таблетке 3 раза в день, мы сохраняем концентрацию выше минимальной ингибирующей. Но стоит пациенту пропустить одну дозу, и концентрация снижается ниже минимальной ингибирующей. По данным исследований, пропуск третьего приема наблюдается почти в половине случаев. Через несколько дней такого приема возможна и отрицательная динамика из-за формирования устойчивости (см. рис. 5).
Двукратный прием лекарственных средств увеличивает приверженность пациента в сравнении с более частым. Как выход, допустимо назначать антибиотики в более высокой дозировке, например, амоксициллин по 1000 мг 2 раза в день. Ряд исследований демонстрируют меньшее количество клинических неудач в лечении инфекций при таком варианте дозы и кратности.
Рисунок 5. Фармакокинетическая кривая амоксициллина.
Ошибка № 5
Нерациональное назначение вместе с антибиотиком патогенетического лечения: избыточная противовоспалительная, иммуностимулирующая и отхаркивающая терапия
Нерациональной патогенетической терапией можно навредить. Пациент с респираторной инфекцией при повышении температуры практически всегда будет использовать аспирин, парацетамол или другие НПВС. Реклама настойчиво велит это делать!
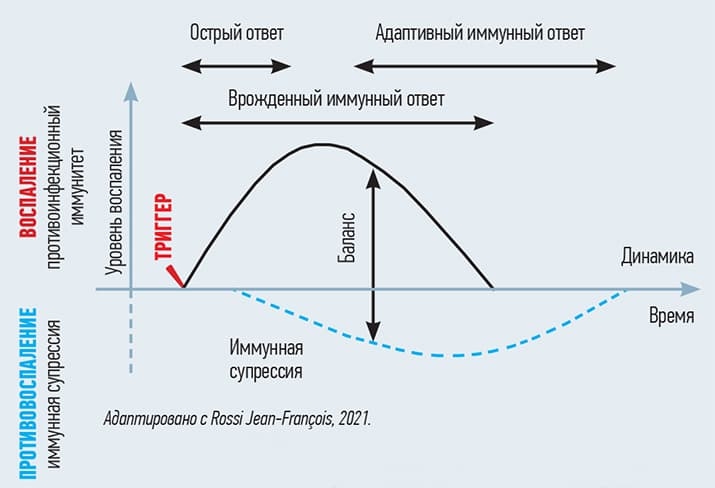
Но воспаление при респираторном заболевании спасает жизнь пациента, с его помощью организм борется с инфекцией (см. рис. 6).
Рисунок 6. Динамика нормальной воспалительной реакции — хорошее воспаление.
Противовоспалительные же препараты дают обратный эффект и нередко приводят к затяжному и осложненному течению инфекции. Рекомендация всем хорошо известна — если лихорадка не изнуряет пациента и не выше 38,5 °С, НПВС не используются при условии достаточной водной нагрузки.
Дмитрий Рузанов:
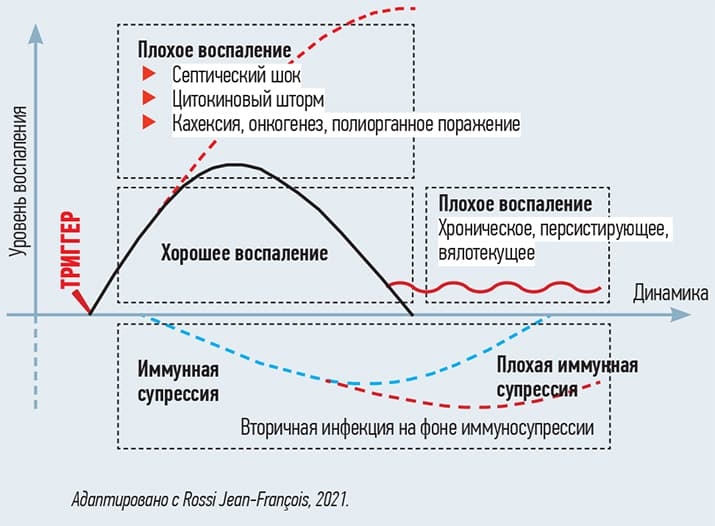
Есть хорошее воспаление, но есть и плохое (например, при коронавирусной инфекции в виде цитокинового шторма). Плохое воспаление может персистировать после перенесенной респираторной инфекции — у пациента продолжается лихорадка, сохраняются респираторные симптомы. Это нарушение баланса между про- и противовоспалительной реакцией (см. рис. 7).
Рисунок 7. Иммунный дисбаланс плохого воспаления.
Но не нужно впадать и в другую крайность — рутинно стимулировать провоспалительную активность организма. Все постсоветское пространство, по словам Дмитрия Рузанова, отличается стремлением стимулировать иммунитет при инфекциях. Особенно в педиатрической практике.
Стоит ребенку пойти в садик, он абсолютно естественно, сталкиваясь с незнакомыми инфекциями, начинает болеть, у него формируется иммунитет, но тут на него обрушивается весь богатый арсенал фармацевтического рынка в виде иммуностимулирующей терапии. Растут и риски «расплаты» за эту провоспалительную активность — дебютом через несколько месяцев аллергических и аутоиммунных заболеваний.
Дмитрий Рузанов:
Я не хочу сказать, что такой вид терапии не должен применяться! Но вдумчиво, контролируемо и индивидуально, не забывая о балансе про- и противовоспалительной активности.
И в завершение часто используемая мукоактивная терапия. Самый простой анализ показывает, что лидерами продаж являются лекарственные средства на основе трав, рефлекторные отхаркивающие препараты.
Доказательства эффективности использования растительных экспекторантов отсутствуют, а побочные эффекты превышают возможную пользу.
Ситуация складывается следующая. К врачу приходит пациент с жалобами на сильный кашель с большим количеством выделяемой мокроты уже на протяжении нескольких недель. В анамнезе ОРИ. Доктор предполагает различные диагнозы, ломает голову, как лечить, не пора ли использовать антибиотики. А все очень просто! Пациент пошел в аптеку и купил «безопасные» растительные отхаркивающие, которые быстро «помогли» — мокроты стало много, правда, и кашель усилился, да еще и изжога появилась. Увы, это миф — чем больше мокроты, тем эффективнее «очищение».
ВОЗ в общеврачебной практике рекомендует при назначении антибиотиков в качестве мукоактивной терапии использовать ацетилцистеин. Этот препарат обладает целым рядом важных патогенетических эффектов, в том числе препятствует формированию биопленок.
- Ацетилцистеин обладает клинически значимыми антибактериальными свойствами.
- За счет предотвращения адгезии обладает профилактическими свойствами в отношении бактериальных инфекций.
- Синергизм при совместном использовании с антибиотиками.
Однако важно помнить об особенностях его использования.
Рекомендации по приему ацетилцистеина при ОРИ:
- Начинать в первый день острой респираторной инфекции, продолжительность от одной до четырех недель в дозе не менее 600 мг.
- Последний вечерний прием должен быть не позднее 18–19 часов для дополнительной активности по эвакуации секрета.
- Для улучшения дренажной функции бронхов через 60 минут после приема рекомендовать пациенту активно покашлять, провести дыхательную гимнастику.
- Показаны кинезотерапия, вибрационный массаж. Особенно их проведение важно у больных пожилого возраста со сниженным кашлевым рефлексом и у детей.
Вопрос от слушателей
«Амоксициллин или амоксиклав? Как в двух словах их разграничить и определить нишу для каждого?»
Д. Р.: Все просто: если в анамнезе были антибиотики последние 3 месяца, а также если это коморбидный пациент или возраст старше 60 лет, то стоит назначать амоксициллин, защищенный клавулановой кислотой. В остальных случаях достаточно амоксициллина (см. рис. 8).
Рисунок 8. Что выбрать: амоксициллин или амоксиклав?
Только цифры
Повлияла ли пандемия COVID-19 на потребление антибиотиков?
На этот вопрос Дмитрий Рузанов однозначно ответил положительно. В качестве примера привел такие данные: в 2021 году амбулаторное потребление антибиотиков выросло почти в 1,5 раза, а количество использованного азитромицина увеличилось в 3,4 раза. Естественно, рост потребления антибиотиков в популяции является риском роста антибиотикорезистентности. И общая задача — в постковидную эру вернуться на рельсы бережного и рационального отношения к антибиотикам.
Термин антибиотик в переводе с греческого означает «против жизни». Действительно, этот тип препаратов уничтожает бактерии. Первый антибиотик, пенициллин, открытый в 1928 году, стал настоящим прорывом в медицине. Благодаря антибиотикотерапии стали излечимыми тяжелейшие инфекционные заболевания, например, туберкулез и чума, которые ранее часто приводили к смерти.
Многим кажется, что антибиотики излечивают все. Поэтому всякий раз, когда в организме появляется инфекция, такие люди бегут не к врачу, а в аптеку за антибиотиками. Действительно, правильно подобранные таблетки быстро уменьшают симптомы заболевания, но этот тип препаратов следует применять только в строго определенных случаях. Например, они не подходят для лечения вирусов.
Не секрет, что россияне злоупотребляют антибиотиками – мы находимся на переднем крае европейских стран, где антибиотики прописывают, когда надо и не надо.
Когда использовать антибиотики?
Антибиотики могут быть бактериостатическими или бактерицидными. В первом случае они препятствуют размножению бактерий, во втором – они уничтожают живые клетки. При этом антибиотики эффективны только тогда, когда инфекция вызвана бактериями. Поэтому назначение антибиотика должно происходить только тогда, когда врач уверен, что инфекция бактериальная.
К сожалению, тесты, подтверждающие этиологию инфекции, проводятся редко. При назначении антибиотика врачи обычно полагаются на конкретные симптомы бактериальной инфекции и место возникновения инфекции, зная, что определенные группы бактерий вызывают определенные симптомы.
Если у врача есть сомнения относительно происхождения заболевания, он обязан назначить анализ, подразумевающий посев биологической жидкости, например, мокроты, на специальную питательную среду. На таких средах бактерии быстро разрастаются, образуя колонии, хорошо различимые под микроскопом.
Затем можно воздействовать на выявленные бактерии разными антибиотиками, чтобы понять, какой из них будет уничтожать обнаруженный вид бактерий. Такой же анализ необходимо провести, если лечение уже назначенным антибиотиком остается неэффективным.
Ошибки при антибиотикотерапии
Успех лечения антибиотиками зависит как от правильного типа препарата, так и от способа его приема. Наиболее распространенные ошибки, допускаемые пациентами во время лечения антибиотиками, включают в себя:
Ошибка 1. Несоблюдение сроков приема препарата
Антибиотики следует принимать через регулярные промежутки времени – каждые 24, 12 или 8 часов в зависимости от типа. Благодаря регулярной дозе препарата их концентрация в организме постоянна, и бактерии не могут размножаться.
Делая слишком много перерывов, пациент дает им время для дальнейшего развития, что задерживает процесс выздоровления.
Ошибка 2. Несоблюдение полного курса лечения
Антибиотики всегда следует принимать до конца, то есть столько, сколько предписано врачом. Обычно лечение антибиотиками длится 8-10 дней, хотя лечение инфекции мочевого пузыря может быть ограничено 3 днями. Пациенты часто бросают лечение антибиотиками в середине курса, как только почувствуют себя лучше.
Это неправильно, так как значительно увеличивает вероятность того, что бактерии вызовут рецидив заболевания.
Ошибка 3. Отсутствие защиты пищеварительной системы
Антибиотики смертельны не только для болезнетворных бактерий, но и для бактерий, которые колонизируют в пищеварительной системе и полезны для нашего здоровья. Результатом стерилизации организма является постантибиотическая диарея.
В рамках защиты полезных бактерий следует принимать защитные препараты – пробиотики как в виде лекарственных препаратов, так и натуральные – йогурт, кефир. Пробиотические препараты следует принимать примерно через час после введения антибиотика. Они также могут быть использованы после окончания антибиотикотерапии для ускорения восстановления бактериальной флоры в пищеварительной системе.
Устойчивость к антибиотикам – почему не проходит болезнь
В последние годы специалисты бьют тревогу по поводу злоупотребления антибиотиками, из-за чего патогенные бактерии становиться устойчивыми к антибиотикотерапии. Чаще всего пациенты принимают таблетки, путая бактериальную инфекцию с вирусной.
Пример, когда антибиотики не помогут – очень распространенные болезни: бронхит, фарингит, синусит, отит. Подавляющее большинство случаев острого бронхита – около 95% – вызвано вирусами. То же самое относится к острому синуситу и острому фарингиту – в этих случаях вирусы вызывают около 80% случаев. Также нет смысла вводить антибиотик при среднем отите, по крайней мере, на первом этапе, который вызван вирусами. Только со временем могут развиться осложнения, для лечения которых необходим антибиотик.
На практике, однако, такие заболевания, особенно если они касаются детей, часто лечат антибиотиком, хотя для этого нет причины – антибиотики не предотвратят бактериальную инфекцию. Они только научат бактерии бороться. И в следующий раз, когда действительно потребуется антибиотикотерапия, она не поможет! Это еще одна причина, по которой этот класс препаратов следует применять только тогда, когда это действительно необходимо.
Проблема рациональной антибактериальной терапии инфекций дыхательных путей не теряет актуальности и в настоящее время. Наличие большого арсенала антибактериальных препаратов, с одной стороны, расширяет возможности лечения различных инфекций, а с другой — требует от врача-клинициста осведомленности о многочисленных антибиотиках и их свойствах (спектр действия, фармакокинетика, побочные эффекты и т. д.), умения ориентироваться в вопросах микробиологии, клинической фармакологии и других смежных дисциплинах.
Согласно И. В. Давыдовскому, «врачебные ошибки — род добросовестных заблуждений врача в его суждениях и действиях при исполнении им тех или иных специальных врачебных обязанностей». Ошибки в антибактериальной терапии инфекций дыхательных путей имеют наибольший удельный вес в структуре всех лечебно-тактических ошибок, совершаемых в пульмонологической практике, и оказывают существенное влияние на исход заболевания. Кроме того, неправильное назначение антибактериальной терапии может иметь не только медицинские, но и различные социальные, деонтологические, экономические и другие последствия.
При выборе способа антибактериальной терапии в амбулаторной практике необходимо учитывать и решать как тактические, так и стратегические задачи. К тактическим задачам антибиотикотерапии относится рациональный выбор антибактериального препарата, обладающего наибольшим терапевтическим и наименьшим токсическим воздействием.
Стратегическая задача антибиотикотерапии в амбулаторной практике может быть сформулирована как уменьшение селекции и распространения резистентных штаммов микроорганизмов в популяции.
В соответствии с этими положениями следует выделять тактические и стратегические ошибки при проведении антибактериальной терапии инфекций дыхательных путей в амбулаторной практике (см. таблицу 1).
| Таблица 1. Ошибки антибактериальной терапии в амбулаторной практике. | |
| Тактические ошибки | Стратегические ошибки |
|
Планирование антибактериальной терапии без учета региональных тенденций резистентности возбудителей |
Тактические ошибки антибактериальной терапии
I. Необоснованное назначение антибактериальных средств
Особую категорию ошибок представляет неоправданное применение антибактериальных препаратов (АП) в тех ситуациях, когда их назначение не показано.
Показанием для назначения антибактериального препарата является диагностированная или предполагаемая бактериальная инфекция.
Наиболее распространенная ошибка в амбулаторной практике — назначение антибактериальных препаратов при острых респираторных вирусных инфекциях (ОРВИ), имеющее место как в терапевтической, так и в педиатрической практике. При этом ошибки могут быть обусловлены как неправильной трактовкой симптоматики (врач принимает ОРВИ за бактериальную бронхолегочную инфекцию в виде пневмонии или бронхита), так и стремлением предотвратить бактериальные осложнения ОРВИ.
При всех трудностях принятия решения в подобных ситуациях необходимо отдавать себе отчет в том, что антибактериальные препараты не оказывают влияния на течение вирусной инфекции и, следовательно, их назначение при ОРВИ не оправдано (см. таблицу 2). В то же время предполагаемая возможность предотвращения бактериальных осложнений вирусных инфекций с помощью назначения антибактериальных препаратов не находит себе подтверждения в клинической практике. Кроме того, очевидно, что широкое неоправданное применение антибактериальных препаратов при ОРВИ чревато формированием лекарственной устойчивости и повышением риска возникновения нежелательных реакций у пациента.
| Таблица 2. Инфекционные заболевания дыхательных путей преимущественно вирусной этиологии и не требующие антибактериальной терапии. | |
| Инфекции верхних дыхательных путей | Инфекции нижних дыхательных путей |
|
Острый бронхит |
Одной из распространенных ошибок при проведении антибактериальной терапии является назначение одновременно с антибиотиком противогрибковых средств с целью профилактики грибковых осложнений и дисбактериоза. Следует подчеркнуть, что при применении современных антибактериальных средств у иммунокомпетентных пациентов риск развития грибковой суперинфекции минимален, поэтому одновременное назначение антимикотиков в этом случае не оправдано. Комбинация антибиотика с противогрибковым средством целесообразна только у больных, получающих цитостатическую или противоопухолевую терапию или у ВИЧ-инфицированных пациентов. В этих случаях оправдано профилактическое назначение антимикотиков системного действия (кетоконазол, миконазол, флуконазол), но не нистатина. Последний практически не всасывается в желудочно-кишечном тракте и не способен предотвратить грибковую суперинфекцию иной локализации — полости рта, дыхательных или мочевыводящих путей, половых органов. Часто практикующееся назначение нистатина с целью профилактики дисбактериоза кишечника вообще не находит логического объяснения.
Часто врач назначает нистатин или другой антимикотик в случае обнаружения в полости рта или в моче грибов рода Сandida. При этом он ориентируется лишь на данные микробиологического исследования и не учитывает наличие или отсутствие симптомов кандидоза, а также факторов риска развития грибковой инфекции (тяжелый иммунодефицит и др.).
Выделение грибов рода Сandida из полости рта или мочевых путей пациентов в большинстве случаев служит свидетельством бессимптомной колонизации, не требующей коррегирующей противогрибковой терапии.
II. Ошибки в выборе антибактериального препарата
Пожалуй, наибольшее число ошибок, возникающих в амбулаторной практике, связано с выбором антибактериального средства. Выбор антибиотика должен производиться с учетом следующих основных критериев:
- спектр антимикробной активности препарата in vitro;
- региональный уровень резистентности возбудителей к антибиотику;
- доказанная в ходе контролируемых клинических исследований эффективность;
- безопасность препарата.
Определяющим фактором выбора препарата должен быть спектр природной активности антибиотика: необходимо, чтобы он охватывал основных возбудителей внебольничных инфекций дыхательных путей (см. таблицу 3).
Кроме того, при выборе препарата следует учитывать уровень приобретенной резистентности возбудителей в популяции. Основные тенденции, касающиеся резистентности возбудителей, отмеченной в последние годы, отражены в таблице 4. Наиболее значимые проблемы, связанные с применением основных антибактериальных средств при инфекциях дыхательных путей, могут быть сформулированы следующим образом.
β-лактамы:
- высокая активность in vitro против основных возбудителей, за исключением атипичных;
- невысокий уровень резистентности в Центральной России (настораживает однако тенденция к его увеличению);
- надежная клиническая и бактериологическая эффективность.
Макролиды:
- рост резистентности S. pneumoniae и S. pyogenes; устойчивость может сопровождаться снижением клинической эффективности;
- низкая активность против H. influenzae — высокая частота бактериологического неуспеха терапии (персистирование возбудителей).
Ранние фторхинолоны:
- низкая природная активность против S. pneumoniae и S. pyogenes;
- рост резистентности S. pneumoniae.
Новые фторхинолоны:
- высокая активность против S. pneumoniae, в том числе штаммов, устойчивых к пенициллину и макролидам; устойчивость минимальна.
Ко-тримоксазол:
- высокий уровень резистентности S. pneumoniae и H. influenzae.
Тетрациклины:
- высокий уровень устойчивости S. pneumoniae.
С учетом вышесказанного, оптимальными средствами для лечения внебольничных инфекций дыхательных путей в настоящее время могут быть признаны β-лактамные антибиотики и новые фторхинолоны (см. таблицу 5). Использование макролидов должно быть ограничено — препараты можно назначать при нетяжелой пневмонии у детей или пациентов молодого возраста, особенно при наличии признаков атипичного течения (микоплазменная, хламидийная).
 |
| Таблица 5. Значение антибактериальных средств при инфекциях нижних дыхательных путей в амбулаторной практике. |
Следует подчеркнуть, что назначение некоторых антибактериальных препаратов, применяемое в амбулаторной практике при респираторных инфекциях, нельзя признать рациональным. К таким препаратам прежде всего относятся:
- гентамицин — отсутствие активности в отношении наиболее частого возбудителя S. pneumoniae и потенциально высокая токсичность;
- ко-тримоксазол — высокий уровень резистентности S. pneumoniae и H. Influenzae;
- ранние фторхинолоны (ципрофлоксацин, офлоксацин, пефлоксацин, ломефлоксацин) — низкая активность против S. pneumoniae;
- пероральные цефалоспорины III поколения (цефтибутен) — низкая активность против S. pneumoniae;
- ампиокс — нерациональная комбинация, дозы ампициллина и оксациллина (по 0,125 мг) значительно ниже терапевтических.
В таблице 6 приведены современные рекомендации по антибактериальной терапии внебольничных респираторных инфекций, с учетом всех требуемых критериев и доказанной эффективности в контролируемых клинических исследованиях.
Представленные рекомендации имеют наиболее общий характер. В то же время с практических позиций выбор оптимального антибактериального препарата также должен осуществляться с учетом особенностей пациента и заболевания. Так, например, у больных пневмонией молодого и среднего возраста без отягощающих факторов терапевтический эффект оказывают амоксициллин, макролиды, защищенные пенициллины и новые фторхинолоны. Однако у больных пожилого возраста в этиологии заболевания большее значение приобретают S. aureus и грамотрицательные бактерии, что объясняет снижение эффективности амоксициллина и макролидов у этой категории больных.
Также распространенной во врачебной практике ошибкой является отказ от назначения антибактериальной терапии при пневмонии беременным женщинам из-за опасения негативного влияния препаратов на плод. Следует отметить, что перечень антибактериальных препаратов, прием которых нежелателен во время беременности из-за риска эмбриотоксического действия, ограничен — тетрациклины, хлорамфеникол, сульфаниламиды, ко-тримоксазол, фторхинолоны, аминогликозиды. Другие антибиотики, в частности β-лактамы, макролиды, могут применяться у беременных женщин.
Другие возможные факторы, влияющие на выбор антибактериального препарата, представлены в таблице 7.
 |
| Таблица 7. Особые клинические ситуации при внебольничных инфекциях нижних дыхательных путей. |
Нередки ошибки при выборе антибактериального препарата в случае неэффективности первоначального. Здесь необходимо также остановиться на ошибках антибактериальной терапии, которые касаются несвоевременной оценки неэффективности первоначального антибиотика. Общепринятым критическим сроком оценки эффективности (или неэффективности) антибактериальной терапии считаются 48—72 ч с момента его назначения. К сожалению, приходится нередко сталкиваться с такими случаями, когда больной продолжает получать назначенный антибиотик в течение недели и более, несмотря на отсутствие очевидного клинического эффекта. Обычно критерием эффективности антибактериальной терапии является снижение или нормализация температуры тела больного, уменьшение признаков интоксикации. В тех случаях (не столь частых), когда лихорадка с самого начала заболевания отсутствует, приходится ориентироваться на другие признаки интоксикации (головная боль, анорексия, общемозговая симптоматика и т. д.), а также на отсутствие прогрессирования заболевания за период проводимого лечения.
Продолжение антибактериальной терапии, невзирая на ее неэффективность, имеет немало негативных последствий. При этом затягивается назначение другого, более адекватного антибиотика, что ведет к прогрессированию воспаления (особенно важно при тяжелых пневмониях, у больных с сопутствующей патологией) и развитию осложнений, а также удлиняет сроки лечения. Кроме того, повышается риск возникновения побочных (токсических) эффектов препаратов, а также развития и усиления антибиотикорезистентности. Продолжение лечения, несмотря на неэффективность проводимой терапии, подрывает доверие больного и его родственников к лечащему врачу. Очевидна и неэкономичность такой ошибочной тактики антибактериальной терапии (напрасный расход неэффективного АП, дополнительные затраты на лечение токсических эффектов и др.).
Кроме того, ошибки встречаются при замене неэффективного антибиотика на другой, т. е. при смене препарата. При этом врач забывает, что принцип выбора антибактериального препарата остается прежним, т. е. ориентироваться следует на клиническую ситуацию с учетом, однако, неэффективности первоначального препарата и ряда других дополнительных признаков. Отсутствие эффекта от первоначально назначенного антибиотика в известной степени должно служить дополнительным ориентиром, позволяющим обосновать выбор второго препарата. Так, например, отсутствие эффекта от применения β-лактамных антибиотиков (пенициллины, цефалоспорины) у больного с внебольничной пневмонией позволяет предполагать атипичную этиологию пневмонии (микоплазменной, хламидийной или легионеллезной) с учетом, разумеется, других клинических признаков.
Клинические признаки атипичной пневмонии, вызванной Mycoplasma pneumoniae или Chlamydia pneumoniae:
- постепенное начало (в течение трех—семи дней);
- часто субфебрильная температура;
- непродуктивный кашель;
- отсутствие гнойной мокроты;
- внелегочная симптоматика (фарингит, миалгии, головная боль, диарея);
- интерстициальные инфильтраты;
- двустороннее поражение.
Наличие клинических признаков атипичной пневмонии делает обоснованным назначение антибактериальных препаратов из группы макролидов, доксициклина или фторхинолонов (левофлоксацин, моксифлоксацин, офлоксацин).
III. Ошибки в выборе режима дозирования антибактериального препарата
Ошибки в выборе оптимальной дозы антибактериального средства могут заключаться в назначении как недостаточной, так и избыточной дозы препарата. И те и другие ошибки чреваты негативными последствиями.
Если доза антибиотика недостаточна и не создает в крови и тканях дыхательных путей концентрацию, превышающую минимальную дозу для подавления основных возбудителей инфекции, что является условием эрадикации соответствующего возбудителя, то это не только может служить одной из причин неэффективности терапии, но и создает реальные предпосылки для формирования резистентности микроорганизмов. Ошибки в выборе оптимальной дозы могут быть связаны как с назначением недостаточной разовой дозы, так и с неправильным режимом дозирования (недостаточная кратность введения).
В качестве примера неадекватного режима дозирования антибиотиков при внебольничной пневмонии можно привести амоксициллин, который ранее рекомендовался в суточной дозе до 1 г. Однако современные рекомендации предполагают назначение амоксициллина в суточной дозе 1,5 и даже 3 г для преодоления возможной резистентности S. pneumoniae. Примеры неадекватных режимов дозирования антибиотиков в амбулаторной практике при респираторных инфекциях приводятся в таблице 8.
 |
| Таблица 8. Неадекватные режимы дозирования пероральных антибактериальных препаратов в амбулаторной практике при респираторных инфекциях у взрослых. |
Неправильный выбор интервалов между введениями антибактериальных препаратов обычно обусловлен не столько сложностями парентерального введения препаратов в амбулаторных условиях или негативным настроем больных, сколько неосведомленностью практикующих врачей о некоторых фармакодинамических и фармакокинетических особенностях препаратов, которые должны определять режим их дозирования. Типичной ошибкой является назначение в амбулаторной педиатрической практике при пневмонии бензилпенициллина с кратностью введения два раза в сутки, так как более частое его введение неудобно для пациента. Следует отметить, что при нетяжелом течении пневмонии вряд ли оправдано стремление некоторых врачей к обязательному назначению парентеральных антибиотиков. Современные антибактериальные препараты характеризуются хорошей биодоступностью при приеме внутрь, а также одинаковой клинической эффективностью с парентеральными препаратами, поэтому в подавляющем большинстве случаев оправдано лечение пероральными препаратами. Если назначение парентеральных антибиотиков действительно необходимо, следует выбрать препарат с длительным периодом полувыведения (например, цефтриаксон), что позволяет назначать его один раз в сутки.
IV. Ошибки при комбинированном назначении антибиотиков
Одной из ошибок антибактериальной терапии внебольничных респираторных инфекций является необоснованное назначение комбинации антибиотиков. Врачи старших поколений помнят то время (50—70-е гг. прошлого столетия), когда при лечении пневмонии обязательным считалось назначение пенициллина и стрептомицина, о чем свидетельствовали многие учебные пособия и руководства. Это был своеобразный стандарт лечения пневмоний для того времени. Несколько позднее одновременно с антибиотиками рекомендовалось назначение сульфаниламидов, с учетом полученных в свое время З. В. Ермольевой данных о химиотерапевтическом синергизме сульфаниламидов и пенициллина.
В современной ситуации, при наличии большого арсенала высокоэффективных антибактериальных препаратов широкого спектра, показания к комбинированной антибактериальной терапии значительно сужены, и приоритет в лечении респираторных инфекций остается за монотерапией. В многочисленных контролируемых исследованиях показана высокая клиническая и бактериологическая эффективность адекватных антибактериальных средств при лечении респираторных инфекций в режиме монотерапии (амоксициллин, амоксициллин/клавуланат, цефалоспорины II-III поколений, новые фторхинолоны). Комбинированная антибактериальная терапия не имеет реальных преимуществ ни в выраженности эффекта, ни в предотвращении развития резистентных штаммов.
Основными показаниями к комбинированной антибактериальной терапии являются тяжелое течение пневмонии — в этом случае общепринятым стандартом лечения становится комбинированное назначение парентерального цефалоспорина III поколения (цефотаксим или цефтриаксон) и парентерального макролидного антибиотика (эритромицин, или кларитромицин, или спирамицин); последние включаются в комбинацию для воздействия на вероятных атипичных микроорганизмов (легионелла или микоплазма). Следует отметить, что в настоящее время в клинической практике появились новые антибактериальные препараты (левофлоксацин, моксифлоксацин) с высокой активностью в отношении как типичных, так и атипичных возбудителей, что позволяет назначать их в режиме монотерапии даже при тяжелой пневмонии.
Другой клинической ситуацией, оправдывающей комбинированное назначение антибиотиков, является пневмония у иммунокомпрометированных пациентов (лечение цитостатиками, СПИД), при которой имеется высокая вероятность ассоциации возбудителей (см. таблицу 7).
К сожалению, часто в амбулаторной практике приходится сталкиваться с ситуациями, при которых больным с нетяжелым течением пневмонии, при отсутствии осложнений, тяжелой фоновой патологии назначается два антибиотика. Логичного обоснования этой тактики лечения нет, при этом следует учитывать возможный антагонизм препаратов, более высокий риск нежелательных реакций и увеличение стоимости лечения.
Следует отметить, что нерациональные комбинации антибактериальных препаратов имеют и официальные лекарственные формы, которые выпускаются отечественной фармацевтической промышленностью, например ампиокс, олететрин. Разумеется, применение таких препаратов недопустимо.
V. Ошибки, связанные с длительностью антибактериальной терапии и критериями клинической эффективности
В некоторых случаях проводится необоснованно длительная антибактериальная терапия. Такая ошибочная тактика обусловлена, прежде всего, недостаточным пониманием цели самой антибактериальной терапии, которая сводится прежде всего к эрадикации возбудителя или подавлению его дальнейшего роста, т. е. направлена на подавление микробной агрессии.
Собственно воспалительная реакция легочной ткани, которая проявляется различными клинико-рентгенологическими признаками (аускультативная картина, сохраняющаяся рентгенологическая инфильтрация, ускорение СОЭ) регрессирует медленнее и не требует продолжения антибактериальной терапии (см. таблицу 9). В связи с этим следует считать ошибочной тактику, согласно которой у больногос сохраняющимися рентгенологическими признаками легочной инфильтрации, крепитирующими хрипами (crepitacio redux), увеличением СОЭ при нормализации температуры тела и исчезновении (или уменьшении) признаков интоксикации продолжают проводить антибактериальную терапию.
 |
| Таблица 9. Сроки исчезновения симптомов при эффективной антибактериальной терапии внебольничной пневмонии. |
Еще более ошибочна тактика замены одного антибиотика на другой в подобных ситуациях, расцениваемых врачом как неэффективность назначенной антибактериальной терапии. У некоторых больных после исчезновения признаков интоксикации и даже регрессии воспалительных изменений в легких в течение длительного времени может сохраняться слабость, потливость, субфебрильная температура. Последняя расценивается врачом как проявление не полностью купированной бронхолегочной инфекции, что «подтверждается» рентгенологическими данными в виде изменения легочного рисунка или «остаточными явлениями пневмонии» и обычно влечет за собой назначение антибактериального препарата, несмотря на отсутствие изменений со стороны крови. Между тем подобная клиническая ситуация часто обусловлена вегетативной дисфункцией после легочной инфекции (постинфекционная астения) и не требует антибактериальной терапии, хотя, разумеется, в каждом конкретном случае необходимы тщательное обследование больного и расшифровка всей имеющейся симптоматики.
Рекомендованная длительность применения антибактериальных препаратов при бронхолегочных инфекциях приведена в таблице 10.
 |
| Таблица 10. Длительность антибактериальной терапии бактериальных респираторных инфекций в амбулаторной практике. |
Л. И. Дворецкий, доктор медицинских наук, профессор
С. В. Яковлев, доктор медицинских наук, профессор
ММА им. И. М. Сеченова, Москва
Врачи медицинского центра Доверие разработали памятку для своих пациентов в которой указаны основные ошибки при приёме антибиотиков. Как и все врачи мира – настойчиво рекомендуем – не занимайтесь самолечением! Не злоупотребляйте приёмом антибиотиков! Добавьте памятку себе в закладки, положите её к себе в аптечку, дайте почитать близким и знакомым.
Итак, какие основные ошибки при приёме антибиотиков совершают родители
- Нельзя назначать ребёнку антибиотики на свое усмотрение, без консультации врача. Решение принимает только врач (и не фармацевт в аптеке).
- Нельзя лечить ребёнка антибиотиками без осмотра врача и анализов. Должно быть установлено, что природа заболевания — бактериальная (осмотр врача, клинический анализ крови и т.д).
- Нельзя давать ребёнку антибиотики от вирусных инфекций и температуры. Антибиотики не воздействуют на вирусы, не являются жаропонижающим средством!
- Нельзя пренебрегать приемом антибиотиков, назначенных врачом. Некоторые заболевания, такие как воспаление легких, острый гнойный синусит, острый средний отит (до 6 месяцев), паратонзиллит всегда являются основанием для назначения антибиотиков.
- Надо обязательно учитывать предшествующее лечение. Назначая антибиотики, нужно учитывать, какие антибактериальные препараты получал ребенок в течение 3 предыдущих месяцев, а также вероятные варианты причин заболеваний, характерные для конкретного региона.
- Надо учитывать особенности здоровья и факторы риска при выборе препарата. Каждый препарат имеет свой спектр действия, возрастные и другие ограничения. Только врач точно определит, какой из них окажет нужное воздействие на организм вашего ребёнка.
- Нельзя по желанию отменять приём антибиотиков. При приеме антибиотиков родители должны проконтролировать, чтобы ребенок прошел полный курс лечения. Улучшение состояния — это не повод отменять прием препаратов, неполный курс повышает риск устойчивости бактерий к этому антибиотику.
- Нельзя корректировать самостоятельно назначенные врачом препараты. При отсутствии должного эффекта от приема антибиотика (в течение 2-3 суток), только врач может заменить препарат или скорректировать дозировку. Основной признак эффективности антибиотика — снижение температуры через 24-48 часов.
- Обязательно надо учитывать возможные побочные эффекты для конкретного организма. В числе возможных побочных эффектов — аллергические реакции, тошнота, рвота, диарея, очень редко псевдомембранозный колит, временное изменение состава кишечной флоры, токсические реакции.
- Не стоит дополнять лечение другими препаратами по своему усмотрению. Другие препараты при использовании антибиотиков назначает доктор (пробиотики, противогрибковые препараты и т.д.), исходя из состояния здоровья ребенка и анамнеза.
- Не следует давать ребёнку антибиотики совместно с жаропонижающими. Для оценки эффективности антибиотика лучше не увлекаться жаропонижающими препаратами, дабы оценить динамику температуры. Правило не применимо с детьми, у которых серьёзное повышение температуры — могут развиться судороги.
- Нельзя закупать антибиотики про запас и принимать всей семьей. Антибиотики не приобретают заранее и не применяют без врачебной рекомендации для других членов семьи!
Берегите себя и своих ребятишек! Своевременная консультация у врача поможет эффективно справиться с заболеванием и предупредит осложнения.
ПОСМОТРЕТЬ ЦЕНЫ √ РАСПИСАНИЕ РАБОТЫ
Записаться на прием, получить консультацию:
+7 (423) 267-61-30; +7 (423) 274-32-22; +7 914-704-32-22.
Записаться на приём он-лайн:
Если остались вопросы, задайте их в форме комментариев ниже↓↓↓
Основные ошибки приема антибиотиков в домашних условиях.
О пользе и вреде антибиотиков ведется немало разговоров, и многие уже давно знают, что у них очень много побочных действий. Они подавляют иммунитет, на фоне их приема может возникнуть аллергическая реакция и развиться дисбактериоз, они вредны для слизистой внутренних органов – и это далеко не полный список. Да, многие знают, что применять их можно и нужно только в случаях тяжелых инфекций. Но применяются они, зачастую, без необходимости и без ведома врача. И этому виной их широкое распространение и легкая доступность, они есть практически в каждом доме.
Сейчас ими принято лечить любую болезнь, начиная от банального насморка и заканчивая золотухой. Не врачами, конечно же, а «обычными смертными», хотя и врачи этим грешат, назначая их, когда нужно и не нужно. Однако же стоит знать самые грубые ошибки в применении антибиотиков, а так же случаи, когда они могут применяться, но не являются обязательными.
Итак, самая серьезная ошибка – применение антибиотиков в случаях острой респираторной вирусной инфекции. Современные антибиотики совершенно никак не действуют на вирус, поэтому их назначение теряет всякий здравый смысл. А если учесть прямое действие антибиотика (снижение естественного иммунитета), то его применение может нанести еще больший вред организму и запустить более тяжелую форму имеющейся болезни. Антибиотики назначаются только при серьезных микробных инфекциях, и только после выявления природы инфекции. А для этого, как минимум, нужно сдать анализы в больничной лаборатории.
Следующая распространенная ошибка – самостоятельное удлинение курса приема антибиотиков. Некоторые люди считают, что если пить антибиотики дольше, то организм станет еще здоровее. Но это далеко не так, антибиотик необходим для борьбы с инфекцией, а не для замещения нормальных (природных) функций организма. Если применение антибиотика в течении 3-4 дней является успешным и состояние человека стабилизируется, то курс следует сократить, а не увеличить.
Многие думают, что антибиотики можно пить для профилактики инфекционных болезней. И это еще одна грубая ошибка обычного человека. Антибиотик предназначен для борьбы с микробной средой в организме. Если он ее не обнаруживает, то начинает разрушаться и от действия продуктов распада страдают внутренние органы человека.
Вопреки распространенному заблуждению, антибиотик не понижает температуру тела и не имеет обезболивающего действия. Для этого есть другие препараты, которые не так вредны для организма. Так же, антибиотик не применяется при расстройствах желудочных функций, если речь не идет об инфекции. Но даже, если это и инфекция, то применение антибиотика находится под вопросом, ответ на который может дать только соответствующий специалист и только после проведения обследования. Кроме того, расстройство может носить вирусный характер, быть проявлением аллергии или отравления, дисбактериозом и многое другое. И в таких случаях, антибиотик просто противопоказан.
Нельзя часто употреблять один и тот же антибиотик. Организм привыкает к его действию и вырабатывается устойчивость, в следующий раз придется выбирать более сильнодействующий препарат.
Ошибочно употреблять какой-то конкретный антибиотик только потому, что он помог в лечении другому человеку. Каждый случай индивидуален и назначение антибиотика должно происходить после проведения обследования.
Об этих ошибках должен знать каждый человек. Только зная, он может защитить свою семью и себя самого от нанесения вреда организму. Да, антибиотики важны и нужны, но только как крайний случай, а не норма при любой болезни.
Вывод
Антибиотики — мощное оружие в борьбе со многими заболеваниями, иногда их применение — единственный способ спасти жизнь. Но человечество, зачастую впадая в крайности, бесконтрольно применяет или же наоборот — полностью отрицает препараты этой группы.
Беспечное отношение ведёт к возникновению суперустойчивых микробов, появление которых фармакологическим компаниям пока что удаётся контролировать, изобретая новые препараты. Однако, за последние два десятилетия было изобретено только два вида антибиотиков нового класса. И если в ближайшем будущем ситуация кардинально не изменится, неэффективное применение существующих антибиотиков при первых симптомах респираторного заболевания неизбежно приведёт к проигрышу человечества в борьбе с резистентными микробами.
Источник : https://монастырёв.рф/
https://polzaivredno.ru/
https://cmtscience.ru/