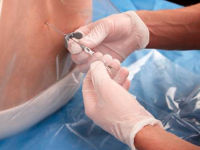
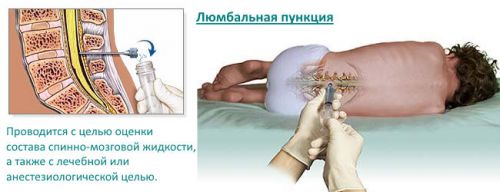
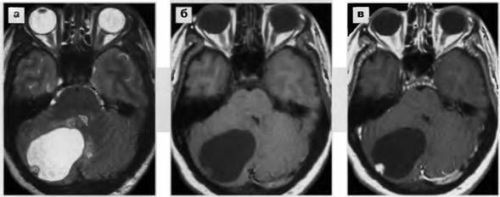
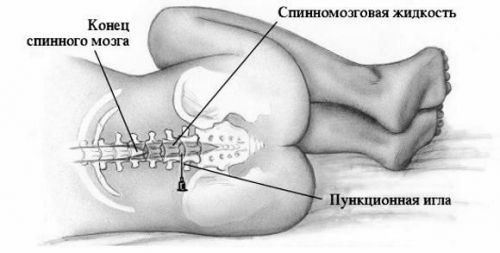
При люмбальной пункции (ЛП) иглу вводят в субарахноидальное пространство спинного мозга поясничного отдела позвоночника с целью сбора спинномозговой жидкости (СМЖ) для лабораторных исследований, измерения давления в СМЖ, а иногда для интратекального введения диагностических или терапевтических агентов.
Если возникают трудности с пальпаторным определением ориентиров (например, из-за ожирения) нейрорадиолог может провести люмбальную пункцию под контролем рентгеноскопии. Ультросонграфию также можно использовать для определения ориентиров и, реже, для контроля правильного положения иглы в режиме реального времени, при наличии оборудования и персонала. Тем не менее ультрасонография все еще редко используется за пределами учебных центров.
Диагностические показания*
-
Подозрение на внутричерепную гипотензию
-
Введении рентгеноконтрастного вещества для миелографии
* Заранее решите, какую информацию вам нужно получить из материала, взятого при поясничной пункции, и какие анализы вам нужно назначить. Перед началом процедуры в клинической лаборатории необходимо подтвердить требования к каким-либо нестандартным тестам.
Терапевтические показания
-
Снижение внутричерепного давления при идиопатической внутричерепной гипертензии
-
Введение интратекальных препаратов (например, спинальная или эпидуральная анестезия, интратекальная химиотерапия)
Абсолютные противопоказания
-
Подозрение на инфекцию (например, флегмона, абсцесс) в месте введения иглы или рядом с ним: по возможности, используйте альтернативный, неинфицированный участок. Это проводится посредством субокципитального (цистернального) или шейного доступа (С1-С2) и всегда выполняется под рентгеноскопическим контролем.
Относительные противопоказания
-
Подозрение на повышенное внутричерепное давление вследствие внутричерепного новвобразования (например, опухоли, абсцесс мозга или кровь), которое может вызвать транстенториальное или мозжечковое вклинивание Вклинение головного мозга Дислокация головного мозга возникает при аномальном выпячивании мозговой ткани через отверстия ригидных преград внутри черепа (например, вклинение в тенториальную выемку), из-за повышенного… Прочитайте дополнительные сведения
* после люмбальной пункции. Если есть подозрительные признаки (например, очаговый неврологический дефицит, изменение психического состояния, отек диска зрительного нерва, признаки грыжи Клинические проявления Дислокация головного мозга возникает при аномальном выпячивании мозговой ткани через отверстия ригидных преград внутри черепа (например, вклинение в тенториальную выемку), из-за повышенного… Прочитайте дополнительные сведения
), перед люмбальной пункцией проводят КТ или МРТ. (Тем не менее риск вклинения не всегда можно предсказать с помощью КТ или МРТ).
-
Сердечно-легочная недостаточность или респираторный дистресс-синдром, которые могут усугубляться при лежачем положении во время люмбальной пункции
-
Анатомические аномалии в месте введения (например, спондилодез, ламинэктомия, врожденные аномалии)
Было показано, что бактериемия не предрасполагает к менингиту после люмбальной пункции и, таким образом, не является противопоказанием.
† Антикоагулянтная терапия (например, при тромбоэмболии легочной артерии) увеличивает риск кровотечения при катетеризации подключичной вены, однако этот риск должен быть сбалансирован с учетом повышенного риска тромбоза (например, инсульта) при отмене антикоагулянтной терапии. Если позволяет время, обсудите любые предполагаемые изменения с врачом, который контролирует антикоагулянтную терапию пациента.
-
Кровоизлияние в эпидуральное пространство (спинальная гематома)
-
Дискомфорт в нижней части спины или боль, которая может иррадиировать в задние отделы ног (самоограничивающая)
-
Эпидермоидная опухоль, возникает спустя годы после люмбальной пункции; риск увеличивается, если спинальная игла введена или извлечена без стилета (редко)
-
Вклинение головного мозга (редко)
-
Кортикальная слепота (редко)
-
Инфаркт спинного мозга в шейном отделе (редко)
-
Транзиторная или постоянная глухота (редко)
-
Ятрогенная инфекция (редко)
-
Транзиторная тошнота и/или звон в ушах
Головная боль развивается после люмбальной пункции примерно у 10% пациентов, обычно от нескольких часов до дня или двух после, и может быть тяжелой. Риск развития головной боли после ЛП повышен у лиц молодого возраста с небольшой массой тела. Использование более узких, нережущих игл может несколько уменьшить риск головной боли. Эти иглы вводят так, чтобы скос был обращен к правой или левой стороне пациента (его боков). Ни количество взятой СМЖ, ни длительность пребывания в лежачем положении после люмбальной пункции не влияют на частоту головной боли.
Во многих центрах имеются готовые наборы для люмбальной пункции. Если их нет, необходимое оборудование включает следующее:
-
Стерильные перчатки, халат, лицевая маска и головной убор
-
Стерильные хирургические простыни и/или полотенца
-
Раствор антисептика (например, хлоргексидин, повидон-йод, спиртовые салфетки)
-
Стерильную марлю (например, квадраты размером 10 см × 10 см [4 «× 4»])
-
Раствор для местной анестезии (например, 1% раствор лидокаина без адреналина, иглы 25-го и 20-го калибра, шприц 10 мл
-
Местные анестетики (стандартные для детей): безыгольное газовое инжекторное устройство с лидокаином, лидокаин-эпинефрин-тетракаиновый (ЛЭТ) гель или крем с лидокаином и прилокаином
-
Игла для спинномозговой пункции со стилетом: режущая игла (скошенный кончик) или нережущая (атравматическая) игла* (коническая); 20 или 22 * калибр; 9 см длиной для взрослых, 6 см для детей, 4 см для младенцев
-
Манометр и задвижка; опционально — короткая удлинительная трубка
-
Адгезивная повязка
* Использование специальных игл без режущих граней и игл меньшего калибра (т.е., 22-го калибра) снижает риск возникновения постпункционной головной боли.
Для ультразвукового контроля направления:
-
Прикроватное ультразвуковое устройство с высокочастотным линейным матричным зондом
-
При необходимости следует взять кровь на анализ глюкозы для сравнения с уровнем глюкозы в СМЖ; одновременно может быть взята кровь на олигоклональные полосы.
-
Краткосрочная седация (например, с применением пропофола или фентанила и/или мидазолама) может быть необходима для детей и взрослых с тревожностью.
-
Иглу желательно вводить в промежутках L3-L4 или L4-L5; таким образом, игла вводится ниже уровня спинного мозга.
-
Остистый отросток L4 лежит на воображаемой линии между верхушками задних верхних подвздошных гребней.
-
При введении по средней линии (наиболее распространенный подход) спинномозговая игла сначала пересекает надостистые и межостистые связки между остистыми отростками позвонков, прежде чем достигнет желтой связки.
Латеральное введение (например, на 1 см латеральнее и каудальнее от средней линии введения) не затрагивает связки в области средней линии и может облегчить люмбальную пункцию у пожилых пациентов, чьи связки кальцифицированы и склерозированы.
-
Желтая связка представляет собой толстую соединительнотканную структуру, при прохождении сквозь нее иглы может ощущаться «проваливание» (не всегда).
-
Затем игла проходит через эпидуральное пространство (жировую ткань и внутреннее позвоночное венозное сплетение) и через твердую мозговую оболочку (и одновременно через прилежащую арахноидальную оболочку), при этом снова может возникнуть ощущение «проваливания», после чего входит в субарахноидальное пространство (спинномозговой канал). Обратите внимание, что во многих случаях «проваливание» не ощущается.
У детей или младенцев, у которых соединительная ткань обладает низкой устойчивостью к проникновению, при прохождении иглой связки или твердой мозговой оболочки, «проваливание» не ощущается.
Позвоночник следует согнуть в поясничном отделе с целью расширения пространств между позвонками. Пациент может находиться в положении лежа на боку или сидеть. Положение лежа на боку, в целом, более предпочтительно, его следует использовать, если желательно проведение манометрии СМЖ. Положение сидя может быть более эффективным для пациентов с ожирением и предпочтительнее для младенцев.
-
Положение лежа на боку: пациент лежит на боку в позе эмбриона, с согнутыми настолько, насколько это допустимо, бедрами. Убедитесь, что таз, спина и плечи перпендикулярны кровати. Положите одну подушку под голову, чтобы голова была на одном уровне с позвоночником, а другую подушку, если это необходимо для удобства, между коленями. Ассистент может помочь пациенту максимально свернуться. Прежде чем начать, примите удобное положение рядом с пациентом.
-
Положение сидя: пациент сидит на краю кровати с ногами на стуле или кресле, согнутыми в тазобедренных суставах, и наклоняется вперед, положив голову и плечи на прикроватный столик.
При выполнении процедуры у младенца помощник держит его руки и ноги спереди, удерживая младенца в сидячей позе эмбриона на кровати. Для предотвращения асфиксии из-за сгибания шеи также необходима поддержка головы.
-
Поместите пациента в правильное положение, используя помощника, если это необходимо.
-
Определите место введения иглы клинически: пальпируйте остистые отростки позвонков поясничного отдела позвоночника для выявления наиболее близкого к воображаемой линии между задними верхними подвздошными остями подвздошной кости; наиболее близким остистым отростком обычно является L4 (иногда L3 у женщин). Местом введения является углубление немного каудальнее этого остистого отростка (т.е., промежуток L3-L4 для отростка L4). Пометьте место вмешательства с помощью маркера для кожи. Хотя обычным местом введения является промежуток между L3-L4, промежутки между L4-L5 или L2-L3 также являются приемлемыми.
-
При проведении пункции детям, нанесите местный анестетик на кожу и подождите, пока он подействует.
-
Обработайте место введения антисептическим раствором от центра к периферии несколькими концентрическими кругами около 20 см в диаметре.
-
Дайте раствору антисептика высохнуть в течение по крайней мере 1 минуты. Если используется йод или хлоргексидин, вытрите его спиртом, чтобы предотвратить его попадание в субарахноидальное пространство со спинальной иглой.
-
Поместите стерильное оборудование на стерильный поднос и накройте стерильной салфеткой.
-
Наденьте стерильные перчатки. Если у вас есть какие-либо респираторные симптомы, носите маску. Если действуют протоколы изоляции, наденьте халат, маску и шапочку.
-
Соедините вместе манометр, кран и короткую соединительную трубку. Короткая соединительная трубка обеспечивает некоторую подвижность, помогая предотвратить неожиданное движение подключенного аппарата от смещения иглы, например, при неожиданном движении пациента.
-
Убедитесь, что кран, спинальная игла и стилет двигаются плавно.
-
Поместите стерильные простыни вокруг места операции.
-
С помощью иглы 25-го калибра введите анестетик в месте введения иглы, до образования папулы, а затем глубоко анестезируйте мягкие ткани вдоль предполагаемого пути введения иглы.
-
Стилет должен полностью находиться на спинальной игле, когда она вводится или извлекается.
-
Удерживайте скошенную спинальную иглу таким образом, чтобы скос был обращен к правой или левой стороне пациента (т.е., направлен к пациенту, который находится в положении лежа на боку). Хотя иглу можно держать и одной рукой, фиксация двумя руками обеспечивает лучший контроль в случае, если пациент двигается или дергается.
-
Пропальпируйте гребень подвздошной кости и остистые отростки позвонков, чтобы убедиться в правильности места введения.
-
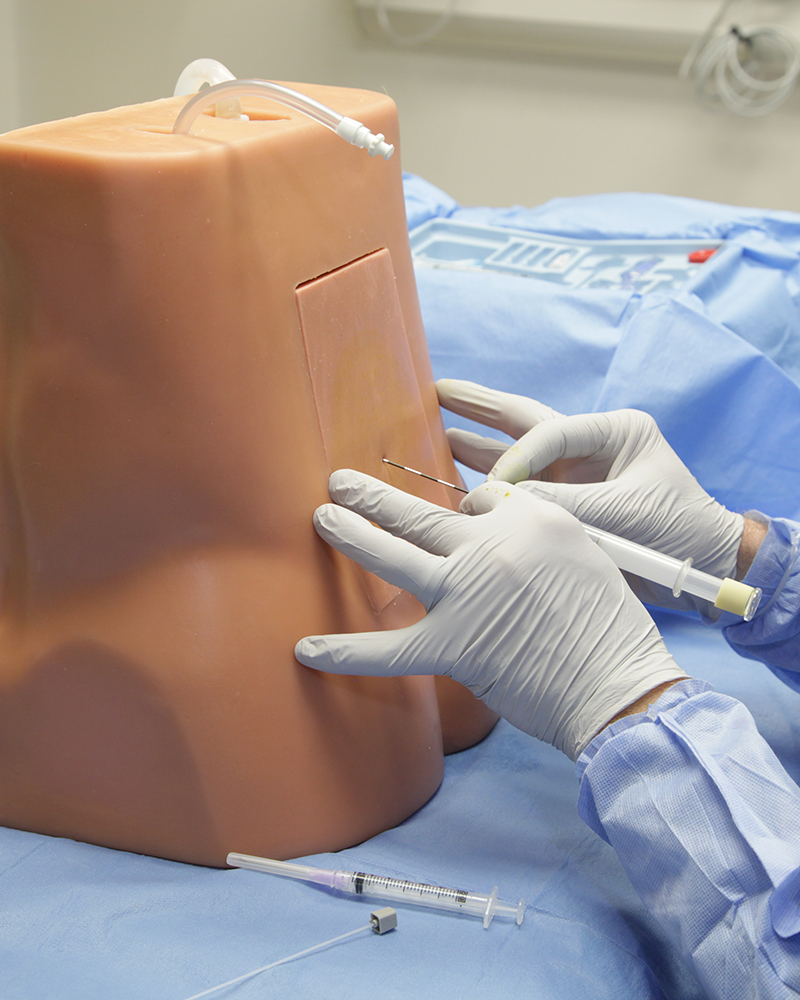
Вводите иглу, направленную в сторону пупка, примерно на 15° краниально, и продвигайте ее небольшими толчками примерно по 2–3 мм. При прокалывании иглой желтой связки (при попадании в эпидуральное пространство) и иногда при прокалывании твердой мозговой оболочки (при попадании в субарахноидальное пространство) может быть чувство «проваливания». При введении иглы детям такое ощущение обычно менее выраженно. Часто, для того чтобы попасть в субарахноидальное пространство, иглу необходимо продвинуть на большую часть ее длины. Удалите стилет во время дальнейшего продвижения иглы, чтобы проверить наличие тока СМЖ (указывающего на доступ к субарахноидальному пространству); повторно вставьте стилет перед продолжением продвижения иглы.
Если игла соприкасается с костью, выведите ее на подкожный уровень, направьте ее немного краниальнее, затем введите снова. Убедитесь, что игла направлена к спинномозговому каналу, а не в сторону.
Если при глубоком введении появляется кровь, то игла могла попасть в венозное сплетение в вентральной части спинного мозга. Извлекают иглу последовательными маленькими (например, 1 мм) движениями, проверяя возврат ЦСЖ при каждом движении.
-
Иногда кончик иглы блокируется нервными корешками или другими тканевыми структурами. Если СМЖ не получена, несмотря на успешное проникновение в субарахноидальное пространство, поверните иглу на 90° и выполните процедуру повторно.
-
Сразу после достижения субарахноидального пространства, повторно вставьте стилет и не продвигайте иглу дальше.
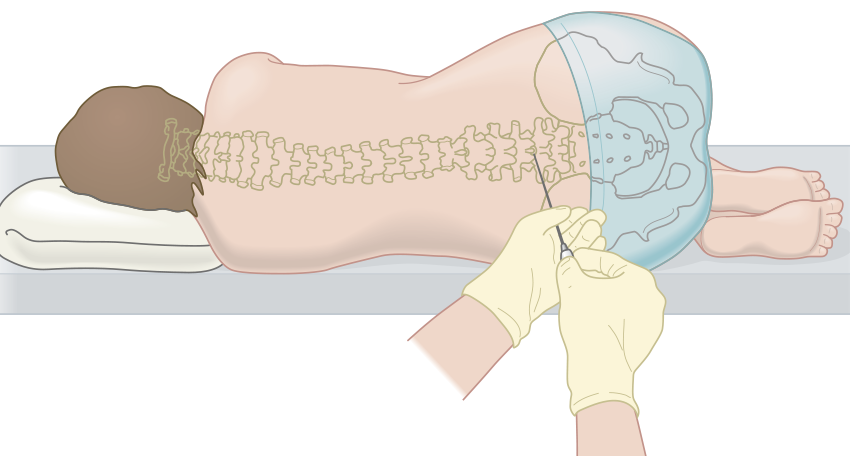
Люмбальная пункция
Люмбальная пункция выполняется пациенту в положении лежа на боку, игла для люмбальной пункции вводиться в промежуток между L3-L4.
Обычно проводят манометрию, но от нее можно отказаться, если пациенты находятся в критическом состоянии, и следует отказаться у пациентов, которые находятся в сидячем положении, потому что такие измерения будут неточными.
-
Снимите мадрен с иглы для спинальной пункции.
-
Прикрепите собранный манометр/кран/удлинительную трубку к игле.
-
Держите манометр на уровне спинальной иглы.
-
Откройте задвижку.
-
СМЖ поднимется в трубке манометра на высоту, соответствующую давлению СМЖ, которое можно определить по нанесенным на трубку делениям. Мениск СМЖ может незначительно колебаться в такт дыханию. Нормальная высота столба жидкости (давление СМЖ) составляет 7–18 см.
Если давление низкое, попросите пациента постепенно выпрямить ноги, чтобы улучшить течение СМЖ. Если нет изменений давления при дыхании, особенно если давление низкое, поверните иглу на 90°, чтобы уменьшить возможную обструкцию нервом, или если игла не полностью находится в субарахноидальном пространстве.
-
Никогда не аспирируйте СМЖ.
-
Если была выполнена манометрия СМЖ, следует отобрать СМЖ из манометра в первую пробирку для сбора. Когда манометр опустеет, снимите его.
-
Позвольте приблизительно 1–2 мл СМЖ стечь в каждую из 4 пробирок по порядку. Для некоторых тестов, таких как обнаружение кислотоустойчивых бацилл, грибов (например, Cryptococcus neoformans, Coccidioides immitis) или карциноматозного менингита, могут быть необходимы большие объемы (до 30–40 мл).
-
Необходимо провести подсчет клеток и разницу в их количестве в 1-й и 3-й пробирках, чтобы можно было сравнивать количество клеток, если присутствуют эритроциты. (Резкое снижение количества эритроцитов от 1-й до 3-й пробирки свидетельствует о травматической пункции).
-
Из 2-й пробирки и, при необходимости, из СМЖ, оставшейся от 1-й и/или 3-й пробирки, необходимо провести другие исследования, в том числе определение уровней белка и глюкозы, определение олигоклональных IgG («олигоклональные полосы» [при необходимости]) и микробиологическое тестирование.
-
В случае, если позже станут необходимыми непредвиденные дополнительные исследования, рассмотрите возможность замораживания 4-й пробирки. Проконсультируйтесь с лабораторией на предмет того, как долго там хранятся образцы, и попросите их сохранить образец в течение более длительного периода времени, если это необходимо.
-
Снова вставьте стилет в иглу.
-
Осторожно извлеките иглу.
-
Наложите адгезивную повязку.
-
После проведения люмбальной пункции постельный режим не является необходимым и не снижает частоту возникновения постпункционной головной боли, однако лежачее положение помогает при лечении такого типа болей.
-
Предполагалось, что увеличение перорального потребления жидкостей лечит постпроцедурную головную боль, но оно не показало эффективности в контролируемых исследованиях. Предотвратить постоперационную головную боль помогает кофеин.
-
Попросите пациента быть начеку в отношении постоянных или усиливающихся болей в спине (могут возникнуть в течение нескольких дней после люмбальной пункции), которые требуют немедленного обследования для исключения диагноза, или гематомы.
-
Убедитесь, что бедра, спина и плечи пациента находятся точно перпендикулярно кровати.
-
При использовании положения лежа на боку, пациенту следует постоянно поддерживать позицию плотно скрученного эмбриона.
-
Не забывайте направлять иглу по средней линии (не уводить ее в сторону) и немного краниальнее.
Ошибки в этом процессе затруднят вход в позвоночный канал.
-
Не вынимайте иглу без повторной установки стилета.
-
Если игла не попала в спинномозговой канал, не пытайтесь изменить ее положение, перемещая кончик в ту или иную сторону; это может привести к повреждению тканей. Вместо этого, перед изменением угла и направления введения, иглу следует оттянуть почти к поверхности кожи (т.е., снаружи межпозвоночной связки).
-
Прежде чем начать выполнение процедуры в положении пациента лежа на боку, сядьте удобно рядом с ним.
-
Для лучшего контроля постарайтесь держать иглу обеими руками.
-
Избегайте введения спинальной иглы через кожу, покрытую татуировками, из-за теоретической возможности того, что чернила для татуировки могут попасть в СМЖ и вызвать раздражение или токсичность. Если необходимо, либо используйте смежный промежуток, либо сделайте по татуированному эпидермису небольшой разрез скальпелем, а затем введите иглу через разрез.
-
После того как игла пройдет через кожу и в остистую связку, еще раз проверьте положение пациента (бедра перпендикулярно кровати) и направление иглы (перпендикулярно позвоночнику) перед дальнейшим введением.
-
Возьмите кровь для определения уровня глюкозы до люмбальной пункции (примерно за 30 минут, например), чтобы можно было точно сравнить ее уровень с уровнем глюкозы в СМЖ. За это время можно также сравнить олигоклональные группы в сыворотке и СМЖ.
-
Если люмбальная пункция не удалась в положении лежа, попробуйте сидячее положение, применение которого может быть более успешным из-за увеличения сгибания позвоночника и открытия межпозвоночного пространства.
Пункция спинного мозга. Такое страшное словосочетание нередко можно услышать на приеме у врача, а еще страшнее становится, когда эта процедура касается именно вас. Зачем врачи пунктируют спинной мозг? Опасна ли такая манипуляция? Какую информацию можно получить в ходе данного исследования?
Первое, что нужно уяснить, когда речь идет о пункции спинного мозга (а именно так данную процедуру чаще всего называют пациенты), то подразумевается не прокол самой ткани органа центральной нервной системы, а только забор небольшого количества спинномозговой жидкости, которая омывает спинной и головной мозг. Такая манипуляция в медицине называется спинномозговой, или люмбальной, пункцией.
Для чего делают пункцию спинного мозга? Целей такой манипуляции может быть три – диагностическая, обезболивающая и лечебная. В большинстве случаев поясничный прокол позвоночника делается для выяснения состава ликвора и давления внутри позвоночного канала, что косвенно отображает патологические процессы, происходящие в головном и спинном мозге. Но пункцию спинного мозга специалисты могут выполнить с терапевтической целью, например, для введения лекарственных препаратов в субарахноидальное пространство, для быстрого снижения спинномозгового давления. Также не нужно забывать о таком методе обезболивания, как спинальная анестезия, когда анестетики вводят в спинномозговой канал. Это дает возможность проведения большого количества оперативных вмешательств без применения общего наркоза.
Учитывая, что в большинстве случаев пункция спинного мозга назначается именно с диагностической целью, именно о данном виде исследования и пойдет речь в этой статье.
Для чего берут пункцию
Люмбальную пункцию берут для исследования спинномозговой жидкости, что позволяет диагностировать некоторые заболевания головного и спинного мозга. Чаще всего такую манипуляцию назначают при подозрении на:
- инфекции центральной нервной системы (менингит, энцефалит, миелит, арахноидит) вирусной, бактериальной или грибковой природы;
- сифилитическое, туберкулезное поражение головного и спинного мозга;
- субарахноидальное кровотечение;
- абсцесс органов ЦНС;
- ишемический, геморрагический инсульт;
- черепно-мозговую травму;
- демиелинизирующие поражения нервной системы, например, рассеянный склероз;
- доброкачественные и злокачественные опухоли головного и спинного мозга, их оболочек;
- синдром Гиенна-Барре;
- др. неврологические заболевания.
Исследование спинномозговой жидкости дает возможность быстро диагностировать тяжелые заболевания головного и спинного мозга
Противопоказания
Запрещено взятие люмбальной пункции при объемных образованиях задней черепной ямки или височной доли головного мозга. В таких ситуациях забор даже небольшого количества ликвора может вызвать дислокацию мозговых структур и стать причиной ущемления ствола мозга в большом затылочном отверстии, что влечет за собой немедленный летальный исход.
Также запрещено проводить поясничный прокол при наличии у пациента гнойно-воспалительных поражений кожи, мягких тканей, позвоночника в месте прокола.
Относительными противопоказаниями являются выраженные деформации позвоночника (сколиоз, кифосколиоз и пр.), так как при этом возрастает риск осложнений.
С осторожностью пункцию назначают пациентам с нарушением свертываемости крови, тем, кто принимает препараты, которые влияют на реологию крови (антикоагулянты, антиагреганты, нестероидные противовоспалительные средства).
При опухолях головного мозга проводить люмбальную пункцию можно только по жизненным показаниям, так как высок риск развития дислокации мозговых структур
Этап подготовки
Процедура люмбальной пункции требует предварительной подготовки. В первую очередь, пациенту назначаются общеклинические и биохимические анализы крови и мочи, обязательно определяется состояние свертывающей системы крови. Проводят осмотр и пальпацию поясничного отдела позвоночника. Чтобы выявить возможные деформации, которые могут препятствовать проведению прокола.
Нужно рассказать врачу о всех лекарствах, которые принимаете сейчас или недавно применяли. Особое внимание следует уделить препаратам, которые влияют на свертываемость крови (аспирин, варфарин, клопидогрель, гепарин и прочие антиагреганты и антикоагулянты, нестероидные противовоспалительные средства).
Также нужно сообщить доктору о возможной аллергии на медикаменты, в том числе на анестетики и контрастные вещества, о перенесенных недавно острых заболеваниях, о наличии хронических недугов, так как некоторые из них могут быть противопоказанием к проведению исследования. Все женщины детородного возраста должны сообщить врачу о возможной беременности.
В обязательном порядке перед выполнением пункции спинного мозга пациент должен получить консультацию доктора
Запрещено есть на протяжении 12 часов до процедуры и пить на протяжении 4 часов до пункции.
Методика проведения пункции
Процедуру проводят в положении пациента лежа на боку. При этом нужно максимально согнуть ноги в коленных и тазобедренных суставах, привести их к животу. Голова должна быть максимально согнутой вперед и приближенной к грудной клетке. Именно в таком положении межпозвоночные промежутки хорошо расширяются и специалисту проще будет попасть иглой в нужное место. В некоторых случаях пункцию проводят в положении пациента сидя с максимально округленной спиной.
Место для прокола выбирает специалист с помощью пальпации позвоночника так, чтобы не повредить нервную ткань. Спинной мозг у взрослого человека заканчивается на уровне 2 поясничного позвонка, но у людей низкого роста, а также у детей (в том числе и новорожденных) он немного длиннее. Поэтому иглу вводят в межпозвоночном промежутке между 3 и 4 поясничными позвонками либо между 4 и 5. Это снижает риск осложнений после пункции.
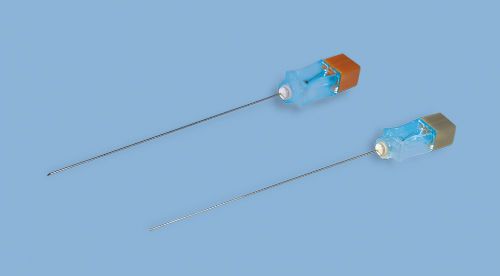
После обработки кожи антисептическими растворами проводят местную инфильтрационную анестезию мягких тканей раствором новокаина или лидокаина обычным шприцом с иглой. После этого проводят непосредственно люмбальную пункцию специальной большой иглой с мандреном.
Так выглядит игла для спинномозговой пункции
Прокол делают в выбранной точке, иглу врач направляет сагиттально и немного вверх. Примерно на глубине 5 см ощущается сопротивление, после чего следует своеобразный провал иглы. Это означает что конец иглы попал в субарахноидальное пространство и можно приступать к забору ликвора. Для этого доктор вынимает из иглы мандрен (внутренняя часть, которая делает инструмент герметичным) и из нее начинает капать ликвор. Если этого не происходит, нужно убедится в правильности проведения пункции и попадании иглы в субарахноидальное пространство.
После набора ликвора в стерильную пробирку иглу осторожно извлекают, а место прокола заклеивают стерильной повязкой. В течении 3-4 часов после прокола пациент должен лежать на спине или на боку.
Прокол выполняют между 3 и 4 или 4 и 5 поясничными позвонками
Исследование спинномозговой жидкости
Первым этапом анализа спинномозговой жидкости является оценка ее давления. Нормальные показатели в положении сидя – 300 мм. вод. ст., в положении лежа – 100-200 мм. вод. ст. Как правило, оценивают давление косвенно – по количеству капель за минуту. 60 капель в минуту соответствует нормальной величине давления ликвора в спинномозговом канале. Повышается давление при воспалительных процессах ЦНС, при опухолевых образованиях, при венозном застое, гидроцефалии и др. заболеваниях.
Дальше ликвор набирают в две пробирки по 5 мл. Их потом используют для проведения необходимого перечня исследований – физико-химического, бактериоскопического, бактериологического, иммунологического, ПЦР-диагностики и пр.
В зависимости от полученных результатов исследования спинномозговой жидкости, врач может распознать заболевание и назначить соответствующее лечение
Последствия и возможные осложнения
В подавляющем большинстве случаев процедура проходит без каких-либо последствий. Естественно, само проведение пункции – это больно, но боль присутствует только на этапе введения иглы.
У некоторых пациентов могут развиваться следующие осложнения.
Постпункционная головная боль
Принято считать, что из отверстия после проведения пункции вытекает определенное количество ликвора, вследствие этого снижается внутричерепное давление и возникает головная боль. Такая боль напоминает головную боль напряжения, имеет постоянный ноющий или сдавливающий характер, снижается после отдыха и сна. Может наблюдаться на протяжении 1 недели после пункции, если цефалгия сохраняется спустя 7 дней – это повод обратиться к врачу.
Травматические осложнения
Иногда могут встречаться травматические осложнения пункции, когда иглой можно повредить спинномозговые нервные корешки, межпозвоночные диски. Это проявляется болью в спине, которая после правильно выполненной пункции не возникает.
Геморрагические осложнения
Если во время прокола повреждены крупные кровеносные сосуды, может возникать кровотечение, формирование гематомы. Это опасное осложнение, которое требует активного медицинского вмешательства.
Дислокационные осложнения
Возникают при резком падении ликворного давления. Такое возможно при наличии объемных образований задней черепной ямки. Чтобы избежать такого риска, перед тем, как взять пункцию, необходимо выполнить исследование на признаки дислокации срединных структур головного мозга (ЭЭГ, РЕГ).
Инфекционные осложнения
Могут возникать из-за нарушения правил асептики и антисептики во время проведения пункции. У пациента может развиваться воспаление мозговых оболочек и даже формироваться абсцессы. Такие последствия пункции опасны для жизни и требуют назначения мощной антибактериальной терапии.
Таким образом, пункция спинного мозга – это очень информативная методика диагностики большого количества заболеваний головного и спинного мозга. Естественно, осложнения во время проведения манипуляции и после нее возможны, но они очень редко встречаются, а польза пункции намного превышает риск развития негативных последствий.
From Wikipedia, the free encyclopedia
| Lumbar puncture | |
|---|---|

Lumbar puncture in a sitting position. The reddish-brown swirls on the patient’s back are tincture of iodine (an antiseptic). |
|
| Other names | Spinal tap |
| ICD-9-CM | 03.31 |
| MeSH | D013129 |
| eMedicine | 80773 |
|
[edit on Wikidata] |
Lumbar puncture (LP), also known as a spinal tap, is a medical procedure in which a needle is inserted into the spinal canal, most commonly to collect cerebrospinal fluid (CSF) for diagnostic testing. The main reason for a lumbar puncture is to help diagnose diseases of the central nervous system, including the brain and spine. Examples of these conditions include meningitis and subarachnoid hemorrhage. It may also be used therapeutically in some conditions. Increased intracranial pressure (pressure in the skull) is a contraindication, due to risk of brain matter being compressed and pushed toward the spine. Sometimes, lumbar puncture cannot be performed safely (for example due to a severe bleeding tendency). It is regarded as a safe procedure, but post-dural-puncture headache is a common side effect if a small atraumatic needle is not used.[1]
The procedure is typically performed under local anesthesia using a sterile technique. A hypodermic needle is used to access the subarachnoid space and collect fluid. Fluid may be sent for biochemical, microbiological, and cytological analysis. Using ultrasound to landmark may increase success.[2]
Lumbar puncture was first introduced in 1891 by the German physician Heinrich Quincke.
Medical uses[edit]
The reason for a lumbar puncture may be to make a diagnosis[3][4][5] or to treat a disease.[4]
Diagnosis[edit]
The chief diagnostic indications of lumbar puncture are for collection of cerebrospinal fluid (CSF). Analysis of CSF may exclude infectious,[4][6] inflammatory,[4] and neoplastic diseases[4] affecting the central nervous system. The most common purpose is in suspected meningitis,[7] since there is no other reliable tool with which meningitis, a life-threatening but highly treatable condition, can be excluded. A lumbar puncture can also be used to detect whether someone has ‘Stage 1’ or ‘Stage 2’ Trypanosoma brucei. Young infants commonly require lumbar puncture as a part of the routine workup for fever without a source. This is due to higher rates of meningitis than in older persons. Infants also do not reliably show classic symptoms of meningeal irritation (meningismus) like neck stiffness and headache the way adults do.[7] In any age group, subarachnoid hemorrhage, hydrocephalus, benign intracranial hypertension, and many other diagnoses may be supported or excluded with this test. It may also be used to detect the presence of malignant cells in the CSF, as in carcinomatous meningitis or medulloblastoma. CSF containing less than 10 red blood cells (RBCs)/mm3 constitutes a «negative» tap in the context of a workup for subarachnoid hemorrhage, for example. Taps that are «positive» have an RBC count of 100/mm³ or more.[8]
Treatment[edit]
Lumbar punctures may also be done to inject medications into the cerebrospinal fluid («intrathecally»), particularly for spinal anesthesia[9] or chemotherapy.
Serial lumbar punctures may be useful in temporary treatment of idiopathic intracranial hypertension (IIH). This disease is characterized by increased pressure of CSF which may cause headache and permanent loss of vision. While mainstays of treatment are medication, in some cases lumbar puncture performed multiple times may improve symptoms. It is not recommended as a staple of treatment due to discomfort and risk of the procedure, and the short duration of its efficacy.[10][11]
Additionally, some people with normal pressure hydrocephalus (characterized by urinary incontinence, a changed ability to walk properly, and dementia) receive some relief of symptoms after removal of CSF.[12]
Contraindications[edit]
Lumbar puncture should not be performed in the following situations:
- Idiopathic (unidentified cause) increased intracranial pressure (ICP)
- Rationale: lumbar puncture in the presence of raised ICP may cause uncal herniation
- Exception: therapeutic use of lumbar puncture to reduce ICP, but only if obstruction (for example in the third ventricle of the brain) has been ruled out
- Precaution
- CT brain, especially in the following situations
- Age >65
- Reduced GCS
- Recent history of seizure
- Focal neurological signs
- Abnormal respiratory pattern
- Hypertension with bradycardia and deteriorating consciousness
- Ophthalmoscopy for papilledema
- CT brain, especially in the following situations
- Bleeding diathesis (relative)
- Coagulopathy
- Decreased platelet count (<50 x 109/L)
- Infections
- Skin infection at puncture site
- Vertebral deformities (scoliosis or kyphosis), in hands of an inexperienced physician.[13][14]
Adverse effects[edit]
Headache[edit]
Post spinal headache with nausea is the most common complication; it often responds to pain medications and infusion of fluids. It was long taught that this complication can be prevented by strict maintenance of a supine posture for two hours after the successful puncture; this has not been borne out in modern studies involving large numbers of people. Doing the procedure with the person on their side might decrease the risk.[15] Intravenous caffeine injection is often quite effective in aborting these spinal headaches. A headache that is persistent despite a long period of bedrest and occurs only when sitting up may be indicative of a CSF leak from the lumbar puncture site. It can be treated by more bedrest, or by an epidural blood patch, where the person’s own blood is injected back into the site of leakage to cause a clot to form and seal off the leak.[16]
The risk of headache and need for analgesia and blood patch is much reduced if «atraumatic» needles are used. This does not affect the success rate of the procedure in other ways.[17][18] Although the cost and difficulty are similar, adoption remains low – only 16% ca. 2014.[19]
The headaches may be caused by inadvertent puncture of the dura mater.[20]
Other[edit]
Contact between the side of the lumbar puncture needle and a spinal nerve root can result in anomalous sensations (paresthesia) in a leg during the procedure; this is harmless and people can be warned about it in advance to minimize their anxiety if it should occur.
Serious complications of a properly performed lumbar puncture are extremely rare.[4] They include spinal or epidural bleeding, adhesive arachnoiditis and trauma to the spinal cord[9] or spinal nerve roots resulting in weakness or loss of sensation, or even paraplegia. The latter is exceedingly rare, since the level at which the spinal cord ends (normally the inferior border of L1, although it is slightly lower in infants) is several vertebral spaces above the proper location for a lumbar puncture (L3/L4). There are case reports of lumbar puncture resulting in perforation of abnormal dural arterio-venous malformations, resulting in catastrophic epidural hemorrhage; this is exceedingly rare.[9]
The procedure is not recommended when epidural infection is present or suspected, when topical infections or dermatological conditions pose a risk of infection at the puncture site or in patients with severe psychosis or neurosis with back pain. Some authorities believe that withdrawal of fluid when initial pressures are abnormal could result in spinal cord compression or cerebral herniation; others believe that such events are merely coincidental in time, occurring independently as a result of the same pathology that the lumbar puncture was performed to diagnose. In any case, computed tomography of the brain is often performed prior to lumbar puncture if an intracranial mass is suspected.[21]
CSF leaks can result from a lumbar puncture procedure.[22][23][24][25]
Technique[edit]
Mechanism[edit]
The brain and spinal cord are enveloped by a layer of cerebrospinal fluid, 125–150 mL in total (in adults) which acts as a shock absorber and provides a medium for the transfer of nutrients and waste products. The majority is produced by the choroid plexus in the brain and circulates from there to other areas, before being reabsorbed into the circulation (predominantly by the arachnoid granulations).[26]
The cerebrospinal fluid can be accessed most safely in the lumbar cistern. Below the first or second lumbar vertebrae (L1 or L2) the spinal cord terminates (conus medullaris). Nerves continue down the spine below this, but in a loose bundle of nerve fibers called the cauda equina. There is lower risk with inserting a needle into the spine at the level of the cauda equina because these loose fibers move out of the way of the needle without being damaged.[26] The lumbar cistern extends into the sacrum up to the S2 vertebra.[26]
Procedure[edit]
The person is usually placed on their side (left more commonly than right). The patient bends the neck so the chin is close to the chest, hunches the back, and brings knees toward the chest. This approximates a fetal position as much as possible. Patients may also sit on a stool and bend their head and shoulders forward. The area around the lower back is prepared using aseptic technique. Once the appropriate location is palpated, local anaesthetic is infiltrated under the skin and then injected along the intended path of the spinal needle. A spinal needle is inserted between the lumbar vertebrae L3/L4, L4/L5[9] or L5/S1[9] and pushed in until there is a «give» as it enters the lumbar cistern wherein the ligamentum flavum is housed. The needle is again pushed until there is a second ‘give’ that indicates the needle is now past the dura mater. The arachnoid membrane and the dura mater exist in flush contact with one another in the living person’s spine due to fluid pressure from CSF in the subarachnoid space pushing the arachnoid membrane out towards the dura. Therefore, once the needle has pierced the dura mater it has also traversed the thinner arachnoid membrane. The needle is then in the subarachnoid space. The stylet from the spinal needle is then withdrawn and drops of cerebrospinal fluid are collected. The opening pressure of the cerebrospinal fluid may be taken during this collection by using a simple column manometer. The procedure is ended by withdrawing the needle while placing pressure on the puncture site. The spinal level is so selected to avoid spinal injuries.[9] In the past, the patient would lie on their back for at least six hours and be monitored for signs of neurological problems. There is no scientific evidence that this provides any benefit. The technique described is almost identical to that used in spinal anesthesia, except that spinal anesthesia is more often done with the patient in a seated position.[citation needed]
The upright seated position is advantageous in that there is less distortion of spinal anatomy which allows for easier withdrawal of fluid. Some practitioners prefer it for lumbar puncture in obese patients, where lying on their side would cause a scoliosis and unreliable anatomical landmarks. However, opening pressures are notoriously unreliable when measured in the seated position. Therefore, patients will ideally lie on their side if practitioners need to measure opening pressure.[citation needed]
Reinsertion of the stylet may decrease the rate of post lumbar puncture headaches.[14]
Although not available in all clinical settings, use of ultrasound is helpful for visualizing the interspinous space and assessing the depth of the spine from the skin. Use of ultrasound reduces the number of needle insertions and redirections, and results in higher rates of successful lumbar puncture.[27] If the procedure is difficult, such as in people with spinal deformities such as scoliosis, it can also be performed under fluoroscopy (under continuous X-ray imaging).[28]
Children[edit]
In children, a sitting flexed position was as successful as lying on the side with respect to obtaining non-traumatic CSF, CSF for culture, and cell count. There was a higher success rate in obtaining CSF in the first attempt in infants younger than 12 months in the sitting flexed position.[29]
The spine of an infant at the time of birth differs from the adult spine. The conus medullaris (bottom of the spinal cord) terminates at the level of L1 in adults, but may range in term neonates (newly born babies) from L1–L3 levels.[30] It is important to insert the spinal needle below the conus medullaris at the L3/L4 or L4/L5 interspinous levels.[31] With growth of the spine, the conus typically reaches the adult level (L1) by 2 years of age.[30]
The ligamentum flavum and dura mater are not as thick in infants and children as they are in adults. Therefore, it is difficult to assess when the needle passes through them into the subarachnoid space because the characteristic «pop» or «give» may be subtle or nonexistent in the pediatric lumbar puncture. To decrease the chances of inserting the spinal needle too far, some clinicians use the «Cincinnati» method. This method involves removing the stylet of the spinal needle once the needle has advanced through the dermis. After removal of the stylet, the needle is inserted until CSF starts to come out of the needle. Once all of the CSF is collected, the stylet is then reinserted before removal of the needle.[31]
Interpretation[edit]
Analysis of the cerebrospinal fluid generally includes a cell count and determination of the glucose and protein concentrations. The other analytical studies of cerebrospinal fluid are conducted according to the diagnostic suspicion.[4]
Pressure determination[edit]
Increased CSF pressure can indicate congestive heart failure, cerebral edema, subarachnoid hemorrhage, hypo-osmolality resulting from hemodialysis, meningeal inflammation, purulent meningitis or tuberculous meningitis, hydrocephalus, or pseudotumor cerebri.[26] In the setting of raised pressure (or normal pressure hydrocephalus, where the pressure is normal but there is excessive CSF), lumbar puncture may be therapeutic.[26]
Decreased CSF pressure can indicate complete subarachnoid blockage, leakage of spinal fluid, severe dehydration, hyperosmolality, or circulatory collapse. Significant changes in pressure during the procedure can indicate tumors or spinal blockage resulting in a large pool of CSF, or hydrocephalus associated with large volumes of CSF.[26]
Cell count[edit]
The presence of white blood cells in cerebrospinal fluid is called pleocytosis. A small number of monocytes can be normal; the presence of granulocytes is always an abnormal finding. A large number of granulocytes often heralds bacterial meningitis. White cells can also indicate reaction to repeated lumbar punctures, reactions to prior injections of medicines or dyes, central nervous system hemorrhage, leukemia, recent epileptic seizure, or a metastatic tumor. When peripheral blood contaminates the withdrawn CSF, a common procedural complication, white blood cells will be present along with erythrocytes, and their ratio will be the same as that in the peripheral blood.[citation needed]
The finding of erythrophagocytosis,[32] where phagocytosed erythrocytes are observed, signifies haemorrhage into the CSF that preceded the lumbar puncture. Therefore, when erythrocytes are detected in the CSF sample, erythrophagocytosis suggests causes other than a traumatic tap, such as intracranial haemorrhage and haemorrhagic herpetic encephalitis. In which case, further investigations are warranted, including imaging and viral culture.[citation needed]
Microbiology[edit]
CSF can be sent to the microbiology lab for various types of smears and cultures to diagnose infections.
- Gram staining may demonstrate gram positive bacteria in bacterial meningitis.[33]
- Microbiological culture is the gold standard for detecting bacterial meningitis. Bacteria, fungi, and viruses can all be cultured by using different techniques.
- Polymerase chain reaction (PCR) has been a great advance in the diagnosis of some types of meningitis, such as meningitis from herpesvirus and enterovirus. It has high sensitivity and specificity for many infections of the CNS, is fast, and can be done with small volumes of CSF. Even though testing is expensive, cost analyses of PCR testing in neonatal patients demonstrated savings via reduced cost of hospitalization.[34][35]
- Numerous antibody-mediated tests for CSF are available in some countries: these include rapid tests for antigens of common bacterial pathogens, treponemal titers for the diagnosis of neurosyphilis and Lyme disease, CoccidioidesCoccidioides antibody, and others.[citation needed]
- The India ink test is still used for detection of meningitis caused by Cryptococcus neoformans,[36][37] but the cryptococcal antigen (CrAg) test has a higher sensitivity.[38]
Chemistry[edit]
Several substances found in cerebrospinal fluid are available for diagnostic measurement.
- Glucose is present in the CSF; the level is usually about 60% that in the peripheral circulation.[39] A fingerstick or venipuncture at the time of lumbar puncture may therefore be performed to assess peripheral glucose levels and determine a predicted CSF glucose value. Decreased glucose levels[40] can indicate fungal, tuberculous[41] or pyogenic infections; lymphomas; leukemia spreading to the meninges; meningoencephalitic mumps; or hypoglycemia. A glucose level of less than one third of blood glucose levels in association with low CSF lactate levels is typical in hereditary CSF glucose transporter deficiency also known as De Vivo disease.[42]
- Increased glucose levels in the fluid can indicate diabetes, although the 60% rule still applies.[43][44]
- Increased levels of glutamine[45] are often involved with hepatic encephalopathies,[46][47] Reye’s syndrome,[48][49] hepatic coma, cirrhosis,[47] hypercapnia and depression.[50]
- Increased levels of lactate can occur the presence of cancer of the CNS, multiple sclerosis, heritable mitochondrial disease, low blood pressure, low serum phosphorus, respiratory alkalosis, idiopathic seizures, traumatic brain injury, cerebral ischemia, brain abscess, hydrocephalus, hypocapnia or bacterial meningitis.[43]
- The enzyme lactate dehydrogenase can be measured to help distinguish meningitides of bacterial origin, which are often associated with high levels of the enzyme, from those of viral origin in which the enzyme is low or absent.[51]
- Changes in total protein content of cerebrospinal fluid can result from pathologically increased permeability of the blood-cerebrospinal fluid barrier,[52] obstructions of CSF circulation, meningitis, neurosyphilis, brain abscesses, subarachnoid hemorrhage, polio, collagen disease or Guillain–Barré syndrome, leakage of CSF, increases in intracranial pressure, or hyperthyroidism. Very high levels of protein may indicate tuberculous meningitis or spinal block.
- IgG synthetic rate is calculated from measured IgG and total protein levels; it is elevated in immune disorders such as multiple sclerosis, transverse myelitis, and neuromyelitis optica of Devic. Oligoclonal bands may be detected in CSF but not in serum, suggesting intrathecal antibody production.
| Infection | Appearance[53] | WBCs / mm3[54] | Protein (g/L)[54] | Glucose[54] |
|---|---|---|---|---|
| Normal | Clear | <5 | 0.15 to 0.45 | > 2/3 of blood glucose |
| Bacterial | Yellowish, turbid | > 1,000 (mostly PMNs) | > 1 | Low |
| Viral | Clear | < 200 (mostly lymphocytes) | Mild increase | Normal or mildly low |
| Tuberculosis | Yellowish and viscous | Modest increase | Markedly Increased | Decreased |
| Fungal | Yellowish and viscous | < 50 (mostly lymphocytes) | Initially normal, then increased | Normal or mildly low |
History[edit]
The first technique for accessing the dural space was described by the London physician Walter Essex Wynter. In 1889 he developed a crude cut down with cannulation in four patients with tuberculous meningitis. The main purpose was the treatment of raised intracranial pressure rather than for diagnosis.[55] The technique for needle lumbar puncture was then introduced by the German physician Heinrich Quincke, who credits Wynter with the earlier discovery; he first reported his experiences at an internal medicine conference in Wiesbaden, Germany, in 1891.[56] He subsequently published a book on the subject.[57][58]
The lumbar puncture procedure was taken to the United States by Arthur H. Wentworth an assistant professor at the Harvard Medical School, based at Children’s Hospital. In 1893 he published a long paper on diagnosing cerebrospinal meningitis by examining spinal fluid.[59] However, he was criticized by antivivisectionists for having obtained spinal fluid from children. He was acquitted, but, nevertheless, he was uninvited from the then forming Johns Hopkins School of Medicine, where he would have been the first professor of pediatrics.[citation needed]
Historically lumbar punctures were also employed in the process of performing a pneumoencephalography, a nowadays obsolete X-ray imaging study of the brain that was performed extensively from the 1920s until the advent of modern non-invasive neuroimaging techniques such as MRI and CT in the 1970s. During this quite painful procedure, CSF was replaced with air or some other gas via the lumbar puncture in order to enhance the appearance of certain areas of the brain on plain radiographs.
References[edit]
- ^ Maranhao, B.; Liu, M.; Palanisamy, A.; Monks, D. T.; Singh, P. M. (17 December 2020). «The association between post‐dural puncture headache and needle type during spinal anaesthesia: a systematic review and network meta‐analysis». Anaesthesia. Wiley. 76 (8): 1098–1110. doi:10.1111/anae.15320. ISSN 0003-2409. PMID 33332606.
- ^ Gottlieb, M; Holladay, D; Peksa, GD (January 2019). «Ultrasound-assisted Lumbar Punctures: A Systematic Review and Meta-Analysis». Academic Emergency Medicine. 26 (1): 85–96. doi:10.1111/acem.13558. PMID 30129102.
- ^ Doherty, Carolynne M; Forbes, Raeburn B (2014). «Diagnostic Lumbar Puncture». The Ulster Medical Journal. 83 (2): 93–102. ISSN 0041-6193. PMC 4113153. PMID 25075138.
- ^ a b c d e f g Sempere, AP; Berenguer-Ruiz, L; Lezcano-Rodas, M; Mira-Berenguer, F; Waez, M (2007). «Punción lumbar: indicaciones, contraindicaciones, complicaciones y técnica de realización» [Lumbar puncture: its indications, contraindications, complications and technique]. Revista de Neurología (in Spanish). 45 (7): 433–6. doi:10.33588/rn.4507.2007270. PMID 17918111.
- ^ Gröschel, K; Schnaudigel, S; Pilgram, S; Wasser, K; Kastrup, A (19 December 2007). «Die diagnostische Lumbalpunktion» [The diagnostic lumbar puncture]. Deutsche Medizinische Wochenschrift (in German). 133 (1/02): 39–41. doi:10.1055/s-2008-1017470. PMID 18095209. S2CID 260115550.
- ^ Matata, C; Michael, B; Garner, V; Solomon, T (24–30 October 2012). «Lumbar puncture: diagnosing acute central nervous system infections». Nursing Standard. 27 (8): 49–56, quiz 58. doi:10.7748/ns2012.10.27.8.49.c9364. PMID 23189602.
- ^ a b Visintin, C.; Mugglestone, M. A.; Fields, E. J.; Jacklin, P.; Murphy, M. S.; Pollard, A. J.; Guideline Development Group; National Institute for Health and Clinical Excellence (28 June 2010). «Management of bacterial meningitis and meningococcal septicaemia in children and young people: summary of NICE guidance». BMJ (Clinical Research Ed.). 340: c3209. doi:10.1136/bmj.c3209. PMID 20584794. S2CID 7685756.
- ^ Mann, David (2002). «The role of lumbar puncture in the diagnosis of subarachnoid hemorrhage when computed tomography is unavailable». Journal of the Canadian Association of Emergency Physicians. 4 (2): 102–105. doi:10.1017/s1481803500006205. PMID 17612428.
- ^ a b c d e f López, T; Sánchez, FJ; Garzón, JC; Muriel, C (January 2012). «Spinal anesthesia in pediatric patients». Minerva Anestesiologica. 78 (1): 78–87. doi:10.1111/j.1460-9592.2011.03769.x. PMID 22211775. S2CID 205522367.
- ^ Biousse, V. (October 2012). «Idiopathic intracranial hypertension: Diagnosis, monitoring and treatment». Revue Neurologique. 168 (10): 673–683. doi:10.1016/j.neurol.2012.07.018. PMID 22981270.
- ^ Kesler, Anat; Kupferminc, Michael (June 2013). «Idiopathic Intracranial Hypertension and Pregnancy». Clinical Obstetrics and Gynecology. 56 (2): 389–396. doi:10.1097/GRF.0b013e31828f2701. PMID 23563883. S2CID 20556772.
- ^ Gallia, Gary L; Rigamonti, Daniele; Williams, Michael A (July 2006). «The diagnosis and treatment of idiopathic normal pressure hydrocephalus». Nature Clinical Practice Neurology. 2 (7): 375–381. doi:10.1038/ncpneuro0237. PMC 5390935. PMID 16932588.
- ^ Roos, KL (March 2003). «Lumbar puncture». Seminars in Neurology. 23 (1): 105–14. doi:10.1055/s-2003-40758. PMID 12870112. S2CID 41878896.
- ^ a b Straus, Sharon E.; Thorpe, Kevin E.; Holroyd-Leduc, Jayna (25 October 2006). «How Do I Perform a Lumbar Puncture and Analyze the Results to Diagnose Bacterial Meningitis?». JAMA. 296 (16): 2012–22. doi:10.1001/jama.296.16.2012. PMID 17062865.
- ^ Zorrilla-Vaca, A; Makkar, JK (May 2017). «Effectiveness of Lateral Decubitus Position for Preventing Post-Dural Puncture Headache: A Meta-Analysis». Pain Physician. 20 (4): E521–E529. doi:10.36076/ppj.2017.E529. PMID 28535561.
- ^ «Epidural Blood Patch — Imaging Glossary — Patients — UR Medicine Imaging Sciences (Radiology) — University of Rochester Medical Center». www.urmc.rochester.edu. Retrieved 24 April 2023.
- ^ Nath, Siddharth; Koziarz, Alex; Badhiwala, Jetan H; Alhazzani, Waleed; Jaeschke, Roman; Sharma, Sunjay; Banfield, Laura; Shoamanesh, Ashkan; Singh, Sheila; Nassiri, Farshad; Oczkowski, Wieslaw; Belley-Côté, Emilie; Truant, Ray; Reddy, Kesava; Meade, Maureen O; Farrokhyar, Forough; Bala, Malgorzata M; Alshamsi, Fayez; Krag, Mette; Etxeandia-Ikobaltzeta, Itziar; Kunz, Regina; Nishida, Osamu; Matouk, Charles; Selim, Magdy; Rhodes, Andrew; Hawryluk, Gregory; Almenawer, Saleh A (March 2018). «Atraumatic versus conventional lumbar puncture needles: a systematic review and meta-analysis». The Lancet. 391 (10126): 1197–1204. doi:10.1016/S0140-6736(17)32451-0. PMID 29223694. S2CID 4436591.
- ^ Rochwerg, Bram; Almenawer, Saleh A; Siemieniuk, Reed A C; Vandvik, Per Olav; Agoritsas, Thomas; Lytvyn, Lyubov; Alhazzani, Waleed; Archambault, Patrick; D’Aragon, Frederick; Farhoumand, Pauline Darbellay; Guyatt, Gordon; Laake, Jon Henrik; Beltrán-Arroyave, Claudia; McCredie, Victoria; Price, Amy; Chabot, Christian; Zervakis, Tracy; Badhiwala, Jetan; St-Onge, Maude; Szczeklik, Wojciech; Møller, Morten Hylander; Lamontagne, Francois (22 May 2018). «Atraumatic (pencil-point) versus conventional needles for lumbar puncture: a clinical practice guideline». BMJ. 361: k1920. doi:10.1136/bmj.k1920. PMC 6364256. PMID 29789372.
- ^ Davis, A; Dobson, R; Kaninia, S; Giovannoni, G; Schmierer, K (February 2016). «Atraumatic needles for lumbar puncture: why haven’t neurologists changed?». Practical Neurology. 16 (1): 18–22. doi:10.1136/practneurol-2014-001055. PMID 26349834. S2CID 36928177.
- ^ Patel, R.; Urits, I.; Orhurhu, V.; Orhurhu, M. S.; Peck, J.; Ohuabunwa, E.; Sikorski, A.; Mehrabani, A.; Manchikanti, L.; Kaye, A. D.; Kaye, R. J.; Helmstetter, J. A.; Viswanath, O. (2020). «A Comprehensive Update on the Treatment and Management of Postdural Puncture Headache». Current Pain and Headache Reports. 24 (6): 24. doi:10.1007/s11916-020-00860-0. PMID 32323013. S2CID 216049548.
- ^ Joffe, Ari R. (29 June 2016). «Lumbar Puncture and Brain Herniation in Acute Bacterial Meningitis: A Review». Journal of Intensive Care Medicine. 22 (4): 194–207. doi:10.1177/0885066607299516. PMID 17712055. S2CID 22924383.
- ^ Ragab, Ashraf; Facharzt, Khalid Noman (2014). «Caffeine, is it effective for prevention of postdural puncture headache in young adult patients?». Egyptian Journal of Anaesthesia. 30 (2): 181–186. doi:10.1016/j.egja.2013.11.005. S2CID 71403201.
- ^ «Iatrogenic CSF Leaks from Lumbar Punctures – a commentary». 20 February 2015.
- ^ «Cerebrospinal Fluid (CSF) Leak: Symptoms & Treatment».
- ^ «Cerebrospinal Fluid Leak (CSF Leak) FAQ».
- ^ a b c d e f Wright, Ben L. C.; Lai, James T. F.; Sinclair, Alexandra J. (26 January 2012). «Cerebrospinal fluid and lumbar puncture: a practical review». Journal of Neurology. 259 (8): 1530–1545. doi:10.1007/s00415-012-6413-x. PMID 22278331. S2CID 2563483.
- ^ Shaikh, F.; Brzezinski, J.; Alexander, S.; Arzola, C.; Carvalho, J. C. A.; Beyene, J.; Sung, L. (26 March 2013). «Ultrasound imaging for lumbar punctures and epidural catheterisations: systematic review and meta-analysis». BMJ. 346 (mar26 1): f1720. doi:10.1136/bmj.f1720. PMID 23532866.
- ^ Cauley, Keith A. (October 2015). «Fluoroscopically Guided Lumbar Puncture». American Journal of Roentgenology. 205 (4): W442–W450. doi:10.2214/AJR.14.14028. PMID 26397351.
- ^ Hanson, Amy L.; Ros, Simon; Soprano, Joyce (May 2014). «Analysis of Infant Lumbar Puncture Success Rates». Pediatric Emergency Care. 30 (5): 311–314. doi:10.1097/PEC.0000000000000119. PMID 24759486. S2CID 43633453.
- ^ a b Cramer, Gregory D.; Yu, Shi-Wei (2014). «Unique Anatomic Features of the Pediatric Spine». Clinical Anatomy of the Spine, Spinal Cord, and Ans. pp. 566–585. doi:10.1016/b978-0-323-07954-9.00013-x. ISBN 978-0-323-07954-9.
- ^ a b Bonadio, William (January 2014). «Pediatric Lumbar Puncture and Cerebrospinal Fluid Analysis». The Journal of Emergency Medicine. 46 (1): 141–150. doi:10.1016/j.jemermed.2013.08.056. PMID 24188604.
- ^ Harald Kluge (2007). Atlas of CSF cytology. Thieme. pp. 45–46. ISBN 978-3-13-143161-5. Retrieved 28 October 2010.
- ^ Pearson, Justin; Fuller, Geraint (August 2012). «Lumbar punctures and cerebrospinal fluid analysis». Medicine. 40 (8): 459–462. doi:10.1016/j.mpmed.2012.05.005. S2CID 73285011.
- ^ Nigrovic, Lise E.; Chiang, Vincent W. (1 August 2000). «Cost Analysis of Enteroviral Polymerase Chain Reaction in Infants With Fever and Cerebrospinal Fluid Pleocytosis». Archives of Pediatrics & Adolescent Medicine. 154 (8): 817–821. doi:10.1001/archpedi.154.8.817. PMID 10922279.
- ^ Rand, Kenneth; Houck, Herbert; Lawrence, Robert (October 2005). «Real-Time Polymerase Chain Reaction Detection of Herpes Simplex Virus in Cerebrospinal Fluid and Cost Savings from Earlier Hospital Discharge». The Journal of Molecular Diagnostics. 7 (4): 511–516. doi:10.1016/S1525-1578(10)60582-X. PMC 1888494. PMID 16237221.
- ^ Zerpa, R; Huicho, L; Guillén, A (September 1996). «Modified India ink preparation for Cryptococcus neoformans in cerebrospinal fluid specimens». Journal of Clinical Microbiology. 34 (9): 2290–1. doi:10.1128/JCM.34.9.2290-2291.1996. PMC 229234. PMID 8862601.
- ^ Shashikala.; Kanungo, R; Srinivasan, S; Mathew, R; Kannan, M (2004). «Unusual morphological forms of Cryptococcus neoformans in cerebrospinal fluid». Indian Journal of Medical Microbiology. 22 (3): 188–90. doi:10.1016/S0255-0857(21)02835-8. PMID 17642731.
- ^ Antinori, S; Radice, A; Galimberti, L; Magni, C; Fasan, M; Parravicini, C (November 2005). «The role of cryptococcal antigen assay in diagnosis and monitoring of cryptococcal meningitis». Journal of Clinical Microbiology. 43 (11): 5828–9. doi:10.1128/JCM.43.11.5828-5829.2005. PMC 1287839. PMID 16272534.
- ^ Nigrovic, Lise E.; Kimia, Amir A.; Shah, Samir S.; Neuman, Mark I. (9 February 2012). «Relationship between Cerebrospinal Fluid Glucose and Serum Glucose». New England Journal of Medicine. 366 (6): 576–578. doi:10.1056/NEJMc1111080. PMID 22316468.
- ^ Hendry, E (June 1939). «The blood and spinal fluid sugar and chloride content in meningitis». Archives of Disease in Childhood. 14 (78): 159–72. doi:10.1136/adc.14.78.159. PMC 1975626. PMID 21032142.
- ^ Gierson, HW; Marx, JI (April 1955). «Tuberculous meningitis: the diagnostic and prognostic significance of spinal fluid sugar and chloride». Annals of Internal Medicine. 42 (4): 902–8. doi:10.7326/0003-4819-42-4-902. PMID 14362261.
- ^ De Vivo, Darryl C.; Trifiletti, Rosario R.; Jacobson, Ronald I.; Ronen, Gabriel M.; Behmand, Ramin A.; Harik, Sami I. (5 September 1991). «Defective Glucose Transport across the Blood-Brain Barrier as a Cause of Persistent Hypoglycorrhachia, Seizures, and Developmental Delay». New England Journal of Medicine. 325 (10): 703–709. doi:10.1056/NEJM199109053251006. PMID 1714544.
- ^ a b Leen, Wilhelmina G.; Willemsen, Michèl A.; Wevers, Ron A.; Verbeek, Marcel M.; Mendelson, John E. (6 August 2012). «Cerebrospinal Fluid Glucose and Lactate: Age-Specific Reference Values and Implications for Clinical Practice». PLOS ONE. 7 (8): e42745. Bibcode:2012PLoSO…742745L. doi:10.1371/journal.pone.0042745. PMC 3412827. PMID 22880096.
- ^ Servo, C; Pitkänen, E (December 1975). «Variation in polyol levels in cerebrospinal fluid and serum in diabetic patients». Diabetologia. 11 (6): 575–80. doi:10.1007/BF01222109. PMID 1205026.
- ^ «Cerebrospinal Fluid Glutamine». clinicallabtesting.com. Archived from the original on 11 August 2013. Retrieved 11 August 2013.
- ^ Hourani, Benjamin T.; Hamlin, EM; Reynolds, TB (1 June 1971). «Cerebrospinal Fluid Glutamine as a Measure of Hepatic Encephalopathy». Archives of Internal Medicine. 127 (6): 1033–6. doi:10.1001/archinte.1971.00310180049005. PMID 5578559.
- ^ a b Cascino, A.; Cangiano, C.; Fiaccadori, F.; Ghinelli, F.; Merli, M.; Pelosi, G.; Riggio, O.; Rossi Fanelli, F.; Sacchini, D.; Stortoni, M.; Capocaccia, L. (September 1982). «Plasma and cerebrospinal fluid amino acid patterns in hepatic encephalopathy». Digestive Diseases and Sciences. 27 (9): 828–32. doi:10.1007/BF01391377. PMID 7105954. S2CID 8186910.
- ^ Glasgow, Allen M.; Dhiensiri, Kamnual (June 1974). «Improved Assay for Spinal Fluid Glutamine, and Values for Children with Reye’s Syndrome» (PDF). Clinical Chemistry. 20 (6): 642–644. doi:10.1093/clinchem/20.6.642. PMID 4830166.
- ^ Watanabe, A; Takei, N; Higashi, T; Shiota, T; Nakatsukasa, H; Fujiwara, M; Sakata, T; Nagashima, H (October 1984). «Glutamic acid and glutamine levels in serum and cerebrospinal fluid in hepatic encephalopathy». Biochemical Medicine. 32 (2): 225–31. doi:10.1016/0006-2944(84)90076-0. PMID 6150706.
- ^ Levine, J; Panchalingam, K; Rapoport, A; Gershon, S; McClure, RJ; Pettegrew, JW (1 April 2000). «Increased cerebrospinal fluid glutamine levels in depressed patients». Biological Psychiatry. 47 (7): 586–93. doi:10.1016/S0006-3223(99)00284-X. PMID 10745050. S2CID 33396490.
- ^ Jay H. Stein (1998). Internal Medicine. Elsevier Health Sciences. pp. 1408–. ISBN 978-0-8151-8698-4. Retrieved 12 August 2013.
- ^ Reiber, Hansotto (2003). «Proteins in cerebrospinal fluid and blood: Barriers, CSF flow rate and source-related dynamics» (PDF). Restorative Neurology and Neuroscience. 21 (3–4): 79–96. PMID 14530572.
- ^ Conly, John M.; Ronald, Allan R. (July 1983). «Cerebrospinal fluid as a diagnostic body fluid». The American Journal of Medicine. 75 (1): 102–108. doi:10.1016/0002-9343(83)90080-3. PMID 6349337.
- ^ a b c Pearson, Justin; Fuller, Geraint (August 2012). «Lumbar punctures and cerebrospinal fluid analysis». Medicine. 40 (8): 459–462. doi:10.1016/j.mpmed.2012.05.005. S2CID 73285011.
- ^ Wynter W. E. (1891). «Four Cases of Tubercular Meningitis in Which Paracentesis of the Theca Vertebralis Was Performed for the Relief of Fluid Pressure». Lancet. 1 (3531): 981–2. doi:10.1016/S0140-6736(02)16784-5.
- ^ Quincke, H (1891). «Verhandlungen des Congresses für Innere Medizin» [Negotiations of the Congress of Internal Medicine]. Proceedings of the Zehnter Congress (in German): 321–31.
- ^ Quincke HI (1902). Die Technik der Lumbalpunktion [The technique of lumbar puncture] (in German). Berlin & Vienna.
{{cite book}}: CS1 maint: location missing publisher (link)[page needed] - ^ Heinrich Irenaeus Quincke at Who Named It?
- ^ Susan E. Lederer (1997). Subjected to Science: Human Experimentation in America Before the Second World War. JHU Press. p. 216. ISBN 978-0-8018-5709-6. Page 62 has a reference to an 1896 publication in Boston Med. Surg. J
Further reading[edit]
- Ellenby, MS; Tegtmeyer, K; Lai, S; Braner, DA (28 September 2006). «Lumbar puncture». Videos in clinical medicine. The New England Journal of Medicine. 355 (13): e12. doi:10.1056/NEJMvcm054952. PMID 17005943.
External links[edit]
Media related to Lumbar puncture at Wikimedia Commons
Люмбальная пункция выполняется для забора спинномозговой жидкости СМЖ (синоним – ликвора), омывающей головной и спинной мозг. В норме в ликворе не должны выявляться вирусы, бактерии, воспалительные клетки – лейкоциты, а также олигоклональные антитела. Если же в спинномозговой жидкости мы обнаруживаем какой-либо патологический агент, то становится возможным точно определить причину заболевания. Например, выявление олигоклональных антител и 2-й тип их синтеза позволяет с большой вероятностью установить диагноз рассеянного склероза.
Записаться на консультацию
Как проводится процедура?
Пациента просят лечь на бок, согнуть голову и прижать согнутые колени к животу, т.е. принять позу эмбриона. Иногда пункцию делают в положении сидя, тогда тоже просят максимально наклониться вперед. Сгибание спины необходимо для того, чтобы увеличить расстояние между соседними позвонками в поясничной области и сократить расстояние от кожи до спинномозгового канала. Перед пункцией выполняют местную анестезию. Прокол выполняю внизу спины в пространство между спинальными отростками 5 или 4 поясничных позвонков. В процессе введения иглы вы можете почувствовать небольшой дискомфорт, но болевых ощущений обычно не возникает из-за местной анестезии. После попадания иглы в спинномозговой канал из просвета иглы начинает отходить ликвор. Обычно забирается 3-5 мл жидкости. Вся процедура обычно занимает около 10 минут. В течение дня-двух после пункции может беспокоить дискомфорт в месте инъекции. Однако болезненные ощущения скорее связаны с раздражающим действием анестетика, чем непосредственно с микротравмой при введении иглы. Пункцию стараются выполнять в первой половине дня, чтобы успеть отправить образец СМЖ в лабораторию.
Можно ли повредить спинной мозг во время пункции?
Несмотря на то, что игла вводится в пространство, где расположен спинной мозг, его травма при стандартной процедуре забора ликвора у взрослых исключена. Дело в том, что спинной мозг заполняет канал на всем протяжении только у младенцев. Рост позвоночника существенно обгоняет рост спинного мозга, поэтому последний как бы «приподнимается вверх», и его нижняя граница оказывается на уровне 1 поясничного позвонка. Оставшееся пространство представляет собой мешок, заполненный жидкостью, в котором находятся корешки спинномозговых нервов, направляющиеся вниз к «своим» отверстиям в позвоночнике. Повредить иглой корешок также сложно, как проткнуть иголкой вермишель в бульоне. Травма межпозвонкового диска исключена, так как игла вводится с противоположной стороны позвонка.
Какие побочные эффекты можно ожидать после пункции?
Наиболее частым (примерно у 20% пациентов) нежелательным эффектом люмбальной пункции является головная боль. Снижение давления ликвора может вызвать раздражение оболочек мозга, содержащих болевые рецепторы. Такой перепад давления наиболее значителен при переходе в вертикальное положение. Поэтому непосредственно после пункции необходимо лежать в течение 2-х часов. Также в течение последующих 2-3 дней рекомендуется исключить физические нагрузки и, по возможности, 2-3 раза в течение дня полежать 30 минут. Головная боль возникает в вертикальном положении и проходит в горизонтальном. Обычные обезболивающие лекарства при постпункционной головной боли, как правило, малоэффективны, лучший способ лечения – принять горизонтальное положение.
Много ли ликвора забирается во время люмбальной пункции?
Общий объем СМЖ взрослого человека составляет от 140 до 270 мл. Ежесуточно вырабатывается 600—700 миллилитров жидкости, то есть ликвор полностью обновляется примерно 4 раза в день. В процессе люмбальной пункции извлекается обычно 3-5 мл жидкости. Таким образом, извлекаемый объем СМЖ довольно незначителен в сравнении с общим объемом ее циркуляции. Предпочтительно выполнять люмбальную пункцию как можно более тонкой иглой, чтобы ликвор не просачивался через прокол. Для быстрого восполнения объема ликвора, можно ускорить его продукцию. С этой целью рекомендуется прием достаточного количества жидкости (не менее 2 литров минеральной воды в день), а также кофе (по 2-3 чашки в день).
Насколько важна люмбальная пункция?
Хотя люмбальная пункция представляет собой инвазивную процедуру, в целом переносится хорошо, не болезненнее забора крови, а диагностическая информация, получаемая после пункции бесценна. А это в свою очередь ускоряет диагностику и позволяет назначить лечение как можно раньше.
Люмбальная пункция – это диагностическая или лечебная процедура, которая выполняется посредством введения иглы в субарахноидальное пространство спинного мозга.
Чаще всего она состоит в заборе образца спинномозговой жидкости, которая циркулирует между мягкой и паутинными оболочками.
Спинной мозг покрывают три оболочки. Внутренняя – мягкая оболочка, средняя – паутинная и внешняя – твердая. В пространстве между двумя внутренними оболочками, мягкой и паутинной (оно называется субарахноидальным) находится спинномозговая жидкость, или ликвор.
При люмбальной пункции врач делает забор ликвора из пространства между внутренними оболочками.
Или врач делает инъекцию препарата, например, обезболивающего (лидокаина). Такая процедура называется эпидуральной блокадой и применяется при хирургических операциях, а также для облегчения болевого синдрома при межпозвоночной грыже, остром радикулите.

Наш эксперт в этой сфере:

Нурутдинова Эльза Ниазовна
Врач-невролог
Показания
Обычно люмбальная пункция делается при необходимости уточнения диагноза, недостаточной информативности МРТ, КТ.
Основные показания:
- подозрение на энцефалит, менингит, арахноидит, нейросифилис или иное инфекционное заболевание центральной нервной системы,
- подозрение на субарахноидальное кровоизлияние,
- диагностика рассеянного склероза,
- диагностика злокачественных опухолей и метастазов,
- подозрение на нейролейкоз (нейролейкемию).
Также люмбальная пункция нередко используется при диагностике полинейропатии, аутоиммунных заболеваний (системная красная волчанка, ревматизм, др.), паранеопластического синдрома, для выяснения причины ликвореи (истечения спинномозговой жидкости).
При исследовании ликвора оцениваются его прозрачность, цвет, исследуется клеточный состав, проводятся биохимический анализ, микробиологические тесты.
В частности, наличие большого количества иммуноглобулинов, белковых продуктов распада миелина имеет существенное значение для диагностики рассеянного склероза.
Во время процедуры измеряется ликворное давление (в норме оно составляет 100 – 200 мм водного столба).
В лечебных целях люмбальная пункция применяется для снижения внутричерепного давления, санации ликвора, введения химиопрепаратов (цитостатиков), антибиотиков, обезболивающих препаратов или иных лекарственных средств.
Подготовка к процедуре
Перед проведением люмбальной пункции проводятся:
- общий и биохимический анализы крови, мочи,
- коагулограмма,
- измерение внутричерепного давления,
- изменение давления глазного дна.
Если люмбальная пункция составляет часть диагностики неврологического заболевания, перед ее проведением обычно делается МРТ или КТ головного мозга.
Как проводится процедура
В Международной клинике Медика24 люмбальную пункцию выполняют врачи с большим опытом, высокой квалификацией, что практически исключает любые осложнения.
Процедура проводится в полном соответствии с протоколами, принятыми в мировой практике (Европы, США, Израиля). Полученные данные исследования заносятся в историю болезни и будут приняты и однозначно истолкованы в любой клинике мира.
Некоторое время после проведения процедуры требуется врачебное наблюдение. В палатах стационара нашей клиники созданы максимально комфортные условия, а профессиональный медицинский персонал обеспечивает лучшие стандарты медицинского ухода.
Люмбальная пункция выполняется очень тонкой иглой, поэтому сама по себе эта процедура почти безболезненная. Тем не менее, при ее проведении используется местная анестезия.
Игла вводится в промежуток между 3 и 4 поясничными позвонками (L3-L4) или между 2 и 3 позвонками (L2 – L3).
Во время люмбальной пункции пациент лежит на боку в позе эмбриона – с опущенной головой и прижатыми к торсу ногами.
Для процедуры используется игла с мандреном. При прокалывании связки и твердой мозговой оболочки ощущается сопротивление. Когда игла проникает в субарахноидальное пространство, ее вхождение становится легким (она как бы проваливается). Для опытного врача это исключает ошибку, поэтому дополнительные средства визуализации, контроля (УЗИ, КТ) для процедуры не требуются.
После вхождения иглы в субарахноидальное пространство к ней присоединяется манометр, измеряется ликворное давление.
Объем забора ликвора обычно составляет 10 – 20 мл. Общий объем спинномозговой жидкости составляет около 120 мл, а ее суточная секреция – 500 мл.
Это значит, что в течение суток спинномозговая жидкость обновляется четыре раза. Поэтому забор ликвора при люмбальной пункции практически не влияет на его объем, давление и циркуляцию.
В зависимости от показаний, образец ликвора помещается в одну пробирку или разделяется на несколько пробирок.
В одну пробирку помещается образец для биохимического анализа, измерения уровня глюкозы, белка.
В другую пробирку помещается образец жидкости для исследования ее клеточного состава.
В третью – для бактериологического исследования.
Процедура занимает совсем немного времени и может быть проведена в условиях дневного стационара Международной клиники Медика24.
Что показывает люмбальная пункция
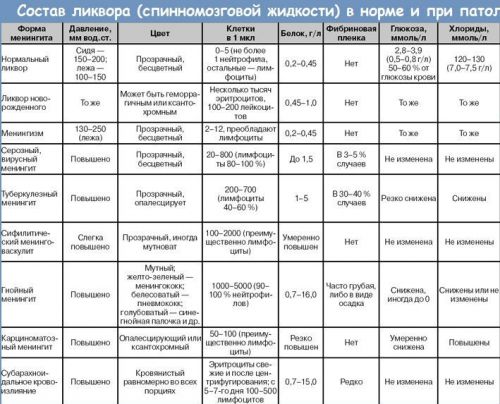
В норме ликвор должен быть бесцветным, прозрачным, содержание белка составляет от 150 мг/л до 450 мг/л, количество глюкозы – до 60% от содержания в крови, лейкоциты не более 5000 в 1 мм3, эритроциты, нейтрофилы отсутствуют.
Любые отклонения от нормы могут указывать на те или иные патологии.
В частности, кровянистый цвет ликвора сообщает о субарахноидальном кровоизлиянии, желтоватый цвет – на геморрагический процесс поздней стадии, серовато-зеленый – на злокачественную опухоль головного мозга.
Мы вам перезвоним
Записаться на прием

Сообщение отправлено!
ожидайте звонка, мы свяжемся с вами в ближайшее время
Возможные осложнения
Несмотря на то, что при люмбальной пункции забирается незначительный объем ликвора, который быстро восстанавливается, это все же может послужить причиной снижения внутричерепного давления и возникновения кратковременных головных болей. Такой побочный эффект возникает в среднем в 15% случаев.
Эти головные боли проходят самостоятельно в течение 3 – 5 дней и не представляют опасности.
Другие осложнения бывают связаны с врачебными ошибками, что при высокой квалификации специалистов Международной клиники Медика24 практически исключено.