Применение дозированного аэрозольного ингалятора (даи)
Ингаляцию выполняют в следующей
последовательности:
-
снять защитный колпачок с мундштука,
встряхнуть баллончик с аэрозолем и
перевернуть дном вверх; -
встать, сделать глубокий выдох, слегка
запрокинуть голову назад, обхватить
мундштук ингалятора губами (баллончик
должен быть направлен дном кверху); -
нажать на дно баллончика и одновременно(!)
сделать максимальной глубокий вдох. В
этот момент происходит выброс одной
ингаляционной дозы. -
задержать дыхание, не выдыхая воздух
по возможности досчитать до десяти,
чтобы препарат осел на стенках бронхов,
вынуть мундштук изо рта; -
сделать выдох. Надеть защитный колпачок
на мундштук.
При необходимости можно повторить
ингаляцию через 1-2 минуты. Медсестра
должна проверить как больной выполнил
ингаляцию лекарства.
Самое главное – необходимым
условием правильного применения ДАИ
является синхронизация вдоха и нажатия
на баллончик (маневр «рука-легкие»).
Много больных допускают различные
ошибки в технике ингаляции.
Наиболее распространенные ошибки при
использовании карманного ингалятора:
-
больной забывает встряхнуть ингалятор
перед применением; -
не обхватывает мундштук губами и держит
на расстоянии от полости рта; -
при проведении ингаляции голова
наклонена вперед, при этом частицы
лекарственного препарата ударяются о
заднюю стенку глотки и частично прилипают
к ней; -
во время вдоха несколько раз нажимают
на дно аэрозольного баллончика; -
вдох и нажатие на баллончик проводят
не синхронно, нажимают на дно баллончика
в конце вдоха; -
не задерживают дыхание на высоте вдоха.
Эффективность применения ингалятора
зависит от правильной техники его
применения. У некоторых пациентов –
маленьких детей, стариков, при нарушении
сознания (оглушении) невозможно
использовать дозированные аэрозольные
ингаляторы и следует применять другие
ингаляционные устройства (небулайзеры).
В последние годы большинство выпускаемых
дозированных ингаляторов не содержать
фреона, т.е. являются безфреоновыми. В
баллончиках ингалятора вместо фреона
используется гидрофторалкан – безвредный
для окружающей среды и человека
наполнитель (пропелент), который не
разрушает озоновый слой атмосферы.
Безфреоновые ДАИ содержат бронхорасширяющие
лекарства и маркируются буквой Н:
беродуал Н, беротек Н. преимуществами
безфреоновых ингаляторов кроме отсутствия
разрушения озонового слоя атмосферы
являются так же:
— более низкая скорость струи аэрозоля
(не возникает кашель в момент ингаляции);
— не нужно встряхивать ингалятор перед
применением;
— меньше накопление (депозиция) препарата
в ротоглотке;
— можно использовать даже при низких
температурах окружающей среды;
— безфреоновые ДАИ образуют
ультрамелкодисперстный аэрозоль, более
эффективно проникающий в бронхи, чем
фреоносодержащие аэрозоли.
Перед использованием безфреонового
ДАИ (беротек Н, беродуал Н) в первый раз
надо дважды нажать на дно баллончика.
Если баллончик не использовался более
трех дней, перед применением следует
однократно нажать на дно баллончика до
появления облака аэрозоля.
Значительно облегчают использование
дозированного аэрозольного ингалятора
– применение спейсера – специального
приспособления в виде пластиковой
камеры различного объема. Спейсер
повышает эффективность ингаляционного
лечения, упрощает технику ингаляции и
уменьшает потенциальный риск развития
побочных реакций. Правила пользования
спейсером очень простые – с одного
конца в спейсер вставляется ингалятор,
а через отверстие с противоположного
конца спейсера больной совершает
спокойный глубокий вдох. При этом
препарат находится внутри спейсера и
необходимость в быстром вдохе с
одновременным нажатием на ингалятор
отпадает.
Спейсер повышает эффективность лечения,
так как больше лекарства попадает в
бронхолегочную систему и меньше оседает
в полости рта и глотки. Крупные, «тяжелые»
частицы аэрозоля остаются на стенках
спейсера. Существует много видов
спейсеров, у которых есть мундштук.
Некоторые снабжены маской для лица.
В последние годы для облегчения техники
ингаляции появились устройства
активируемые вдохом – ингалятор «Легкое
дыхание». Этот ингалятор обладает
важными преимуществами – простотой и
удобной техникой ингаляции и надежной
доставкой лекарства в дыхательные пути.
Ингалятор «Легкое дыхание», активируемый
вдохом пациента, не требует от больного
синхронизации вдоха и активации
ингалятора, а так же усилий при вдохе.
Скорость вдоха при этом может быть
минимальной и под силу большинству
больных.
Техника ингаляции при использовании
ингалятора «легкое дыхание» очень
простая:
— открыть крышку
— сделать вдох
— задержать дыхание, сосчитав до десяти
— закрыть крышку
— при проведении более одной ингаляции
нужно закрыть крышку ингалятора и
повторить процесс.
Не требуется встряхивать баллончик,
нажимать на дно ингалятора, раскручивать
ингалятор.
При использовании ингалятора «Легкое
дыхание» лекарство попадает в бронхиальное
дерево даже при небольшой скорости
вдоха, поэтому его можно успешно применять
у пациентов с выраженной обструкцией
(сужением) дыхательных путей и низкой
скоростью вдоха.
Некоторые больные бронхиальной астмой
избегают пользоваться ингалятором,
считая что к ингалятору можно привыкнуть.
Это мнение является неправильным.
Лекарства, которые находятся в ингаляторе,
привыкания не вызывают. Другое дело,
что течение астмы при недостаточном,
неправильном лечении, может быть такого,
что постоянные обострения заставляют
больного прибегать к помощи ингалятора
слишком часто. Частое использование
ингалятора (больше 3 раз в сутки) говорит
о том, что контроль над астмой неполный
и является сигналом, что следует
обратиться к врачу, чтобы откорректировать
лечение.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Применение дозированного аэрозольного ингалятора (даи)
Ингаляцию выполняют в следующей
последовательности:
-
снять защитный колпачок с мундштука,
встряхнуть баллончик с аэрозолем и
перевернуть дном вверх; -
встать, сделать глубокий выдох, слегка
запрокинуть голову назад, обхватить
мундштук ингалятора губами (баллончик
должен быть направлен дном кверху); -
нажать на дно баллончика и одновременно(!)
сделать максимальной глубокий вдох. В
этот момент происходит выброс одной
ингаляционной дозы. -
задержать дыхание, не выдыхая воздух
по возможности досчитать до десяти,
чтобы препарат осел на стенках бронхов,
вынуть мундштук изо рта; -
сделать выдох. Надеть защитный колпачок
на мундштук.
При необходимости можно повторить
ингаляцию через 1-2 минуты. Медсестра
должна проверить как больной выполнил
ингаляцию лекарства.
Самое главное – необходимым
условием правильного применения ДАИ
является синхронизация вдоха и нажатия
на баллончик (маневр «рука-легкие»).
Много больных допускают различные
ошибки в технике ингаляции.
Наиболее распространенные ошибки при
использовании карманного ингалятора:
-
больной забывает встряхнуть ингалятор
перед применением; -
не обхватывает мундштук губами и держит
на расстоянии от полости рта; -
при проведении ингаляции голова
наклонена вперед, при этом частицы
лекарственного препарата ударяются о
заднюю стенку глотки и частично прилипают
к ней; -
во время вдоха несколько раз нажимают
на дно аэрозольного баллончика; -
вдох и нажатие на баллончик проводят
не синхронно, нажимают на дно баллончика
в конце вдоха; -
не задерживают дыхание на высоте вдоха.
Эффективность применения ингалятора
зависит от правильной техники его
применения. У некоторых пациентов –
маленьких детей, стариков, при нарушении
сознания (оглушении) невозможно
использовать дозированные аэрозольные
ингаляторы и следует применять другие
ингаляционные устройства (небулайзеры).
В последние годы большинство выпускаемых
дозированных ингаляторов не содержать
фреона, т.е. являются безфреоновыми. В
баллончиках ингалятора вместо фреона
используется гидрофторалкан – безвредный
для окружающей среды и человека
наполнитель (пропелент), который не
разрушает озоновый слой атмосферы.
Безфреоновые ДАИ содержат бронхорасширяющие
лекарства и маркируются буквой Н:
беродуал Н, беротек Н. преимуществами
безфреоновых ингаляторов кроме отсутствия
разрушения озонового слоя атмосферы
являются так же:
— более низкая скорость струи аэрозоля
(не возникает кашель в момент ингаляции);
— не нужно встряхивать ингалятор перед
применением;
— меньше накопление (депозиция) препарата
в ротоглотке;
— можно использовать даже при низких
температурах окружающей среды;
— безфреоновые ДАИ образуют
ультрамелкодисперстный аэрозоль, более
эффективно проникающий в бронхи, чем
фреоносодержащие аэрозоли.
Перед использованием безфреонового
ДАИ (беротек Н, беродуал Н) в первый раз
надо дважды нажать на дно баллончика.
Если баллончик не использовался более
трех дней, перед применением следует
однократно нажать на дно баллончика до
появления облака аэрозоля.
Значительно облегчают использование
дозированного аэрозольного ингалятора
– применение спейсера – специального
приспособления в виде пластиковой
камеры различного объема. Спейсер
повышает эффективность ингаляционного
лечения, упрощает технику ингаляции и
уменьшает потенциальный риск развития
побочных реакций. Правила пользования
спейсером очень простые – с одного
конца в спейсер вставляется ингалятор,
а через отверстие с противоположного
конца спейсера больной совершает
спокойный глубокий вдох. При этом
препарат находится внутри спейсера и
необходимость в быстром вдохе с
одновременным нажатием на ингалятор
отпадает.
Спейсер повышает эффективность лечения,
так как больше лекарства попадает в
бронхолегочную систему и меньше оседает
в полости рта и глотки. Крупные, «тяжелые»
частицы аэрозоля остаются на стенках
спейсера. Существует много видов
спейсеров, у которых есть мундштук.
Некоторые снабжены маской для лица.
В последние годы для облегчения техники
ингаляции появились устройства
активируемые вдохом – ингалятор «Легкое
дыхание». Этот ингалятор обладает
важными преимуществами – простотой и
удобной техникой ингаляции и надежной
доставкой лекарства в дыхательные пути.
Ингалятор «Легкое дыхание», активируемый
вдохом пациента, не требует от больного
синхронизации вдоха и активации
ингалятора, а так же усилий при вдохе.
Скорость вдоха при этом может быть
минимальной и под силу большинству
больных.
Техника ингаляции при использовании
ингалятора «легкое дыхание» очень
простая:
— открыть крышку
— сделать вдох
— задержать дыхание, сосчитав до десяти
— закрыть крышку
— при проведении более одной ингаляции
нужно закрыть крышку ингалятора и
повторить процесс.
Не требуется встряхивать баллончик,
нажимать на дно ингалятора, раскручивать
ингалятор.
При использовании ингалятора «Легкое
дыхание» лекарство попадает в бронхиальное
дерево даже при небольшой скорости
вдоха, поэтому его можно успешно применять
у пациентов с выраженной обструкцией
(сужением) дыхательных путей и низкой
скоростью вдоха.
Некоторые больные бронхиальной астмой
избегают пользоваться ингалятором,
считая что к ингалятору можно привыкнуть.
Это мнение является неправильным.
Лекарства, которые находятся в ингаляторе,
привыкания не вызывают. Другое дело,
что течение астмы при недостаточном,
неправильном лечении, может быть такого,
что постоянные обострения заставляют
больного прибегать к помощи ингалятора
слишком часто. Частое использование
ингалятора (больше 3 раз в сутки) говорит
о том, что контроль над астмой неполный
и является сигналом, что следует
обратиться к врачу, чтобы откорректировать
лечение.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Условия эффективности ингаляционной терапии
И.Э. Степанян
В статье рассматриваются особенности и сравнительная эффективность различных ингаляционных устройств. Особое внимание уделяется ошибкам при использовании дозированных аэрозольных ингаляторов и дозированных порошковых ингаляторов, а также особенностям экстрамелкодисперсных аэрозолей.
Ключевые слова: ингаляционные устройства, бронхиальная астма, хроническая обструктивная болезнь легких, дозированные аэрозольные ингаляторы, дозированные порошковые ингаляторы, экстрамелкодисперсные аэрозоли, легочная депозиция, ошибки при ингаляции, формотерол.
Ингаляционный путь введения лекарств широко применяется в лечении пациентов с заболеваниями органов дыхания: бронхиальной астмой, хронической обструк-тивной болезнью легких, муковисцидозом, бронхоэкта-тической болезнью, острым и хроническим бронхитом, артериальной легочной гипертензией. Прямая доставка препаратов к месту их действия в дыхательных путях позволяет добиться требуемого результата с использованием малых доз действующих веществ и минимизировать системные эффекты. Среди препаратов, применяемых ингаляционно, — бронхорасширяющие средства разных фармакологических групп, глюкокортикостероиды (ГКС), муколитики, антибиотики, антисептики, противогрибковые средства и др.
Виды ингаляционных устройств
За последние полвека было создано множество ингаляционных лекарственных препаратов и устройств для их доставки. Всё разнообразие ингаляционных устройств можно подразделить на следующие группы:
• дозированные аэрозольные ингаляторы (ДАИ), в том числе применяемые со спейсерами и клапанными аэрозольными камерами;
• ДАИ, активируемые вдохом;
• дозированные порошковые ингаляторы (ДПИ);
• небулайзеры;
• ингаляторы «мягкого» аэрозоля (soft mist inhalers).
Каждая группа устройств обладает определенными преимуществами и недостатками. В целом эффективность ингаляционной терапии определяется легочной депозици-ей вдыхаемых частиц, которая зависит от их размера и правильности выполнения дыхательных маневров пациентом. Нарушение проходимости дыхательных путей и турбулентность вдыхаемого воздушного потока в местах деления бронхов препятствуют проникновению частиц лекарств в периферические дыхательные пути.
Бурное развитие техники для ингаляционной терапии породило проблему выбора оптимального ингалятора для применения у той или иной категории пациентов. В 2011 г. Европейское респираторное общество опубликовало рекомендации по ингаляционной терапии в пульмонологической практике [1]. В этих рекомендациях сделан акцент на необходимости соблюдения пациентами правильной техники ингаляции и контроля со стороны врача за правильно-
Игорь Эмильевич Степанян — профессор, вед. науч. сотр. отдела дифференциальной диагностики туберкулеза легких и экстракорпоральных методов лечения Центрального НИИ туберкулеза РАМН, Москва.
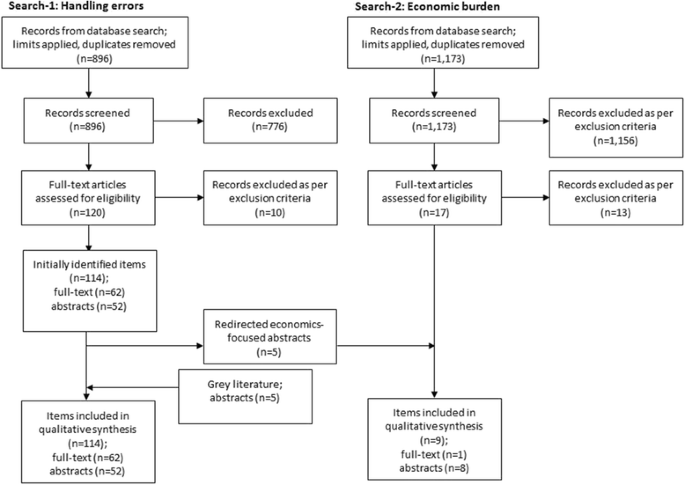
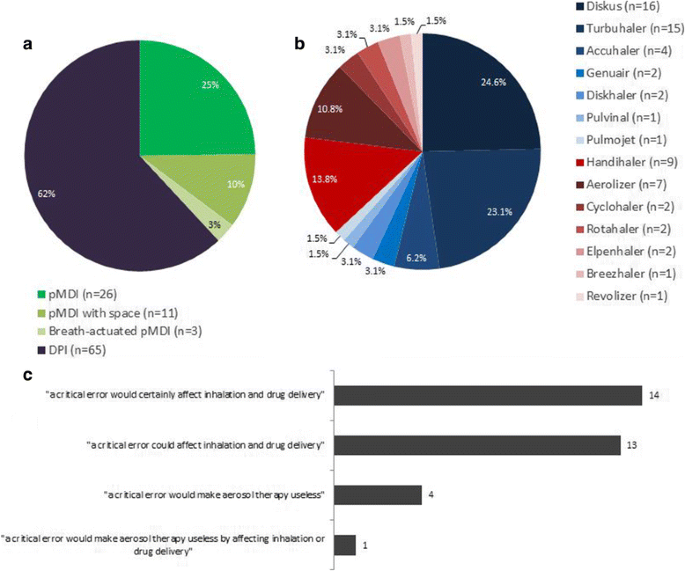
стью пользования ингаляционными устройствами для достижения оптимального эффекта ингаляционной терапии. На практике эти правила довольно часто не соблюдаются. Так, было установлено, что, по крайней мере, одну ошибку в технике ингаляции допускают 76% пациентов, пользующихся ДАИ, и 49-54% больных, применяющих ДАИ, активируемые вдохом; от 4 до 94% пациентов неправильно пользуются ДПИ, а 25% никогда не обучались правильной технике ингаляции [2, 3].
Ошибки при использовании ДАИ и ДПИ
На протяжении многих лет основной проблемой при пользовании ДАИ остается координация вдоха с активацией ингалятора [4].
Факторами, достоверно повышающими риск критических ошибок при ингаляции с помощью ДАИ и ДПИ, являются:
Таблица 1. Ошибки пациентов при использовании ДАИ
Правила ингаляции Частота ошибок, %
Удалить защитный колпачок 0,15*
Встряхнуть ингалятор (в случае суспензии) 37
Произвести полный выдох перед активацией ингалятора 50
Держать ингалятор вертикально донышком вверх 9
Разместить загубник между губами, поверх языка, не перекрывая просвет 0,7*
Выполнить только одну активацию ингалятора во время вдоха 19
Выполнить активацию ингалятора в начале вдоха 18 — во второй половине вдоха, 5* — после окончания вдоха
Вдыхать глубоко и медленно (не прерывать вдох сразу после активации ингалятора) 10* — прерывание вдоха, 52 — форсированный вдох
Вдыхать через рот (не через нос) 2*
Задержать дыхание на 10 с на высоте вдоха 53
* Критические ошибки.
с
Таблица 2. Ошибки пациентов при использовании ДПИ
Правила ингаляции V Технические ошибки, % от числа всех пациентов
Аэролайзер/ХандиХалер Мультидиск Турбухалер
Удалить/повернуть крышку* 0 0,65 0
Вставить капсулу* 9 Неприменимо Неприменимо
Проколоть капсулу* 3 Неприменимо Неприменимо
Правильно загрузить дозу* Неприменимо 7,3 14
Держать ингалятор вертикально Неприменимо Неприменимо 23
Произвести полный выдох (не в ингалятор) 19 22 14
Разместить загубник между губами* 5 5 4
Вдыхать глубоко (не прерывать вдох сразу после активации ингалятора) 26 29 22
Вдыхать быстро (форсированный вдох)* 24 28 22
Вдыхать через рот (не через нос)* 2 1 0
Задержать дыхание на высоте вдоха 25 32 28
Выдохнуть не через загубник ингалятора 19 21 11
Проверить, что капсула не содержит остатков порошка 30 Неприменимо Неприменимо
* Критические ошибки.
• пожилои или детскии возраст;
• отсутствие инструктажа со стороны врача;
• деменция;
• низкий уровень образования;
• использование больным ингаляторов разных типов.
Неправильное пользование ингаляторами приводит к неполному контролю заболевания, более частому возникновению потребности в назначении пероральных ГКС и антибиотиков, увеличивает риск госпитализации [5, 6].
В табл. 1 и 2 суммированы ошибки, допускаемые пациентами при пользовании ДАИ и ДПИ, по данным А^. Ме!ап1 е! а!. [5]. Это многоцентровое наблюдательное исследование было проведено у 1664 больных хронической обструк-тивной болезнью легких и бронхиальной астмой, имеющих опыт использования ингаляторов (оценка проводилась с тем устройством, которым пользуется конкретный пациент). Критическими считались ошибки, которые существенно снижают легочную депозицию препарата. Результаты исследования свидетельствуют о том, что при исполь-
5 г
II
ill I з о
Ct £ ГО
о. 1 m ™
я I
2 —
1 —
0,8
Формотерол ДАИ (Атимос)
Формотерол ДПИ (Аэролайзер)
Рис. 1. Средний аэродинамический диаметр частиц аэрозоля формотерола, образуемого ДАИ и ДПИ.
зовании аэрозольных ингаляторов критические ошибки встречаются достоверно реже (18%), чем в случае порошковых ингаляторов (от 35 до 44% для различных устройств).
Критические ошибки пациентов сводят на нет ожидаемый эффект от ингаляционной терапии, поэтому рекомендации при каждом визите пациента проверять правильность соблюдения техники ингаляций, содержащиеся в руководствах GINA (Global Initiative for Asthma) и GOLD (Global Initiative for Chronic Obstructive Lung Disease), очень актуальны. Перед тем как назначить новый ингалятор, врач должен также оценить способность пациента правильно освоить технику пользования новым устройством.
Новые технологии производства ДАИ
В связи с вышеизложенным разработка новых препаратов и устройств для ингаляционной терапии направлена на упрощение ингаляционной техники и уменьшение вероятности ошибок, снижающих эффективность лечения. Одним из подходов к решению данной проблемы стала технология Модулит, которая была разработана компанией Chiesi для использования в бесфреоновых ДАИ. Технология Модулит, включающая добавление в лекарственную форму дополнительных компонентов и изменение геометрии устья актуа-тора, позволяет формировать аэрозольное облако с частицами заданного размера. Помимо возможности создавать экстрамелкодисперсные аэрозоли (с частицами размером менее 2 мкм) это приводит к снижению скорости аэрозоля и значительному увеличению времени «жизни» облачка аэрозоля (с 0,18 до 1,16 с).
Преимуществами технологии Модулит являются:
• возможность получать аэрозоль с частицами требуемого размера;
• уменьшение скорости струи аэрозоля;
• более продолжительное время жизни облачка аэрозоля;
• упрощение координации вдоха и нажатия на баллончик;
• уменьшение депозиции препарата в верхних дыхательных путях.
Л
с АТИМОС
i^
формотерол 12 м кг/доз«; 120 доз
АТИМОС (экстрамелкодисперсный формотерол) -беЗОШИбОЧНЫЙ Выбор для лечения пациентов
с любой категорией ХОБЛ1:
А: в монотерапии
В: в монотерапии (или в комбинации с тиотропием) С: в комбинации с ИГКС* (или с тиотропием) Р: в комбинации с ИГКС (или/и с тиотропием)
* АТИМос М<
Дэро.
ЗО/ТЬ
«агв & 5с
¿ » 1
®°Pmi
‘°герол
Входит в ЖНВЛП2 и лло3
* Ингаляционные глюкокортоюхлероцды.
1 Согласно QOLD 2011 формотерол может быть использован у всех категорий болы-ых ХОБЛ. Global Initiative for Coronta Obstructiva Lung Dlsease. Global Strategy 1or the Diagnosis, Management, and Prévention of Chranic Obstiuctive Pulmonaiy Disease. Revised 2011И www.goldcopd.org
2 Формотерол, аэрозоль для ингаляций дозированный, включен в перечень ЖНВЛП (Распоряжение Правительства Российской Федерации or 7 декабря 2011 г, Na 2199-р}
3 Приказ Минадравсоцразвитга России № 1340н от 10.11.2011 г. (Per. в MnnocreN 22368 от 23.11.2011 г.): обновленный Перечень лекарственных препаратов, вт.ч. перечень ЛП, назначаемых по решению врачебной комиссии ЛПУ, обеспечение изгорьми осуществляется в соответствии со стандартами медицинской помощи по рецептам врача (фельдшера) при оказании государственной социальной помощи в виде набора социальных услуг
ПЕРЕД ПРИМЕНЕНИЕМ НЕОБХОДИМО ОЗНАКОМИТЬСЯ С ИНСТРУКЦИЕЙ
С Chiesi
iНе можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
ООО «Кьези Фармасьютикалс»
Тел.: (495) 967-12-12, факс: (495) 967-12-11 www.chiesi.ru
Рис. 2. Легочная депозиция формотерола у одного и того же пациента после ингаляции Атимоса (а) и ДПИ формотерола (б) (сцинтиграфия после ингаляции препарата с радиоизотопной меткой).
œ
и
а.
m га
16 14 12 10 8 6 4 2 0
12,2
4,8
5,5
2,7
_1_
_1_
_1_
_1_
7,4
_1_
70 60 50 40 30 20 Скорость вдоха, л/мин
10
Рис. 3. Зависимость размера частиц аэрозоля от скорости инспираторного потока при ингаляции формотерола через порошковый ингалятор Турбухалер.
Технология Модулит была использована при создании ряда ДАИ, как с обычным размером частиц (Кленил Джет -ДАИ с компактным спейсером, содержащий беклометазо-на дипропионат), так и экстрамелкодисперсных — Фостер (беклометазона дипропионат + формотерол) и Атимос (формотерол).
Рассмотрим особенности экстрамелкодисперсных ДАИ на примере Атимоса. Атимос образует экстрамелкодисперсный аэрозоль с размером частиц менее 1 мкм по сравнению с 3,5 мкм у порошковых ингаляторов формоте-рола, что позволяет ему хорошо проникать в малые дыхательные пути (рис. 1) [7, 8].
Благодаря малому размеру частиц и ингаляционному устройству (ДАИ) Атимос обеспечивает более высокую
легочную депозицию по сравнению с ДПИ формотерола (рис. 2) [7, 9].
Следует учитывать, что размер частиц аэрозоля, образуемого порошковым ингалятором, увеличивается по мере ослабления усилия на вдохе (нарастания обструкции), что ухудшает легочную депозицию из ДПИ (рис. 3) [10].
Результаты рандомизированного двойного слепого перекрестного исследования сравнительной эффективности разовой дозы формотерола в ДАИ (Атимос), формотерола в ДПИ (Аэролайзер) и плацебо (ДАИ или Аэролайзер) у пациентов со среднетяжелой и тяжелой бронхиальной астмой показали, что за 12-часовой период наблюдения Атимос обеспечивал эквивалентное с формотеролом ДПИ улучшение объема форсированного выдоха за 1-ю секунду (площадь под фармакокинетической кривой). При этом эффект Атимоса развивался быстрее, чем у формотерола в ДПИ (5 и 7,5 мин соответственно), и сохранялся в течение 12 ч у большего числа пациентов (51 и 33% соответственно) [11].
Таким образом, преимуществами Атимоса — экстрамелкодисперсного препарата формотерола в виде ДАИ -являются:
• высокая легочная депозиция;
• стабильность доставки независимо от тяжести обструкции и силы вдоха;
• доставка препарата не только в крупные, но и в малые дыхательные пути;
• простота ингаляции и низкий риск ошибок.
Знание врачами всего спектра ингаляционных препаратов, средств доставки и правил проведения ингаляции является необходимым условием эффективности ингаляционной терапии. Большой выбор препаратов и устройств для ингаляционной терапии расширяет возможности их индивидуального подбора для конкретного пациента.
^исок литературы
1. Laube B.L. et al. // Eur.Respir. J. 2011. V. 37. P. 1308.
2. Molimard H.et al. // J. Aerosol Med. 2003. V. 16. P. 249.
3. Lavopini F. et al. // Respir. Med. 2008. V. 102. P. 593.
4. Crampton G.K. et al. // Eur. J. Respir. Dis. 1982. V. 63. P. 101.
5. Melani A.S. et al. // Respir. Med. 2011. V. 105. P. 930.
6. van der Palen J. et al. // Eur. Respir. J. 1999. V. 14. P. 1034.
7. Acerbi D. et al. // Pulm. Pharmacol. Ther. 2007. V. 20. P. 290.
8. Crée C.P. et al. // J. Aerosol Med. 2006. V. 19. P. 466.
9. Meyer T. et al. // J. Aerosol Med. 2004. V. 17. P. 43.
10. Nadarassan D.K. et al. //Eur. J. Pharm. Sei. 2010. V. 39. P. 348.
11. Bousquet J. et al. //Respiration. 2005. V. 72. Suppl. 1. P. 13. .
МОСФЕРА П
atm-press.ru
На сайте atm-press.ru вы сможете ПРИОБРЕСТИ все наши книги и журналы по издательским ценам без магазинных наценок. Также на сайте atm-press.ru В БЕСПЛАТНОМ ДОСТУПЕ вы найдете архив журналов «Атмосфера. Пульмонология и аллергология», «Астма и аллергия’ «Лечебное дело», «Атмосфера. Новости кардиологии», «Нервные болезни», «Нервы», переводы на русский язык руководств и брошюр.
×
Предупреждение
Не удалось удалить sourcerer_php_62d33f5925c06465fe60fbbefb74f7e4
коллекция

По статистике, дозирующими аэрозольными ингаляторами (ДАИ) неправильно пользуются от 7% до 64% больных. Каковы главные ошибки и как их избежать?
Вы не подготовили ингалятор к использованию
Перед первым использованием ингалятора нужно два раза распылить его содержимое в воздух. Если этого не сделать, лекарство может не оказать должного действия.
Как надо: сделайте два «пшика» в воздух с 5-секунднымим перерывами, во время которых встряхивайте баллончик; повторите эти действия, если вы не пользовались ингалятором минимум две недели.
Вы забываете встряхивать баллончик
В классическом дозирующем аэрозольном ингаляторе содержатся лекарство, которое помогает лучше дышать, и пропеллент, способствующий его доставке в легкие. Нужно хорошенько встряхнуть баллончик перед использованием, чтобы лекарство и пропеллент смешались в нужных пропорциях, иначе одного ингредиента во вдыхаемой смеси получится много, а другого – мало. По статистике, встряхивать ингалятор забывают 43% больных.
Как надо: перед вдохом 10–15 раз основательно потрясти аэрозольный баллончик.
Полный текст этой статьи доступен только для зарегистрированных пользователей.
Далее в статье: какие еще ошибки совершает большинство людей, пользующихся ДАИ и как правильно их избегать? Важная информация о том, как не потерять время, средства и здоровье при терапии аэрозольными ингаляторами.
Пожалуйста, войдите в свой аккаунт.
Еще из Аллергоэфира
Популярные теги
Full Text
В конце 2008 г. в Российской Федерации официально было зарегистрировано около 2 млн пациентов с установленным диагнозом «бронхиальная астма» (БА) и около 1 млн пациентов с диагнозом «хроническая обструктивная болезнь легких» (ХОБЛ). Результаты аптечных продаж (рис. 1) показали, что за 2008 г. было реализовано (продано, выдано по льготе) около 4 млн упаковок ингаляционных препаратов, которые относятся к базисным при лечении обструктивных заболеваний легких (ингаляционные кортикостероиды, длительно действующие b2-агонисты, холинолитики и их комбинации) и более 15,5 млн упаковок так называемых скоропомощных, короткодействующих бронхолитиков (короткодействующие b2-агонисты и холинолитики и их комбинации). Недополучая базисную терапию, пациенты вынуждены принимать «скоропомощные» препараты, причем в среднем каждый пациент с установленным диагнозом расходует за 1 год более 5 упаковок таких препаратов. Несомненно, короткодействующие бронхолитики играют центральную роль в симптоматическом лечении БА и ХОБЛ. Они могут назначаться как по потребности для облегчения симптомов бронхиальной обструкции, так и на регулярной основе для их предупреждения или уменьшения выраженности. В сложившейся ситуации нам важно было проанализировать количество и качество получаемой ситуационной бронхолитической терапии разными лекарственными препаратами и разными системами ингаляционной доставки в условиях реальной клинической практики. В настоящее время отечественный рынок бронходилататоров короткого действия представлен 4 типами ингаляторов: дозированными аэрозольными ингаляторами (ДАИ), ДАИ, активируемыми вдохом (ингаляторы Легкое Дыхание), порошковыми ингаляторами и небулайзерами. Все устройства можно использовать при различной степени тяжести бронхиальной обструкции, однако последним отдается предпочтение в условиях стационаров, при развитии тяжелой, нередко угрожающей жизни бронхиальной обструкции. Эффективность, безопасность и удобство применения конкретного ингалятора зависят как от лекарственного препарата, находящегося в нем, так и от способа доставки этого препарата в нижние дыхательные пути. «Вероятно, в будущем ингаляционные устройства будут намного важнее, чем развитие новых субстанций, поэтому необходима самая эффективная система доставки», – утверждает проф. Питер Барнс, член научного комитета GINA и GOLD, который представляет позицию Национального института сердца и легких Империального колледжа (Лондон). Основные механизмы депозиции лекарственных веществ в респираторной системе следующие: 1) инерционное оседание (рото-глотка, бифуркация трахеи); 2) седиментация (оседание под воздействием тяжести в дыхательных путях среднего калибра); 3) диффузия (броуновское движение мелких частиц аэрозоля в мелких воздухоносных путях и альвеолах). Частицы более 5 мкм оседают в ротоглотке, частицы менее 5 мкм (респирабельная фракция) проникают в дыхательные пути. Из них частицы размером 2–5 мкм оседают в воздухоносных путях. Частицы менее 2 мкм проникают в альвеолы и могут быть удалены с выдыхаемым воздухом. На депозицию лекарственных аэрозолей в легких влияет скорость поступления аэрозоля, его электрический заряд, состояние слизистой оболочки воздухоносных путей (отек, гиперсекреция, спазм). Разные типы ингаляторов предусматривают разные типы активации аэрозоля, находящегося в нем. Так, для эффективного использования обычных ДАИ обязательным требованием является синхронизация вдоха пациента с выбросом лекарственного препарата из ингалятора. Определенная синхронизация вдоха и активации ингалятора требуется и при использовании вместе с ДАИ спейсеров. Автоматическая активация ингалятора за счет вдоха самого пациента в случае использования ДАИ, активируемых вдохом («Легкое Дыхание»), и порошковых ингаляторов устраняет этот недостаток. В то же время каждый тип ингаляторов эффективно работает при разной скорости вдоха (см. таблицу). Наименьшие усилия пациент затрачивает при использовании ДАИ, активируемых вдохом, и небулайзеров. Для решения поставленной задачи были разработаны 3 взаимодополняющих проекта: 1) анкетирование и опрос мнения пациентов, которые использовали разные короткодействующие бронхолитики для ситуационной терапии БА и ХОБЛ в амбулаторных условиях; 2) анкетирование и опрос мнения врачей, которые осуществляли исследование функции внешнего дыхания с проведением бронходилатационной пробы в амбулаторных условиях; 3) скрининг техники ингаляции тремя типами ингаляторов – обычные ДАИ, порошковый ингалятор (Турбухалер) и ингалятор «Легкое Дыхание» – у врачей, занимающихся лечением обструктивных заболеваний легких. Анкетирование и опрос пациентов В анкетировании приняли участие 305 пациентов из 10 городов Российской Федерации, страдающих БА или ХОБЛ, которые использовали регулярно или в режиме «по потребности» разные ингаляционные короткодействующие бронхолитики: сальбутамол в ДАИ (торговые названия Сальбутамол, Асталин, Вентолин), сальбутамол в ингаляторе Легкое Дыхание (торговое название Саламол Эко Легкое Дыхание), фенотерол в ДАИ (торговое название Беротек Н), комбинированный препарат фенотерола и ипратропиума в ДАИ (торговое название Беродуал Н). Нас интересовало, что пациенты ожидают от препаратов для симптоматической терапии, насколько высоко они оценивают эффективность, безопасность, доступность и удобство их использования. Среди опрошенных большинство пациентов (237 человек; 77,8%) отметили, что самое главное – это эффективность препарата («чтобы помогал быстро снять приступ», «чтобы приступ проходил полностью и быстро» и т.п.). Второе место в ряду «ожиданий» занимает доступность ингалятора [отметили 122 (40,0%) пациента: «чтобы всегда был в аптеке», «был недорогой», «чтобы врач выписывал, а в аптеке выдавали без задержки» и т.п.]. На третьем месте было удобство использования ингалятора [108 (35,6%) человек: «чтобы был небольшим и компактным», «чтобы можно было без труда взять с собой», «чтобы можно было незаметно использовать», «чтобы хватало надолго» и т.п.]. Самое последнее, что пациенты ожидали от короткодействующего бронхолитика, – это его безопасность [всего 34 (11,1%) пациента: «чтобы не вызывал сердцебиения», «чтобы не вредил организму» и т.п.], т.е. для большинства опрошенных в короткодействующих бронхолитиках важна эффективность, зачастую в ущерб безопасности препарата (рис. 2). По мнению респондентов, с точки зрения эффективности практически все бронхолитики были оценены одинаково, за исключением Сальбутамола и Асталина (рис. 3). Респонденты отметили только 2 препарата, обладающих наименьшим количеством побочных эффектов, – Беродуал Н и Саламол Эко Легкое Дыхание (рис. 4). Самым простым и удобным в использовании «скоропомощным» бронхолитиком пациенты признали Саламол Эко Легкое Дыхание. Все остальные ингаляторы, которые выпускаются в форме ДАИ, по мнению пациентов, по простоте использования были практически сопоставимы (рис. 5). Подавляющее большинство пациентов руководствовалось при выборе «скоропомощного» бронхолитика рекомендациями пульмонологов/аллергологов (291 человек; 95,4%) и участковых терапевтов (176 человек; 57,7%). Остальные источники получения информации использовались как дополнительные и не играли решающей роли в выборе того или иного препарата. Таким образом, опрос пациентов, пользующихся «скоропомощными» бронхолитиками короткого действия, показал, что наиболее удобным в использовании является ингалятор Саламол Эко Легкое Дыхание. Его эффективность сопоставима с эффективностью других ингаляционных бронхолитиков, при этом он редко вызывает побочные явления. Анкетирование и опрос врачей В программе приняли участие 119 врачей функциональной диагностики из 21 города Российской Федерации. Целью опроса было изучение мнения врачей и пациентов об эффективности и безопасности применения ДАИ и ингаляторов «Легкое Дыхание» при проведении исследования функции внешнего дыхания в амбулаторных условиях. Всего было получено 3054 анкет. После проверки первичного материала, проведенной по критериям полноты заполнения анкет, корректности заполнения, для проведения анализа были отобраны 308 анкет, что составляет 10,1% от исходного массива и соответствует критерию репрезентативности выборки. В пределах выборки большинство врачей отметили, что научить пациентов пользоваться ингаляторами «Легкое Дыхание» было легко (276 ответов, 89,6%), без особых трудностей (31 ответ, 10,1%), и только у 1 (0,3%) пациента возникли сложности при обучении. При этом большинство (259 человек, 84,1%) осуществляли ингаляцию с помощью ингалятора «Легкое Дыхание» правильно даже при отсутствии посторонней помощи, с незначительными ошибками выполнили ингаляцию 48 (15,6%) пациентов, и только 1 (0,3%) пациент выполнил ингаляцию неправильно. В 276 (89,6%) наблюдениях врачи были полностью удовлетворены эффективностью сальбутамола в форме доставки «Легкое Дыхание», в 29 (9,4%) – частично, в 3 (1,0%) случаях – не удовлетворены. У подавляющего большинства (280 человек, 90,9% от общей выборки) пациентов использование сальбутамола в форме доставки «Легкое Дыхание» не вызвало никаких нежелательных явлений. Из 308 пациентов сведения о нежелательных эффектах присутствуют в 28 картах, что составляет 9,1%. Всего зафиксировано 36 нежелательных явлений. В качестве нежелательных явлений упоминаются тахикардия (11 наблюдений, 30,6% от всех нежелательных явлений), тремор рук (19 наблюдений, 52,8%) и повышение артериального давления (6 случаев, 16,7%). Для сравнения приведем результаты Всероссийской программы СВОБОДА, завершившейся в 2007 г., целью которой было изучение правильности выполнения техники ингаляции, эффективности и безопасности бронходилататоров в форме доставки ДАИ и ДАИ, активируемых вдохом («Легкое Дыхание»). В программу были включены результаты обследования 8475 взрослых больных БА и ХОБЛ, которым была показана бронхолитическая терапия короткодействующими b2-агонистами. Было выявлено, что при использовании обычных ДАИ частота возникновения ошибок достигает 75,3%. При этом нежелательные явления при использовании бронхолитиков в ДАИ отмечали 29,6% пациентов. Для анализа предикторов возникновения ошибок в технике ингаляции и нежелательных явлений из выборки были исключены дети и подростки в возрасте до 18 лет. Анализируемая группа включала 274 пациента в возрасте от 18 до 81 года (средний возраст составил 46,6±1,6 года). При анализе частоты возникновения ошибок во время проведения ингаляции выявлено, что возраст является главным предиктором неправильной техники ингаляции. Средний возраст пациентов, которые ингалировали препарат правильно, составил 45,0±0,9 года. В группе пациентов, которые допустили хотя бы одну ошибку при проведении ингаляции, средний возраст составил 53,8±1,6 года (p<0,001). Относительный риск возникновения ошибок в технике ингаляции значимо увеличивается у людей в возрасте старше 50 лет (относительный риск 3,2, доверительный интервал 2,7–4,4; p<0,05). При анализе частоты возникновения нежелательных явлений при назначении сальбутамола в форме доставки «Легкое Дыхание» также выявлено, что возраст является главным предиктором их возникновения. Средний возраст пациентов, у которых возникло хотя бы одно нежелательное явление, составил 52,4±2,2 года. В группе пациентов, у которых нежелательные явления не отмечались, средний возраст составил 46,0±0,8 года (p<0,01). Таким образом, программа подтвердила положительное отношение как врачей, так и пациентов к использованию в реальной клинической практике ингаляционного препарата Саламол Эко Легкое Дыхание, выразившееся в высоких оценках простоты и удобства использования, эффективности и безопасности применения. Скрининг техники ингаляции у врачей С помощью Inhalation Manager (рис. 6) проведено исследование техники ингаляции у врачей, которые занимаются лечением пациентов с обструктивными заболеваниями легких в условиях реальной клинической практики. В этом проекте приняли участие делегаты и участники XVIII Национального конгресса по болезням органов дыхания, состоявшегося в Екатеринбурге 9–12 декабря 2008 г. Во время скрининга было важно объективно оценить ингаляционный маневр при использовании разных ингаляционных устройств, наблюдать за ингаляционным маневром, чтобы оценить качество ингаляции и исследовать следующие параметры: пиковая скорость вдоха (PIF), время до достижения пика скорости вдоха, погрешности в технике маневра (например, выдох в ингаляционное устройство, повторная активация ингалятора во время вдоха), объемные показатели вдоха, продолжительность ингаляции, задержка вдоха в конце ингаляции, размеры ингалируемых частиц. В программе приняли участие 32 врача, среди них 15 пульмонологов, 7 аллергологов, 8 терапевтов и 2 педиатра (возраст от 27 до 71 года). Каждый врач провел серию ингаляционных маневров с последовательным использованием обычного ДАИ, порошкового ингалятора (Турбухалер) и ингалятора «Легкое Дыхание». В случае неудовлетворительной попытки проводилось обучение и повторные ингаляции с использованием того же ингаляционного устройства до достижения оптимальной техники ингаляции. При использовании обычных ДАИ с первой попытки правильно активировали ингалятор 25% врачей, со второй – 50%, с третьей и более – 25% (см. рис. 7). Основные проблемы: • активация ингалятора до начала вдоха (проблемы с синхронизацией вдоха и нажатия на дно баллончика ингалятора) – 74,9%; • повторное нажатие на баллончик во время ингаляции – 8,4%; • не смогли нажать на баллончик – 4,1%; • выдохнули в ингалятор – 4,1%; • объем вдоха после активации ингалятора менее 500 мл – 8,4%. Порошковый ингалятор (Турбухалер) с первой попытки правильно активировали 78,1% врачей, со второй – 15,6%, с третьей – 3,1%, не смогли активировать ингалятор 3,1% (см. рис. 7). Основные проблемы: • невысокая скорость вдоха < 70 л/мин – 95,7%; • выдох в ингалятор – 14,3%. Ингалятор «Легкое Дыхание» с первой попытки правильно активировали 96,9% врачей, со второй – 3,1% (см. рис. 7). Основная проблема: • завершение вдоха сразу же после активации ингалятора. При этом респирабельная фракция при использовании ДАИ составила 11,5–18,6%, при использовании порошкового ингалятора – 3,3–22,1%, а при использовании ингалятора «Легкое Дыхание» – 47,8–56,5% (рис. 8). Итак, несмотря на кажущуюся простоту использования «скоропомощных» ингаляторов, на практике как пациенты, так и сами врачи допускали массу ошибок, что существенно снижало эффективность используемых препаратов и увеличивало число нежелательных явлений от их использования. В результате проведенных программ нами были сделаны следующие выводы. 1. Все короткодействующие бронхолитики достаточно эффективно контролируют клинические симптомы со стороны органов дыхания у больных с обструктивными заболеваниями легких. 2. Применение ДАИ, активируемых вдохом (Саламол Эко Легкое Дыхание), обеспечивает уменьшение числа технических ошибок, делает технику ингаляции более простой и удобной для большинства пациентов по сравнению с обычными ДАИ и дозированными порошковыми ингаляторами 3. Использование бронхолитиков в ДАИ, активируемых вдохом (Саламол Эко Легкое Дыхание), характеризуется меньшей частотой нежелательных эффектов по сравнению с бронхолитиками в обычных ДАИ. Это позволяет рекомендовать Саламол Эко Легкое Дыхание в качестве эффективного и безопасного средства для ситуационной бронхолитической терапии в условиях реальной клинической практики.
Н.Н. МЕЩЕРЯКОВА, к.м.н., ФГУ НИИ пульмонологии ФМБА России
Хроническая обструктивная болезнь легких – заболевание, характеризующееся персистирующим ограничением скорости воздушного потока, имеющее тенденцию к прогрессированию, обусловленную хроническим воспалительным ответом легких на действие патогенных частиц или газов [1]. Хроническая обструктивная болезнь легких является одним из распространенных заболеваний в мире и занимает четвертое место среди причин смертности. Кроме этого, важной характеристикой заболевания является прогрессирующее и инвалидизирующее течение [2, 3].
В настоящее время показано, что ни одно из лекарственных средств, применяемых для лечения ХОБЛ, в долговременной перспективе не позволяет предупредить снижение функции легких, являющееся отличительной чертой болезни. Однако даже незначительное повышение бронхиальной проходимости у больных ХОБЛ во время обострения приводит к снижению сопротивления дыхательных путей, уменьшению дыхательного усилия и гиперинфляции и, как следствие, улучшению клинических симптомов. Поэтому основными препаратами для лечения ХОБЛ являются бронхолитики, применяемые по потребности или на регулярной основе как при обострении, так и во время ремиссии. Среди средств данной группы важное место занимают β2-агонисты, обладающие выраженной бронхоспазмолитической активностью [4].
Бета2-агонисты
Упоминание о применении β2-агонистов – производных эфедры – встречается в источниках, датируемых несколькими тысячелетиями до нашей эры. Ренессанс средств данной группы начался в конце ХIX – начале XX в., когда был открыт адреналин. Эффективное снижение бронхиальной обструкции при применении адреналина сопровождается рядом нежелательных реакций в виде тремора, тахикардии, подъема артериального давления. Несмотря на это, адреналин и сейчас является препаратом выбора неотложной помощи при острых аллергических реакциях.
В 70-х гг. ХХ в. в клиническую практику вошли селективные агонисты β2-рецепторов, которые обладали преимущественным действием на гладкую мускулатуру бронхов при значительном снижении числа нежелательных проявлений. Сальбутамол и тербуталин приобрели статус золотого стандарта среди селективных β2-агонистов. Селективные β2-агонисты обладают быстрым началом действия, оказывают мощное бронхорасширяющее действие, но мало влияют на β1-адренорецепторы, преобладающие в сердечно-сосудистой системе.
Основным принципом действия β2-агонистов является расслабление гладкой мускулатуры бронхов благодаря стимуляции β2-адренергических рецепторов, которые повышают уровень циклических аденозинмонофосфат и вызывают функциональный антагонизм к бронхоконстрикции. Бета2-агонисты устраняют констрикцию гладкой мускулатуры бронхов, кроме того они проявляют противовоспалительный эффект за счет блокировки синтеза лейкотриенов, интерлейкинов и фактора некроза опухоли-α тучными клетками и эозинофилами, препятствуют дегрануляции тучных клеток и эозинофилов, снижают проницаемость кровеносных сосудов, тормозят секрецию слизи, улучшают мукоцилиарный клиренс и подавляют кашлевой рефлекс [5]. Значительно уступая ингаляционным глюкокортикоидам в противовоспалительной активности, β2-агонисты тем не менее дополняют и усиливают их противовоспалительное действие, особенно при совместном назначении.
Хотя терапевтическая активность β2-агонистов связана со стимуляцией β2-адренорецепторов бронхов, превышение дозы может вызвать отрицательные эффекты со стороны других органов и систем, поскольку данные рецепторы представлены и в сердечно-сосудистой системе. Стимуляция β2-рецепторов в сосудах может привести как к тахикардии, так и к снижению диастолического давления. Кроме того, чрезмерное применение β2-агонистов может вызвать метаболические изменения, приводящие к гипокалиемии, удлинению интервала QT на ЭКГ и возможному развитию аритмии. В скелетной мускулатуре также находятся β2- адренорецепторы, и их стимуляция приводит к тремору, а при сахарном диабете необходим контроль за гликемией.
Данные нежелательные эффекты характерны для всех β2-агонистов, как пролонгированных, так и короткодействующих, но они встречаются довольно редко. Однако пациенты с ХОБЛ нередко имеют сопутствующую патологию сердечно-сосудистой системы, скелетной мускулатуры и эндокринной системы, поэтому контроль за интервалом QT на ЭКГ, уровнем калия и глюкозы в сыворотке крови для них весьма важен.
Способ доставки β2-агонистов
Большое значение для уменьшения нежелательных эффектов имеют способы доставки лекарственных препаратов. Оптимальным способом доставки β2-агонистов является ингаляционный, он обеспечивает максимальное попадание лекарства в дыхательные пути и минимальную системную абсорбцию при размере частиц 2–5 мкм. Депозиция аэрозоля в бронхиальном дереве зависит от размера частиц лекарственного препарата, техники и скорости ингаляции.
При назначении ингаляционных препаратов больным с ХОБЛ необходимо уделять внимание обучению техники ингаляций. Выбор ингаляционного устройства зависит от наличия и стоимости устройств, предпочтений врача, навыков и возможностей пациентов. Больные ХОБЛ могут иметь проблемы с координацией движений, и им бывает тяжело использовать обычный простой дозированный аэрозольный ингалятор (ДАИ), из-за чего лекарство не попадает в нижние дыхательные пути и эффективность ингаляции снижается. Существует альтернатива в виде ингалятора, активизируемого вдохом [6].
ДАИ, активизируемый вдохом, для больных ХОБЛ прост в использовании. При его использовании необходимо сделать следующие маневры: для активации ингалятора необходимо только открыть колпачок ингалятора и вдохнуть лекарство, синхронизации вдоха с моментом активации баллончика не требуется (маневр «рука – легкие» отсутствует). Лекарство попадает в бронхиальное дерево при небольшой пиковой объемной скорости вдоха, поэтому его можно успешно применять у пациентов с выраженной обструкцией дыхательных путей, которые не могут осуществить полноценный форсированный вдох. В этом заключено для больных ХОБЛ важное преимущество, особенно при обострении, когда задержка вдоха затруднена и его сила снижена.
Сальбутамол-Тева − это активируемый вдохом ДАИ с пропеллентом гидрофторалканом, содержащий в одной дозе 100 мкг сальбутамола. Гидрофторалкан обеспечивает лекарственному средству определенное преимущество, создавая меньшую скорость струи аэрозоля и более высокую температуру аэрозольного облака, что облегчает проведение ингаляции и не снижает эффективность лекарственного препарата. Устройство Сальбутамол-Тева позволяет использовать ингалятор при обострении, когда ингаляционный поток недостаточен для применения других ингаляционных устройств. При этом существенно увеличивается респирабельная фракция препарата и уменьшается его оседание в полости рта.
Исследование «СВОБОДА»
Эффективность и безопасность Сальбутамола-Тева (Саламол Эко Легкое Дыхание), а также легкость его применения были продемонстрированы в различных исследованиях, в т. ч. в многоцентровом российском исследовании «СВОБОДА». В исследовании участвовало 8 475 взрослых больных бронхиальной астмой и ХОБЛ. Проводилось сопоставление использования обычного ДАИ Сальбутамол и Сальбутамола-Тева. Сравнение ошибок при применении ингаляторов показало, что при использовании обычного ДАИ пациенты допускали в среднем по 2,2 ошибки, а при использовании ДАИ, активизируемого вдохом, количество ошибок снизилось до 0,3 (p < 0,001). При исследовании скорости наступления бронхолитического эффекта у больных, получающих обычный ДАИ, только у 49,2% отмечался эффект менее чем за 5 мин, а у больных, получающих Сальбутамол-Тева, уже у 92,8% пациентов (p < 0,0001). Продолжительность бронхолитического эффекта более 4 ч в группе больных с обычным ДАИ наблюдалась у 45,6%, а у больных с Сальбутамолом-Тева у 86,6 % (p < 0,0001) (рис. 1). После перевода пациентов с бронхолитика ДАИ на Сальбутамол-Тева происходило достоверное уменьшение числа сердечных сокращений с 78,9 до 74,9 в минуту (p < 0,001), величины систолического от 137,2 до 130,6 мм рт. ст. (p < 0,0001) и диастолического с 84,7 до 80,2 мм рт. ст. (p < 0,001) артериального давления (рис. 2). Тремор рук в группе пациентов с обычным ДАИ составлял 29,6%, а у больных с Сальбутамолом-Тева всего 2,8%. Пациенты оценили использование Сальбутамола-Тева как более удобное и легкое в технике использования. Исследование показало, что применение Сальбутамола-Тева эффективно контролирует клиническую симптоматику бронхиальной обструкции как бронхиальной астмы, так и ХОБЛ. Применение ДАИ, активизируемого вдохом, продемонстрировало высокую комплаентность по сравнению с обычным ДАИ. Кроме того, данный ингалятор показал безопасность в применении. Эффективные способы доставки позволяют избежать нежелательных эффектов применения β2-агонистов [7].
При назначении симпатомиметиков обычным режимом для сальбутамола является доза 2,5 мг при помощи небулайзера или при помощи дозированного ингалятора (ДАИ) 400 мкг каждые 4−6 ч. Ответ на ингаляционный симпатомиметик наблюдается обычно в течение 10−15 мин, если же облегчение симптомов отсутствует, то назначают повторные ингаляции. При тяжелом обострении ХОБЛ кратность введения симпатомиметиков может быть значительно увеличена – возможно назначение препаратов каждые 30–60 мин до достижения контроля. Такие большие дозы β2-агонистов при обострении ХОБЛ объясняются повышением клиренса препаратов вследствие значительного увеличения общего метаболизма [8]. Использование ДАИ, активированного вдохом, позволяет избежать передозировки лекарственного препарата и достичь максимального эффекта у больных ХОБЛ.
Заключение
Применение β2-агонистов является необходимой терапий для больных с ХОБЛ. В ее задачи входит создание высоких концентраций лекарственного препарата в дыхательных путях при минимальных системных нежелательных эффектах. Для достижения адекватной бронхолитической и противовоспалительной терапии необходимы эффективные способы доставки лекарственных препаратов, и ингаляторы, активизируемые вдохом, являются именно такими устройствами. Больным с ХОБЛ подобные ингаляторы позволяют избежать ошибок при выполнении процедуры, обеспечить максимальную доставку лекарственных средств в бронхиальное дерево при небольшой объемной скорости вдоха, которая характерна для данного заболевания.
Список литературы
1. Глобальная стратегия диагностики, лечения и профилактики хронической обструктивной болезни легких. Пересмотр 2011 г. М.: Российское респираторное общество, 2012.
2. World Health Report. Geneva: World Health Organization. Availiable from URL: http://www.who.int/whr/2000/en/statistics.htm;2000.
3. Хроническая обструктивная болезнь легких. Клинические рекомендации. Пульмонология. Под ред. Чучалина А.Г. М.: ГЕОТАР-Медиа, 2005:171-222.
4. Fridman M. Changing practices in COPD. A new pharmaqcologic treatment algorithm. Chest, 1995;107,5:194-197.
5. Княжеская Н.П., Белевский А.С. Особенности применения Саламола Эко Легкое Дыхание при хронических обструктивных заболеваниях легких. Пульмонология и аллергология, 2009;3:29-33.
6. Al-Showair RA, Tarsin WY, Assi KH, Pearson SB, Chrystyn H. Can all patients with COPD use the correct inhalation flow with all inhalers and does training help? Respir. Med., 2007;101:2395-401.
7. Шмелев Е.И. Амбулаторное лечение больных бронхиальной астмой и хронической обструктивной болезнью легких (Результаты Всероссийской программы «СВОБОДА»). Сonsilium Medicum, 2007;9:58-63.
8. Siafakas NM, Vermeire P, Pride NB, et al. Optimal assessment and management of chronic obstructive pulmonary disease (COPD). The European Respiratory Society Task Force. Eur. Respir. J., 1995;8:1398-1420.
1. Программа обучения пациентов
• Техника мобилизации мокроты(аутогенный
дренаж)
• Мобилизация грудной клетки
• Тренировка дыхательных мышц
• Обучение и мониторинг техники ингаляции
• Координация вдоха и движений
• Тренинг самопомощи
• Обучение техники кашля
• Анатомия и патофизиология дыхательной
системы
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
2. Ингаляционная терапия
• Ингаляционная терапия начинается с
обучения технике ингаляций
• Требуется регулярное обсуждение
действия и возможных побочных
эффектах терапии
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
3. Цель медикаментозной аэрозольтерапии
• Целенаправленная депозиция (доставка
медикамента в пораженный орган)
• Уменьшение дозы медикамента и
общего воздействия на организм
• Высокая эффективность
терапии(действие медикамента должно
ощущаться)
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
4. Ошибки при использовании ДПИ
• Недостаточная мощность вдоха
• Вдох через нос
• Не делают паузу после вдыхания
медикамента
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
5. Осаждение медикамента при ингаляционном пути
• Реальное кол-во медикамента попадающее в
дыхательные пути в каждодневной клинической
практике не превышает 10-20% и зависит от
многих причин
• 70-90% медикаментов не поступают по
назначению и теряются (осаждение в ротоглотке
и ЖКТ, осаждение на стенках приборов, потери в
окружающую среду
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
6. Ошибки при использовании ДАИ
• 65% пациентов не делают выдох перед
ингаляцией
• 67% пациентов нажимают на дно
баллончика слишком поздно после
начала вдоха
• 70% пациентов неправильно
осуществляют вдох
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
7. Выбор способа доставки аэрозоля в дыхательные пути
Важнейшие аспекты при выборе ингаляционного устройства
Функциональность и эффективность
доставки аэрозольных частиц
Простота использования, размеры
прибора, время ингаляции,
гигиеническое обслуживание прибора,
возможность многократного
использования и стоимость
8. Ошибки при использовании небулайзера
• Форсированное дыхание,
приводящее к гипервентиляции
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
9. Помощь в принятии решений при введении в лечение ингаляционной терапии
• Оценка возможностей для Compliance с
пациентами
• Оценка общей моторики и способность к
координации у пациентов
• Оценка функциональных возможностей грудной
клетки, дыхательных путей и легких.
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
10. Предпосылки для оптимальной депозиции аэрозоля
• Удельный вес респирабельной фракции аэрозоля
• Исправность прибора
• Удовлетворяющая требованиям пациента
ингаляционная система
• Правильная техника ингаляции
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
11. Цели ингаляции:
• Доставка медикамента в дыхательные
пути с помощью различных субстанций«носителей»
• Даже самые эффективные способы
доставки позволяют депонировать в
периферические отделы
респираторного тракта лишь 30%
медикамента
12. Значение сотрудничества с пациентом
• Готовность, умение и также
возможность, выполнять врачебные
рекомендации
• Интеллектуальные способности
• Физические возможности выполнения
ингаляций ( тремор, артроз и др.)
• Положительное эмоциональное
восприятие медикамента и способа
лечения
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
13.
Konrad Lorenz:
Сказано — не означает услышано
Услышано — не означает понято
Понято — не означает согласие
Согласие — не означает действие
Действие — не означает продолжение
(Verhaltensforscher)
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
14. Обучение пациентов
• Часто рекомендуется использование
ингаляционных приборов пациентам без
предварительного инструктажа и обучения
правилам использования устройств
• Регулярный контроль техники ингаляций
пациентом
• Разъяснение действия и возможных побочных
эффектов медикаментов назначенных для
ингаляции , гарантирует успех лечения
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
15. Оценка некоторых критериев при назначении ингаляции
Возраст
Способности координации движений
Частота дыхания
Степень тяжести заболевания
Compliance
Мощность вдоха ( при использовании порошка)
Архитектоника дыхательных путей
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
16. Причины неудовлетворительного сотрудничества с пациентами
• При ингаляционной терапии степень
комплаентности напрямую связана с
количеством ингаляций
• Compliance увеличивается с 19% до 73%,в
случае уменьшения частоты ингаляций с 4-х
до 2-х раз в день
• Отсутствие ощущения достаточной
эффективности лечения
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
17. Препятствия для эффективности ингаляции
Много мокроты
Выраженная обструкция
Непродуктивный кашель
Выраженное вздутие
Неравномерная вентиляция участков легких
( Нарушение архитектоники дыхательных путей)
Важно: Геометрия дыхательных путей
обязательно должна учитываться при выборе
техники ингаляций
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
18. Нарушение проходимости бронхов
Спазм мускулатуры
бронхов
Отек слизистой
бронхов
Вязкая мокрота
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
19. Наиболее частые ошибки (при разных методах ингаляций)
Не убирается крышка ДАИ
Выдох вместо вдоха
Расположение мундштука перед зубами
Слабый вдох(Порошок)
Слишком быстрый вдох (ДАИ)
Вдох через нос
Вдох с открытым ртом
Не делается пауза после вдоха
Рекомендации: Предпочтительно использовать
носовую клемму.
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
20. Средства доставки аэрозоля
Категории ингаляционных приборов:
1. Ультразвуковой небулайзер
2. Компрессорный небулайзер
3. ДАИ с фреоновым распылителем со
спейсером/адаптером или без
4. ДАИ с безфреоновым распылителем с
спейсером/адаптером или без
5. ДПИ
6. Электронный небулайзер
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
21. Схема работы ультразвукового небулайзера
Вдыхаемый
воздух
Air inlet
Aerosol
Аэрозоль
Раствор медикамента
Inhalation
solution
Contact medium
Контактное
средство
(вода)
(water)
Piezo-electric
crystal
Пьезоэлемент
22. Ультразвуковой небулайзер
Преимущества:
1. Бесшумный
2. Не требуется координации дыхания
3. Подходящий спектр частиц
4. Быстрая доставка аэрозоля в дыхательные пути
Недостатки:
Высокая стоимость
Требует технического обслуживания
Не все медикаменты можно распылять
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
23. Небулайзер: депозиция аэрозоля в дыхательных путях в зависимости от размера частиц
Размер частиц:
зависит от параметров компрессора,состояния сопла
небулайзера и состояния трубки-воздуховода
Отделы дыхательных
путей
Размер частиц
Центральные
5-8 мкм
оптимальная депозиция в бронхах,
высокая депозиция в гортани и трахее
Средние
3-5 мкм
Оптимальная депозиция
в альвеолах, средняя в бронхах
Периферические
высокая депозиция в альвеолах,
минимум осаждения в гортани
1-3 мкм
24. Компрессорные небулайзеры
Преимущества :
• Не требуется координация дыхания
• Высокая депозиция в дыхательных путях
• Низкое осаждение медикамента в
ротоглотке
• увлажнение слизистой дыхательных
путей
• Возможность распыления любых
медикаментов
PARI: Возможность сочетания с другими
приборами для физиотерапии
Недостатки :
• Сравнительно дороги
• Недостаточно мобильны
• Шумность
25. Небулайзеры активируемые вдохом
PARI LC PLUS
PARI LL
26. Особенности небулайзеров
• Быстрая доставка лекарства в
дыхательные пути
Тяжелобольные пациенты считают их
наиболее подходящими для быстрого
лечения
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
27. Небулайзер с лицевой маской
Внимательно изучите инструкции по
использованию!
Маски:
• Твердые маски с отверстиями без клапана
• Мягкие маски из силикона без клапана 4
размеров
• Мягкая маска из силикона с клапаном выдоха
! Следует обратить внимание, что маска
должна покрывать нос и рот
28. Программа обучения техники небулайзерной ингаляции
Темы обучения:
1. Подготовка прибора к ингаляции
2. Показать алгоритм проведения ингаляции
3. Знакомство с прерывистой
ингаляцией(прерыватель)
4. Продолжительность ингаляции (Cystische
Fibrose)
5. Демонстрация очистки небулайзера
6. Методы контроля лечения (пф-метрия до и
после ингаляции бронхолитика)
29. Ингаляции у взрослых и детей
-1
-3
-2
4-
-5
1 – маска пластмассовая для взрослых
2 – мундштук с клапаном выдоха
3 – переходник к маске
4 – маска силиконовая детская
5 – смарт маска с клапаном выдоха
30. Ингаляции с маской
• При использовании маски с отверстиями клапан
вдоха небулайзера убирается
• При использовании маски с клапаном выдоха
крышка небулайзера с клапаном вдоха остается
Потери медикаментов при неплотном прилегании
маски к лицу
• Расстояние от маски до лица 1 cм – потери 50%
• Расстояние от маски до лица 2 cм – потери 80%
31.
Небулайзерные ингаляции у детей
PARI JuniorBOY
32.
Сочетание ингаляционной терапии и дыхания с
положительным давлением на выдохе
33. Дозировочный аэрозольный ингалятор
Приборы для тренировки и контроля, которые
позволяют разъяснить правильную технику
ингаляции и успешное осуществление вдыхания
лекарства
• Аэрозольмонитор Bambini (Fa. Vitalograph)
• Тренажер вдоха ( Firma Deal ) Flowcheck для
ингалирования порошков и аэрозолей (Pulver und
Aerosole)
• Разные дыхательные тренажеры
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
34. Дозировочные аэрозольные ингаляторы
Преимущества:
1. Портативность (маленький размер)
2. Мобильность
3. Быстрое применение
Недостатки:
1. Содержат фреон, снимаются с производства
2. Необходимость четкой координации дыхания
3. Осаждение медикамента в ротоглотке
4. Ощущение холода после ингаляции
5. Часто неправильное использование
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
35. ДАИ
ДАИ
со спейсером
ДАИ
без спейсера
Автохалер
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
36. ДАИ
Примечания:
80% наблюдаемых пациентов делают
ошибки при ингаляционной терапии
Наиболее часто это встречается при
использовании ДАИ
Использование спейсера снижает частоту
ошибок в ингаляционной технике
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
37. Правила использования ДАИ
Спокойно выдохнуть
Слегка запрокинуть голову
Медленно начать вдох
С началом вдоха нажать на дно
баллончика
5. Спокойно продолжить вдох,на сколько
это возможно
6. Задержать дыхание до 10 сек.
1.
2.
3.
4.
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
38. Частые ошибки при использовании ДАИ
1. Слишком раннее нажатие на дно
баллончика
2. Мундштук баллончика расположен перед
зубами
3. Слишком позднее нажатие на дно
баллончика
4. Слишком быстрый вдох
5. Слишком медленный вдох
6. Вдох через нос
7. Не сделана пауза после вдыхания
лекарства
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
39. Приспособления, помогающие проведению ингаляции: спейсер
• Спейсер упрощает процедуру ингаляции
• Разные размеры спейсеров
• Разные материалы: пластик или металл
• Пластиковый спейсер =
(электростатическое поле)
• Металлический спейсер
• (Fa.Astra Zeneca, Швеция)
• ( Fa. PARI, Германия)
40. Спейсер
Простота использования
1. Для пациентов имеющих проблемы с
координацией
2. Для маленьких детей и новорожденных
3. Для тяжелобольных пациентов
4. Для пациентов с неврологическими
заболеваниями
5. Обязательное использование спейсера:
при ингаляции кортикостероидов
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
41. Спейсер
Размер спейсера должен теоретически
соответствовать объему вдоха пациента.
Если спейсер слишком большой,
пациент не может сразу вдохнуть весь
объем лекарства, а мелкие и средние
частицы аэрозоля могут оседать на
стенках спейсера
Слишком маленький спейсер должен
немедленно после распыления лекарства
опорожняться (вдох)
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
42. Спейсер: использование у детей
1. При использовании спейсера у грудных
детей с хроническими бронхо-легочными
заболеваниями для получения большего
эффекта следует убрать клапан вдоха.
2. Клапан вдоха спейсера действует у
маленьких детей как дополнительной
сопротивление вдоху, снижая его мощность.
( также у тяжелобольных пациентов)
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
43.
Vermerk unter den
Небухалер с маской
Fotos:
Nur einen Hub zur Zeit
in die Kammer
Волюматик
С мягкой маской
Оптичамбер
44. Спейсеры, имеющие большой объем «мертвого пространства».
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
Клапан вдоха
Вход для
присоединения ДАИ
Мундштук
Корпус
Клапан выдоха
ДАИ
Вход для
присоединения ДАИ
Клапан выдоха
корпус
Клапан вдоха
Маска
45. Сравнение использования спейсера в детском возрасте
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
Spacer/Firma
Спейсер/производитель
Form
Форма
Поток клапан
Volumen
Ventil
Мл
вд/выд
ml
in/ex
Nebulator®
Birne
750
A
s
A
e
T
y
a
i
t
h
s
a
S
a
l
o
—
r
B
h
x
t
s
c
e
b
l
A
d
a
n
a
o
u
G
A
r
r
r
B
a
t
m
l
M
a
l
a
A
b
e
e
U
t
c
w
e
d
r
h
r
i
e
d
e
a
l
C
Падение
DruckabfallМертвое
Totraum
Давления пространство
Pa
ml
inaktiviert ―
―
―
n
®
c
поток
Fluss
л/мин
l/min
a
n
a
d
Z
y
l
i
n
d
e
r
1
4
5
i
n
Z
y
l
i
n
d
e
r
3
5
0
i
n
/
e
B
i
2
5
0
i
n
/
e
1
5
2
5
x
1
5
1
0
x
1
5
1
0
—
3
―
0
a
®
4
K
t
B
i
s
c
S
h
e
c
h
r
w
S
t
e
d
a
h
e
l
n
s
p
a
c
e
r
r
n
e
0
—
1
2
5
―
0
46. Гигиена и профилактика электризации стенок
1. Каждые 2-3 недели необходимо
чистить, мыть и сушить при комнатной
температуре (не вытирать)
2. В новый спейсер перед первым
использованием,необходимо
2-3 раза впрыснуть лекарство из
баллончика, аэрозоль оседает на
стенках, не вдыхать !
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
47. Порошковые ингаляции
Преимущества:
• Портативность
• Мобильность
• Многократное использование (Не для всех типов )
Недостатки:
• Провоцируют кашель при гиперреактивности бронхов
• Требуют высокой мощности вдоха
• Не все медикаменты можно распылять
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
48. Порошковые ингаляторы
Применение:
Спокойно и полностью выдохнуть
Обхватить мундштук губами
Слегка запрокинуть голову
Быстро и глубоко вдохнуть(возможно
использовать назальную клемму)
5. Задержать дыхание на 10 сек.
1.
2.
3.
4.
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
49. Порошковые ингаляции
Преимущества:
1. Простота использования
2. Хороший комплаенс
Недостатки:
1. Склеивание порошка при повышенной
влажности.
2. Мокрые капсулы невозможно открывать
3. Затупление перфоратора
4. При сильной бронхообструкции и уменьшении
просвета дыхательных путей, частицы порошка
могут не попадать в периферические отделы
дыхательных путей
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
50. Порошковые ингаляторы
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
Турбохалер
Изихалер
Дискхалер
51.
52. Заключение
1. Терапевт и пациент
(родители/родственники) должны
обучиться правильной технике
ингаляций с последующим контролем.
2. Необходим индивидуальный подход при
подборе ингаляционных систем
3. Необходимо постоянное обслуживание и
очистка ингаляционных приборов
4. Постоянный контроль эффективности
ингаляционной терапии. (исследование
ФВД /Пикфлоуметрия)
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
53.
+49-4682-34132
ИНГАЛЯЦИОННАЯ ТЕРАПИЯ
Показания для ингаляционной терапии: 1. 2. 3. 4. 5. ОРВИ (ринит, фарингит, ларингит, трахеит) и их осложнения (риносинусит, ларинготрахеит). Обострение хронического ринита, хронического синусита, хронического тонзиллита. Бронхиальная астма. Пневмонии в период разрешения. Острый и обострение хронического бронхита. Бронхоэктатическая болезнь лёгких. 7. Грибковые поражения верхних и нижних дыхательных путей. 8. Туберкулёз лёгких и бронхов. 9. Муковисцидоз. 10. Для профилактики послеоперационных осложнений. 11. ВИЧ – инфекция (стадия респираторных расстройств). 6.
Преимущества ингаляционной терапии: l l l Доставка препарата происходит именно в пораженный орган (дыхательные пути) Доставляемая доза препарата меньше, а следовательно уменьшается риск системных побочных эффектов Действие лекарства наступает быстрее
Виды ингаляционных средств доставки Лекарственные формы Порошковые ЛС: ДПИ (дозирующие порошковые ингаляторы) Жидкие ЛС: ДАИ (дозирующие порошковые ингаляторы) Небулайзеры
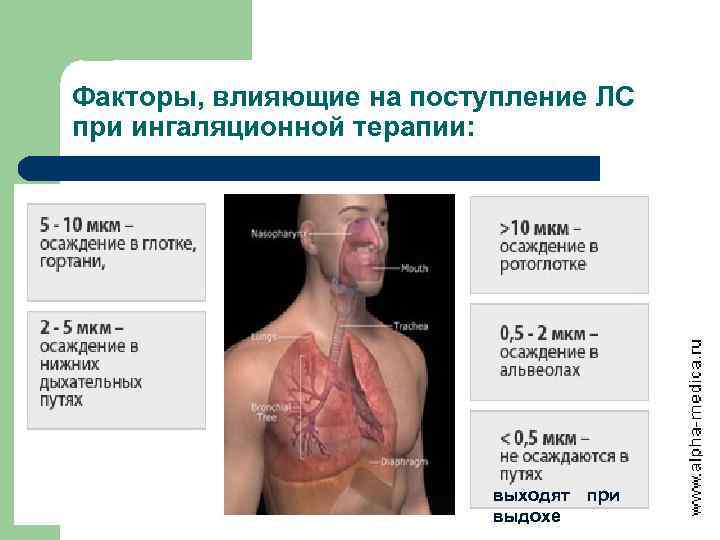
Факторы, влияющие на поступление ЛС при ингаляционной терапии: выходят при выдохе
СПОСОБЫ ПРИМЕНЕНИЯ ИНГАЛЯЦИОННЫХ ПРЕПАРАТОВ Дозированный аэрозольный ингалятор (ДАИ) ДАИ со спейсером
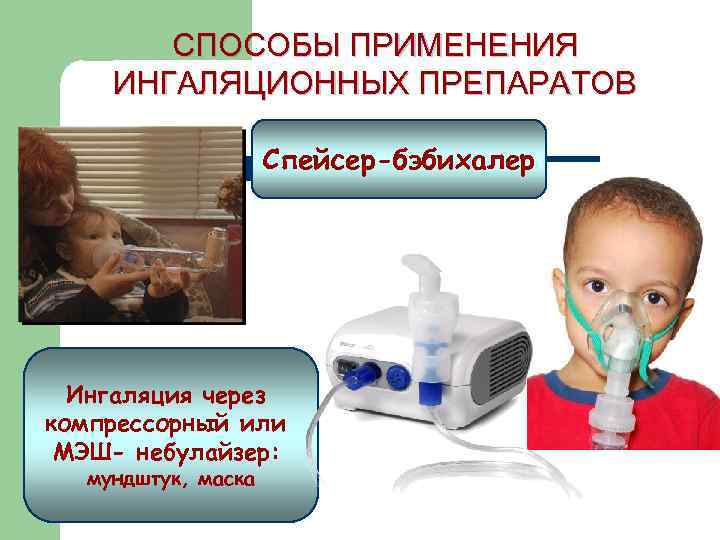
СПОСОБЫ ПРИМЕНЕНИЯ ИНГАЛЯЦИОННЫХ ПРЕПАРАТОВ Спейсер-бэбихалер Ингаляция через компрессорный или МЭШ- небулайзер: мундштук, маска
СПОСОБЫ ПРИМЕНЕНИЯ ИНГАЛЯЦИОННЫХ ПРЕПАРАТОВ (ДПИ) Мультидиск Аэролайзер Турбухалер
У 30% взрослых и 70 -90% детей отмечаются трудности в использовании дозирующих ингаляторов, особенно дети раннего возраста.
ПРИМЕРНАЯ СХЕМА ВЫБОРА СПОСОБА ДОСТАВКИ ЛЕКАРСТВА В ЗАВИСИМОСТИ ОТ ВОЗРАСТА Возраст Оптимальные способы доставки Дети 0 — 2 лет Небулайзер; Дозированный аэрозоль с лицевой маской (бэбихалер, аэрочэмбер). Дети 3 — 5 лет Дозированный аэрозоль со спейсером; Небулайзер. Дети 5 — 15 лет Порошковые ингаляторы; Дозированный аэрозоль со спейсером; Дозированный аэрозоль «Легкое дыхание» . Взрослые Порошковые ингаляторы; Дозированный аэрозоль со спейсером; Дозированный аэрозоль «Легкое дыхание» . Пожилые люди Порошковые ингаляторы; Дозированный аэрозоль со спейсером; Дозированный аэрозоль «Легкое дыхание» .
ПРАВИЛЬНОЕ ИСПОЛЬЗОВАНИЕ ДАИ l Все дозирующие ингаляторы снабжены инструкциями, которым вы должны обязательно следовать.
ПРАВИЛЬНОЕ ИСПОЛЬЗОВАНИЕ ДАИ 1. 2. 3. 4. 5. 6. Спокойно выдохнуть. Слегка запрокинуть голову. Медленно начать вдох. С началом вдоха нажать на дно баллончика. Спокойно продолжить вдох, насколько это возможно. Задержать дыхание на 10 секунд
Частые ошибки при использовании ДАИ: l l l Слишком раннее нажатие на дно баллончика. Мундштук баллончика расположен перед зубами. Слишком позднее нажатие на дно баллончика. Слишком быстрый/медленный вдох Вдох через нос. Не сделана пауза после вдыхания препарата
Спейсеры l Специальная клапанная камера для оптимизации использования ДАИ, существенно упрощает процедуру ингаляции с ДАИ. НЕТ НЕОБХОДИМОСТИ СИНХРОНИЗИРОВАТЬ ВДОХ С НАЖАТИЕМ!
ДОЗИРУЮЩИЕ ПОРОШКОВЫЕ ИНГАЛЯТОРЫ • • не содержат пропеллентов, вредных для окружающей среды «работают» на активном вдохе, т. е. препарат попадает к вам в легкие, только когда вы совершаете вдох. Воздушный поток во время вдоха увлекает за собой ингаляционную дозу препарата в виде пудры, и нажимать ни на что не нужно!
ПРИМЕНЕНИЕ ДПИ: 1. 2. 3. 4. 5. Спокойно и полностью выдохнуть. Обхватить мундштук губами. Слегка запрокинуть голову Быстро и глубоко вдохнуть. Задержать дыхание на 10 сек.
Ошибки при использовании ДПИ: l l l Недостаточная мощность вдоха. Вдох через нос. Не делается пауз после вдыхания медикамента
Недостатки ДПИ: l l Склеивание порошка при повышенной влажности Мокрые капсулы невозможно открывать Затупление перфоратора При сильной бронхообструкции частицы порошка могут не попадать в периферические отделы дыхательных путей
ИНГАЛЯТОР СУХОЙ ПУДРЫ ТУРБУХАЛЕР l l Турбухалер очень прост в использовании и в отличие от аэрозолей не требует координации вдоха с нажатием на баллончик. Уникальное дозирующее устройство очень точно отмеряет дозу препарата, и пациент может быть уверен, что вдыхает именно предписанное ему количество лекарства.
ИНГАЛЯТОР СУХОЙ ПУДРЫ ТУРБУХАЛЕР
ДИСКУС ИЛИ МУЛЬТИДИСК l l l Последнее поколение порошковых ингаляторов Компактный Хватает на длительный срок Хорошо защищен от всевозможных воздействий Очень низкое сопротивление на вдохе, что позволяет применять дискус у маленьких детей
ИСПОЛЬЗОВАНИЕ НЕБУЛАЙЗЕРА l l Небулайзеры эффективно доставляют противоастматические препараты в виде мелкого тумана через мундштуки, маски различного размера (детские и взрослые). Использование распыляемых при помощи небулайзера противоастматических препаратов особенно полезно у младенцев, детей младшего возраста и некоторых пожилых пациентов, которые не в состоянии применять ДАИ. Напоминаем о необходимости получить надлежащую инструкцию по использованию вашего небулайзера (уточнить тип небулайзера и растворы, которые можно использовать). .
Ошибки при использовании небулайзера l Форсированное дыхание, приводящее в итоге к гипервентиляции
Как можно контролировать эффективность ингаляционной терапии? ? ? l l l По субъективному ощущению ребенка (облегчение дыхания, уменьшение одышки, отхождение мокроты и т. д. ) По динамике физикальных данных По результатам ФВД в динамике
Наиболее частые ошибки при использовании дозированного ингалятора:
1. Более одной (обычно две) ингаляции за один вдох.
2. Не задерживается дыхание на вдохе.
3. Не запрокидывается голова кверху перед ингаляцией. Если голова в обычном положении, то при проведении ингаляции большое количество препарата остается на задней стенке глотки и не попадает в легкие.
Техника безопасности при применении ингалятора.
а) перед первым использованием ингалятора или в том случае, если ингалятором не пользовались неделю и дольше, следует удалить колпачок с мундштука, слегка сдавив колпачок с боков, хорошо встряхнуть ингалятор и нажать на клапан аэрозоля для высвобождения одной ингаляционной дозы в воздух, чтобы убедиться в исправности ингалятора;
б) ингалятор необходимо чистить не реже 1 раза в неделю:
1. Извлечь металлический баллончик из пластмассового корпуса и снять крышку мундштука.
2. Тщательно промыть пластмассовый корпус и крышку мундштука под струей теплой воды.
3. Просушить пластмассовый корпус и крышку мундштука полностью как снаружи, так и внутри. Не допускать перегрева.
4. Поместить металлический баллончик в пластмассовый корпус и надеть крышку мундштука.
Не погружать металлический баллончик в воду!
Применение дозированного ингалятора в нос
Цель: лечебный процесс.
Показания: назначение врача (воспалительный процесс носоглотки).
Противопоказания: индивидуальная непереносимость лекарственного средства.
Оснащение: ингаляционный баллончик.
Последовательность действий:
- Вымыть и осушить руки.
- Встряхнуть препарат.
- Снять с баллончика защитный колпачок.
- Слегка запрокинуть голову и склонить к левому плечу.
- Прижать пальцем левое крыло носа к носовой перегородке.
- Сделать глубокий выдох через рот.
- Ввести наконечник ингалятора в правый носовой ход, Сделать глубокий вдох через нос и одновременно нажать на дно баллончика.
- Извлечь наконечник ингалятора. Прижать правое крыло носа к носовой перегородке и задержать дыхание на 5-10 секунд.
- Произвести спокойный выдох через рот.
- Повторить те же действия в левый носовой ход.
- Вымыть и осушить руки.
Раздача лекарственных препаратов для энтерального применения.
Цель: обеспечение пациента своевременным лечением.
Показания: назначение врача.
Противопоказания: индивидуальная непереносимость лекарственного препарата. Неэффективность при оказании неотложной помощи.
Оснащение: журнал назначений, лекарственные препараты, передвижной столик, мензурки, графин с питьевой водой, ножницы.
Алгоритм манипуляции
| Последовательность действий | Обоснование |
|
Эффективность выполнения манипуляции. |
|
Инфекционная безопасность. |
|
Обеспечение правильного выполнения назначений. |
|
Соблюдение принципа безопасного и эффективного лечения. |
Примечание. Предоставить пациенту необходимую информацию: название препарата, цель приёма лекарства, как, когда и как долго принимать препарат, имеет ли значение пропуск приёма и как в этом случае поступить, как распознать побочные эффекты, взаимодействие лекарства с другими лекарствами, пищей и алкоголем. |
Создание максимального комфорта пациенту.
Право пациента на информацию. |
|
Эффективность выполнения манипуляции. |
|
|
|
Инфекционная безопасность. |
|
Инфекционная безопасность. |
|
Контроль выполнения манипуляции. |
Данный алгоритм обеспечивает следующие преимущества:
- контроль приема медикаментов пациентом;
- исключение ошибок при раздаче лекарственных средств;
- достоверную информацию пациенту о назначенном ему лекарственном
средстве.
В некоторых лечебных отделениях с целью экономии времени медсестры раскладывают лекарственные средства заранее на одни сутки в специальные лотки, разделенные на ячейки. В каждой ячейке указаны Ф.И.О. пациента и номер палаты. Медсестра разносит лекарственные средства пациентам по палатам, контролируя их прием.
Применение суппозитория
Цель: лечебный процесс.
Показания: при невозможности и нецелесообразности перорального введения препаратов (при рвоте, нарушении глотания, поражении слизистой оболочки желудка, бессознательном состоянии пациента); при необходимости местного действия препарата. Назначение врача.
Противопоказания: кровотечение из прямой кишки.
Оснащение: перчатки, суппозитории (свечи), ножницы, салфетки, лоток, ширма, ёмкость с дезраствором.
Алгоритм манипуляции
| Последовательность действий | Обоснование |
|
Эффективность выполнения манипуляции. |
|
Право пациента на информацию. |
|
Эмоциональная безопасность пациента. |
|
Эффективность выполнения манипуляции. |
|
Инфекционная безопасность. |
|
Эффективность выполнения манипуляции. |
|
|
|
|
|
Инфекционная безопасность. |
|
Создание максимального комфорта пациенту. Эффективность выполнения манипуляции. |
|
|
|
Инфекционная безопасность. |
|
Контроль выполнения манипуляции. |
Примечание: 1) суппозитории становятся жидкими при температуре тела, поэтому вскрывать их необходимо непосредственно перед введением;
2) перед введением суппозиторий общего воздействия на организм необходимо опорожнить кишечник или сделать очистительную клизму.
Применение мази
Цель: лечебный процесс.
Показания: назначение врача.
Противопоказания: индивидуальная непереносимость лекарственного средства.
Оснащение: перчатки, мазь, стерильный аппликатор, ножницы, бинт или лейкопластырь, вода (37-38оС), раствор антисептика для обработки кожи (по необходимости), лоток, ширма, ёмкость с дез. раствором, стерильные: салфетки, шпатель, перевязочный материал, перчатки.
Последовательность действий:
- Втирание мази в кожу
- Внимательно изучить инструкцию по применению мази. Приготовить всё необходимое для выполнения манипуляции.
- Сообщить пациенту информацию о ходе манипуляции и о лекарственном средстве. Получить согласие пациента.
- Отгородить пациента ширмой. Помочь пациенту занять удобное положение.
- Обработать руки, надеть перчатки.
- Осмотреть участок кожи для применения мази.
- Обработать и высушить кожу салфеткой или полотенцем.
- Нанести мазь из тюбика на аппликатор; при его отсутствии втирать мазь только в перчатках.
Не втирайте мазь пациенту незащищёнными руками – это небезопасно для Вашего здоровья!
- Втирать мазь лёгкими вращательными движениями 3-4 минуты до полного всасывания, в некоторых случаях имеются точные инструкции о том, когда следует прекратить втирание (обеспечить тепло, если указанно в инструкции по применения мази).
- Аппликатор в лоток для отработанного материала.
- Снять перчатки и сбросить в лоток для отработанного материала.
- Обеспечить пациенту комфортные условия.
- Надеть перчатки, провести дезинфекцию отработанного материала. После снять перчатки, обработать руки.
- Сделать отметку о выполнении назначения.
- Нанесение мази на кожу
- Внимательно изучить инструкцию по применению мази. Приготовить всё необходимое для выполнения манипуляции.
- Сообщить пациенту информацию о ходе манипуляции и о лекарственном средстве. Получить согласие пациента.
- При необходимости отгородить пациента ширмой. Помочь пациенту занять удобное положение.
- Обработать руки, надеть перчатки.
- Осмотреть участок кожи для применения мази.
- Выдавить из тюбика на аппликатор нужное количество мази.
- Нанести тонкий слой мази на кожу и оставить кожу открытой в течение 10-15 минут до полного всасывания.
- Снять перчатки, сбросить в ёмкость для отработанного материала.
- Обработать руки.
- Через 10-15 мин. осмотреть кожу, убедиться, что мазь впиталась.
- Сделать отметку в документации о выполнении назначения.
III. Наложение мазевой повязки.
- Внимательно изучить инструкцию по применению мази. Приготовить всё необходимое для выполнения манипуляции.
- Сообщить пациенту информацию о ходе манипуляции и о лекарственном средстве. Получить согласие пациента.
- При необходимости отгородить пациента ширмой. Помочь пациенту занять удобное положение.
- Обработать руки, надеть перчатки.
- Осмотреть участок кожи или раны для применения мази.
- Обработать и высушить кожу стерильной салфеткой.
- С помощью стерильного шпателя нанести необходимое количество мази на стерильную салфетку.
- По показаниям наложить салфетку с мазью на поражённый участок (на салфетку с сильнопахнущей или пачкающей одежду мазью можно положить сверху небольшой слой ваты). Зафиксировать бинтом (марлевым или трубчатым).
- Спросить пациента, не испытывает ли он дискомфорт в связи с наложенной повязкой.
- Снять перчатки и сбросить в лоток для отработанного материала.
- Обеспечить пациенту комфортные условия.
- Надеть перчатки, провести дезинфекцию отработанного материала. После снять перчатки, обработать руки.
- Сделать отметку о выполнении назначения.
Введение мази в нос
Цель: лечебный процесс (обеспечить носовое дыхание, противовоспалительная терапия, иммуностимуляция).
Показания: назначение врача.
Противопоказания: индивидуальная непереносимость лекарственного средства.
Оснащение: стерильные ватные турунды, флакон или тюбик с мазью, стерильная стеклянная лопаточка, перчатки, ёмкость для отработанного материала.
Алгоритм манипуляции
| Последовательность действий | Обоснование |
|
Эффективность выполнения манипуляции. |
|
Право пациента на информацию. |
|
Эффективность выполнения манипуляции. |
|
|
|
Инфекционная безопасность. |
|
Эффективность выполнения манипуляции. |
|
Обеспечение правильного выполнения назначений |
|
|
|
Инфекционная безопасность. |
|
|
|
Контроль выполнения манипуляции. |
1. Программа обучения пациентов
• Техника мобилизации мокроты(аутогенный
дренаж)
• Мобилизация грудной клетки
• Тренировка дыхательных мышц
• Обучение и мониторинг техники ингаляции
• Координация вдоха и движений
• Тренинг самопомощи
• Обучение техники кашля
• Анатомия и патофизиология дыхательной
системы
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
2. Ингаляционная терапия
• Ингаляционная терапия начинается с
обучения технике ингаляций
• Требуется регулярное обсуждение
действия и возможных побочных
эффектах терапии
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
3. Цель медикаментозной аэрозольтерапии
• Целенаправленная депозиция (доставка
медикамента в пораженный орган)
• Уменьшение дозы медикамента и
общего воздействия на организм
• Высокая эффективность
терапии(действие медикамента должно
ощущаться)
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
4. Ошибки при использовании ДПИ
• Недостаточная мощность вдоха
• Вдох через нос
• Не делают паузу после вдыхания
медикамента
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
5. Осаждение медикамента при ингаляционном пути
• Реальное кол-во медикамента попадающее в
дыхательные пути в каждодневной клинической
практике не превышает 10-20% и зависит от
многих причин
• 70-90% медикаментов не поступают по
назначению и теряются (осаждение в ротоглотке
и ЖКТ, осаждение на стенках приборов, потери в
окружающую среду
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
6. Ошибки при использовании ДАИ
• 65% пациентов не делают выдох перед
ингаляцией
• 67% пациентов нажимают на дно
баллончика слишком поздно после
начала вдоха
• 70% пациентов неправильно
осуществляют вдох
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
7. Выбор способа доставки аэрозоля в дыхательные пути
Важнейшие аспекты при выборе ингаляционного устройства
Функциональность и эффективность
доставки аэрозольных частиц
Простота использования, размеры
прибора, время ингаляции,
гигиеническое обслуживание прибора,
возможность многократного
использования и стоимость
8. Ошибки при использовании небулайзера
• Форсированное дыхание,
приводящее к гипервентиляции
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
9. Помощь в принятии решений при введении в лечение ингаляционной терапии
• Оценка возможностей для Compliance с
пациентами
• Оценка общей моторики и способность к
координации у пациентов
• Оценка функциональных возможностей грудной
клетки, дыхательных путей и легких.
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
10. Предпосылки для оптимальной депозиции аэрозоля
• Удельный вес респирабельной фракции аэрозоля
• Исправность прибора
• Удовлетворяющая требованиям пациента
ингаляционная система
• Правильная техника ингаляции
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
11. Цели ингаляции:
• Доставка медикамента в дыхательные
пути с помощью различных субстанций«носителей»
• Даже самые эффективные способы
доставки позволяют депонировать в
периферические отделы
респираторного тракта лишь 30%
медикамента
12. Значение сотрудничества с пациентом
• Готовность, умение и также
возможность, выполнять врачебные
рекомендации
• Интеллектуальные способности
• Физические возможности выполнения
ингаляций ( тремор, артроз и др.)
• Положительное эмоциональное
восприятие медикамента и способа
лечения
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
13.
Konrad Lorenz:
Сказано — не означает услышано
Услышано — не означает понято
Понято — не означает согласие
Согласие — не означает действие
Действие — не означает продолжение
(Verhaltensforscher)
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
14. Обучение пациентов
• Часто рекомендуется использование
ингаляционных приборов пациентам без
предварительного инструктажа и обучения
правилам использования устройств
• Регулярный контроль техники ингаляций
пациентом
• Разъяснение действия и возможных побочных
эффектов медикаментов назначенных для
ингаляции , гарантирует успех лечения
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
15. Оценка некоторых критериев при назначении ингаляции
Возраст
Способности координации движений
Частота дыхания
Степень тяжести заболевания
Compliance
Мощность вдоха ( при использовании порошка)
Архитектоника дыхательных путей
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
16. Причины неудовлетворительного сотрудничества с пациентами
• При ингаляционной терапии степень
комплаентности напрямую связана с
количеством ингаляций
• Compliance увеличивается с 19% до 73%,в
случае уменьшения частоты ингаляций с 4-х
до 2-х раз в день
• Отсутствие ощущения достаточной
эффективности лечения
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
17. Препятствия для эффективности ингаляции
Много мокроты
Выраженная обструкция
Непродуктивный кашель
Выраженное вздутие
Неравномерная вентиляция участков легких
( Нарушение архитектоники дыхательных путей)
Важно: Геометрия дыхательных путей
обязательно должна учитываться при выборе
техники ингаляций
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
18. Нарушение проходимости бронхов
Спазм мускулатуры
бронхов
Отек слизистой
бронхов
Вязкая мокрота
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
19. Наиболее частые ошибки (при разных методах ингаляций)
Не убирается крышка ДАИ
Выдох вместо вдоха
Расположение мундштука перед зубами
Слабый вдох(Порошок)
Слишком быстрый вдох (ДАИ)
Вдох через нос
Вдох с открытым ртом
Не делается пауза после вдоха
Рекомендации: Предпочтительно использовать
носовую клемму.
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
20. Средства доставки аэрозоля
Категории ингаляционных приборов:
1. Ультразвуковой небулайзер
2. Компрессорный небулайзер
3. ДАИ с фреоновым распылителем со
спейсером/адаптером или без
4. ДАИ с безфреоновым распылителем с
спейсером/адаптером или без
5. ДПИ
6. Электронный небулайзер
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
21. Схема работы ультразвукового небулайзера
Вдыхаемый
воздух
Air inlet
Aerosol
Аэрозоль
Раствор медикамента
Inhalation
solution
Contact medium
Контактное
средство
(вода)
(water)
Piezo-electric
crystal
Пьезоэлемент
22. Ультразвуковой небулайзер
Преимущества:
1. Бесшумный
2. Не требуется координации дыхания
3. Подходящий спектр частиц
4. Быстрая доставка аэрозоля в дыхательные пути
Недостатки:
Высокая стоимость
Требует технического обслуживания
Не все медикаменты можно распылять
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
23. Небулайзер: депозиция аэрозоля в дыхательных путях в зависимости от размера частиц
Размер частиц:
зависит от параметров компрессора,состояния сопла
небулайзера и состояния трубки-воздуховода
Отделы дыхательных
путей
Размер частиц
Центральные
5-8 мкм
оптимальная депозиция в бронхах,
высокая депозиция в гортани и трахее
Средние
3-5 мкм
Оптимальная депозиция
в альвеолах, средняя в бронхах
Периферические
высокая депозиция в альвеолах,
минимум осаждения в гортани
1-3 мкм
24. Компрессорные небулайзеры
Преимущества :
• Не требуется координация дыхания
• Высокая депозиция в дыхательных путях
• Низкое осаждение медикамента в
ротоглотке
• увлажнение слизистой дыхательных
путей
• Возможность распыления любых
медикаментов
PARI: Возможность сочетания с другими
приборами для физиотерапии
Недостатки :
• Сравнительно дороги
• Недостаточно мобильны
• Шумность
25. Небулайзеры активируемые вдохом
PARI LC PLUS
PARI LL
26. Особенности небулайзеров
• Быстрая доставка лекарства в
дыхательные пути
Тяжелобольные пациенты считают их
наиболее подходящими для быстрого
лечения
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
27. Небулайзер с лицевой маской
Внимательно изучите инструкции по
использованию!
Маски:
• Твердые маски с отверстиями без клапана
• Мягкие маски из силикона без клапана 4
размеров
• Мягкая маска из силикона с клапаном выдоха
! Следует обратить внимание, что маска
должна покрывать нос и рот
28. Программа обучения техники небулайзерной ингаляции
Темы обучения:
1. Подготовка прибора к ингаляции
2. Показать алгоритм проведения ингаляции
3. Знакомство с прерывистой
ингаляцией(прерыватель)
4. Продолжительность ингаляции (Cystische
Fibrose)
5. Демонстрация очистки небулайзера
6. Методы контроля лечения (пф-метрия до и
после ингаляции бронхолитика)
29. Ингаляции у взрослых и детей
-1
-3
-2
4-
-5
1 – маска пластмассовая для взрослых
2 – мундштук с клапаном выдоха
3 – переходник к маске
4 – маска силиконовая детская
5 – смарт маска с клапаном выдоха
30. Ингаляции с маской
• При использовании маски с отверстиями клапан
вдоха небулайзера убирается
• При использовании маски с клапаном выдоха
крышка небулайзера с клапаном вдоха остается
Потери медикаментов при неплотном прилегании
маски к лицу
• Расстояние от маски до лица 1 cм – потери 50%
• Расстояние от маски до лица 2 cм – потери 80%
31.
Небулайзерные ингаляции у детей
PARI JuniorBOY
32.
Сочетание ингаляционной терапии и дыхания с
положительным давлением на выдохе
33. Дозировочный аэрозольный ингалятор
Приборы для тренировки и контроля, которые
позволяют разъяснить правильную технику
ингаляции и успешное осуществление вдыхания
лекарства
• Аэрозольмонитор Bambini (Fa. Vitalograph)
• Тренажер вдоха ( Firma Deal ) Flowcheck для
ингалирования порошков и аэрозолей (Pulver und
Aerosole)
• Разные дыхательные тренажеры
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
34. Дозировочные аэрозольные ингаляторы
Преимущества:
1. Портативность (маленький размер)
2. Мобильность
3. Быстрое применение
Недостатки:
1. Содержат фреон, снимаются с производства
2. Необходимость четкой координации дыхания
3. Осаждение медикамента в ротоглотке
4. Ощущение холода после ингаляции
5. Часто неправильное использование
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
35. ДАИ
ДАИ
со спейсером
ДАИ
без спейсера
Автохалер
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
36. ДАИ
Примечания:
80% наблюдаемых пациентов делают
ошибки при ингаляционной терапии
Наиболее часто это встречается при
использовании ДАИ
Использование спейсера снижает частоту
ошибок в ингаляционной технике
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
37. Правила использования ДАИ
Спокойно выдохнуть
Слегка запрокинуть голову
Медленно начать вдох
С началом вдоха нажать на дно
баллончика
5. Спокойно продолжить вдох,на сколько
это возможно
6. Задержать дыхание до 10 сек.
1.
2.
3.
4.
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
38. Частые ошибки при использовании ДАИ
1. Слишком раннее нажатие на дно
баллончика
2. Мундштук баллончика расположен перед
зубами
3. Слишком позднее нажатие на дно
баллончика
4. Слишком быстрый вдох
5. Слишком медленный вдох
6. Вдох через нос
7. Не сделана пауза после вдыхания
лекарства
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
39. Приспособления, помогающие проведению ингаляции: спейсер
• Спейсер упрощает процедуру ингаляции
• Разные размеры спейсеров
• Разные материалы: пластик или металл
• Пластиковый спейсер =
(электростатическое поле)
• Металлический спейсер
• (Fa.Astra Zeneca, Швеция)
• ( Fa. PARI, Германия)
40. Спейсер
Простота использования
1. Для пациентов имеющих проблемы с
координацией
2. Для маленьких детей и новорожденных
3. Для тяжелобольных пациентов
4. Для пациентов с неврологическими
заболеваниями
5. Обязательное использование спейсера:
при ингаляции кортикостероидов
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
41. Спейсер
Размер спейсера должен теоретически
соответствовать объему вдоха пациента.
Если спейсер слишком большой,
пациент не может сразу вдохнуть весь
объем лекарства, а мелкие и средние
частицы аэрозоля могут оседать на
стенках спейсера
Слишком маленький спейсер должен
немедленно после распыления лекарства
опорожняться (вдох)
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
42. Спейсер: использование у детей
1. При использовании спейсера у грудных
детей с хроническими бронхо-легочными
заболеваниями для получения большего
эффекта следует убрать клапан вдоха.
2. Клапан вдоха спейсера действует у
маленьких детей как дополнительной
сопротивление вдоху, снижая его мощность.
( также у тяжелобольных пациентов)
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
43.
Vermerk unter den
Небухалер с маской
Fotos:
Nur einen Hub zur Zeit
in die Kammer
Волюматик
С мягкой маской
Оптичамбер
44. Спейсеры, имеющие большой объем «мертвого пространства».
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
Клапан вдоха
Вход для
присоединения ДАИ
Мундштук
Корпус
Клапан выдоха
ДАИ
Вход для
присоединения ДАИ
Клапан выдоха
корпус
Клапан вдоха
Маска
45. Сравнение использования спейсера в детском возрасте
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
Spacer/Firma
Спейсер/производитель
Form
Форма
Поток клапан
Volumen
Ventil
Мл
вд/выд
ml
in/ex
Nebulator®
Birne
750
A
s
A
e
T
y
a
i
t
h
s
a
S
a
l
o
—
r
B
h
x
t
s
c
e
b
l
A
d
a
n
a
o
u
G
A
r
r
r
B
a
t
m
l
M
a
l
a
A
b
e
e
U
t
c
w
e
d
r
h
r
i
e
d
e
a
l
C
Падение
DruckabfallМертвое
Totraum
Давления пространство
Pa
ml
inaktiviert ―
―
―
n
®
c
поток
Fluss
л/мин
l/min
a
n
a
d
Z
y
l
i
n
d
e
r
1
4
5
i
n
Z
y
l
i
n
d
e
r
3
5
0
i
n
/
e
B
i
2
5
0
i
n
/
e
1
5
2
5
x
1
5
1
0
x
1
5
1
0
—
3
―
0
a
®
4
K
t
B
i
s
c
S
h
e
c
h
r
w
S
t
e
d
a
h
e
l
n
s
p
a
c
e
r
r
n
e
0
—
1
2
5
―
0
46. Гигиена и профилактика электризации стенок
1. Каждые 2-3 недели необходимо
чистить, мыть и сушить при комнатной
температуре (не вытирать)
2. В новый спейсер перед первым
использованием,необходимо
2-3 раза впрыснуть лекарство из
баллончика, аэрозоль оседает на
стенках, не вдыхать !
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
47. Порошковые ингаляции
Преимущества:
• Портативность
• Мобильность
• Многократное использование (Не для всех типов )
Недостатки:
• Провоцируют кашель при гиперреактивности бронхов
• Требуют высокой мощности вдоха
• Не все медикаменты можно распылять
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
48. Порошковые ингаляторы
Применение:
Спокойно и полностью выдохнуть
Обхватить мундштук губами
Слегка запрокинуть голову
Быстро и глубоко вдохнуть(возможно
использовать назальную клемму)
5. Задержать дыхание на 10 сек.
1.
2.
3.
4.
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
49. Порошковые ингаляции
Преимущества:
1. Простота использования
2. Хороший комплаенс
Недостатки:
1. Склеивание порошка при повышенной
влажности.
2. Мокрые капсулы невозможно открывать
3. Затупление перфоратора
4. При сильной бронхообструкции и уменьшении
просвета дыхательных путей, частицы порошка
могут не попадать в периферические отделы
дыхательных путей
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
50. Порошковые ингаляторы
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
Турбохалер
Изихалер
Дискхалер
51.
52. Заключение
1. Терапевт и пациент
(родители/родственники) должны
обучиться правильной технике
ингаляций с последующим контролем.
2. Необходим индивидуальный подход при
подборе ингаляционных систем
3. Необходимо постоянное обслуживание и
очистка ингаляционных приборов
4. Постоянный контроль эффективности
ингаляционной терапии. (исследование
ФВД /Пикфлоуметрия)
Х-M.Юнг – «Клиника Саттельдюне», Амрум — Германия
53.
+49-4682-34132
- Review
- Open Access
- Published: 16 January 2018
- Federico Lavorini2,
- Jonathan Marshall3,
- William Christopher Nigel Dunlop3,
- Louise Heron4,
- Emily Farrington4 &
- …
- Richard Dekhuijzen5
Respiratory Research
volume 19, Article number: 10 (2018)
Cite this article
-
22k Accesses
-
153 Citations
-
129 Altmetric
-
Metrics details
Abstract
Background
Inhaled drug delivery is the cornerstone treatment for asthma and chronic obstructive pulmonary disease (COPD). However, use of inhaler devices can be challenging, potentially leading to critical errors in handling that can significantly reduce drug delivery to the lungs and effectiveness of treatment.
Methods
A systematic review was conducted to define ‘critical’ errors and their impact on health outcomes and resource use between 2004 and 2016, using key search terms for inhaler errors in asthma and COPD (Search-1) and associated health-economic and patient burden (Search-2).
Results
Search-1 identified 62 manuscripts, 47 abstracts, and 5 conference proceedings (n = 114 total). Search-2 identified 9 studies. We observed 299 descriptions of critical error. Age, education status, previous inhaler instruction, comorbidities and socioeconomic status were associated with worse handling error frequency. A significant association was found between inhaler errors and poor disease outcomes (exacerbations), and greater health-economic burden.
Conclusions
We have shown wide variations in how critical errors are defined, and the evidence shows an important association between inhaler errors and worsened health outcomes. Given the negative impact diminished disease outcomes impose on resource use, our findings highlight the importance of achieving optimal inhaler technique, and a need for a consensus on defining critical and non-critical errors.
Background
Inhaled drug delivery is the cornerstone of therapy for the treatment of obstructive chronic airway diseases, such as asthma and chronic obstructive pulmonary disease (COPD) [1]. The most common devices used to administer aerosolized medication in day-to-day respiratory practice are the pressurized metered-dose inhaler (pMDI) and the dry powder inhaler (DPI). pMDIs are most often prescribed [2], but patients need to inhale correctly and coordinate breathing and actuation to ensure effective drug delivery [3,4,5,6]. In contrast, DPIs are breath-actuated, with most devices relying on a rapid and powerful inhalation manoeuvre for drug delivery, which can be particularly problematic for patients who struggle to inhale forcefully [6].
Recent advances in inhaler technologies have seen an explosion in the number of devices [7]. This plethora of devices, however, has led to confusion in their use amongst health-care providers (HCPs) and patients, who may not properly understand how to use inhalers [8]. Indeed, mastering an inhaler device involves correct preparation and handling of the device before inhalation, and an optimal inhalation technique; an error in any step of this process may lead to inadequate drug delivery to the lungs.
There is no one ‘perfect device’ and several studies have shown that inhaler technique errors made by patients with asthma and COPD are common in real life with both pMDIs and DPIs despite advances in inhaler device technology [3, 9,10,11,12]. Although study results vary, estimates of those making inhaler errors range up to 90% of patients irrespective of the device type used [13, 14]. Most importantly, it is vital to distinguish between ‘critical’ (sometimes defined as ‘essential’ or ‘crucial’) errors, which are likely to significantly impair the delivery of adequate medication to the lungs, and ‘non-critical’ errors, which are likely to result in a reduced amount of drug reaching the lungs compared with that attained using the correct technique [15, 16].
A recent major cross-sectional study of asthma patients has compared inhaler technique data with data on disease control, in order to determine which errors are most associated with poor health outcomes [17]. The results of this may provide the most coherent basis for defining and identifying critical errors; however, progress towards fully elucidating these errors is slow.
The societal and health-economic burden of poor inhaler technique is increasingly being recognised [10]. Worryingly, in three countries (the UK, Spain and Sweden) poor inhaler technique accounted for over €750 million in direct and indirect costs in 2015, for the two most commonly used DPIs [18]. These cost data, together with the increasing prevalence of obstructive lung diseases and restriction in healthcare spending is propagating the imperative need for inhaler competency (that is, correct and effective inhaler use) [15].
Recent global position documents from the Global Initiative for Asthma (GINA) and Global Initiative for Chronic Obstructive Lung Disease (GOLD) both give significant prominence to assessing and correcting poor inhalation technique before escalating drug therapy [19, 20].
Price et al. proposed the need for policy change and research focusing on current gaps in knowledge: specifically on the association between device errors and health economic and clinical outcomes, and on the patient characteristics associated with a higher frequency of errors [15]. Indeed, clinicians must recognise that the device itself and its characteristics are at least equally as important as the prescribed drug; and that in future, the choice of drug compound may be considered to be of secondary importance [3].
The aim of this study was to define ‘critical’ errors and their impact on health outcomes and resource use between 2004 and 2016. This was accomplished through systematically reviewing the scientific literature on inhaler errors made by patients when using pMDIs and DPIs, and the approaches used to assess them — exploring the relationships between inhaler errors, disease outcomes, quality of life, and healthcare resource use, and associations between patient characteristics and inhaler errors. Given the striking variety of inhaler errors reported in the literature [11], this paper focuses on critical errors, as these are most likely to have a health impact.
Methods
Overview
This systematic review was undertaken in accordance with the methodological and reporting standards recommended by PRISMA [21], and was registered in the PROSPERO international prospective register of systematic reviews (CRD42016036118). The review consisted of two distinct searches: search-1 focused on definitions and descriptions of critical errors, and search-2 aimed to identify the literature regarding economic models on the cost of critical errors and patient burden (see Additional file 1: Table S1).
Inclusion criteria
Studies from search-1 were included if they reported data on inhaler errors with pMDI and/or DPIs in patients with asthma or COPD, and if they related inhaler technique to disease outcomes or quality of life (QoL). Studies from search-2 were included if they reported data on the patient and/or economic burden of inhaler errors. Soft-mist inhalers and nebulisers were not considered in either search, as pMDIs and DPIs are estimated to make up around 99.8% of the global market share of inhaler devices [22].
Both searches were conducted, reviewed, and each article checked, by two authors (LH, EF) in four online databases (Embase, Medline, EconLIT and Evidence-Based Medicine Reviews), limited to studies published in English between 2004 and May 2016. International conference proceedings from 2013 to 2016 were also scanned (see Additional file 1: Table S1). All the authors reviewed the finalized list of selected articles for approval.
Data extraction
The following data were recorded from each selected article: author and contact details; number of patients; patient characteristics including age, gender, education, comorbidities, socioeconomic class, concurrent device use, and previous instruction; type(s) of inhaler; type(s) of inhaler error(s); definition of critical error(s); type of disease (asthma, COPD, or both); and findings on disease outcomes or QoL.
We grouped the emergent themes into 5 domains in our systematic review; (1) patient characteristics, (2) educational aspects, (3) disease outcomes, (4) quality of life, (5) health economics. This qualitative assessment of the study results allowed results to be reported more clearly, in order to help explore the impact of critical errors on health outcomes and resource use.
When studies were examined for evidence of an association between patient characteristics and presence or rate of inhaler errors, an a priori predefined list of characteristics agreed by consensus between the authors was used to focus analysis. This included: patient age, gender, socioeconomic class, education level, inhaler education, comorbidities, and the number of inhaler devices prescribed at the same time.
Additionally, the reference lists of all retrieved papers were reviewed for any potentially relevant studies, and editorials, commentaries, case studies, letters and opinion pieces were excluded. Studies examining nebuliser inhaler errors or those pooling nebulizer inhaler errors data with data for other inhalers were excluded, as our aim was to assess inhaler devices that administer a single discrete dose. Studies that did not specify inhaler types were included, as it was considered likely that pMDIs and DPIs would have been used, due to these of inhaler types comprising the majority of market share [23]. Descriptive methods were used to analyse data for the associations mentioned above.
Results
Search results
Initially (not including grey literature), Search-1 yielded 114 studies: 62 of these were full-text articles and 52 were abstracts. Of these, five abstracts were identified as having an economics focus and were therefore moved to the results of Search-2 (Fig. 1). Following the addition of five grey literature abstracts, the total yield of Search-1 was again 114 studies.
PRISMA diagram. The database search and analysis in Search-1 initially yielded 114 full-text articles or abstracts; give abstracts were removed and incorporated into the results of Search-2 due to being economics-focused; a further five abstracts were added to Search-1 following the grey literature search. Therefore, the final yield of Search-1 was 114
Full size image
All studies (n = 114) in Search-1 reported inhaler error data on pMDIs with or without spacers, and single- or multiple-dose DPIs (Fig. 2a and b). Study details including population age, respiratory disease, and inhaler device type are presented in Table 1.
a. Journal articles reporting critical inhaler errors for pMDIs and DPIs. Note: percentages are calculated as a proportion of total mentions (n = 105) of each inhaler type by all inhaler error studies. Individual studies may mention more than one inhaler type. b. Journal articles reporting critical inhaler errors for specific DPI device types, both multi-dose (blue) and single-dose (red). Note: percentages are calculated as a proportion of total mentions (n = 65) of all device types by all inhaler error studies. Individual studies may mention more than one inhaler type. c. Studies stating a definition of a critical error, separated into categories. Details of each study and the exact wording used by each are presented in Additional file 1: Table S4. Note: In this figure the term “critical error” refers to both critical errors and critical steps that, when performed incorrectly, constitute critical errors
Full size image
Full size table
Search-2 on the health-economic burden of inhaler errors yielded only one full-text article and three abstracts that fulfilled the inclusion criteria, to which five abstracts from Search-1 were added (Fig. 1).
Definition of critical inhaler errors
Among the 36 studies giving specific examples of ‘critical’ errors, 32 included a definition of ‘critical’ inhaler errors, and the definition itself substantially varied between the studies (Fig. 2c). In most cases, studies did not provide information on the origin of their definition of a critical error; however, where this information was provided, definitions were commonly taken from previous studies, rather than being formulated by the study researchers. Astonishingly, our search yielded 299 descriptions of critical errors across the device types.
The most common definition was an action affecting the lung deposition of inhaled drug, resulting in little or no medicine being inhaled or reaching the lungs (n = 27), where 14 definitions stated a critical error “would” certainly affect inhalation and drug delivery [24,25,26,27,28,29,30,31,32,33,34,35,36,37], and 13 others said a critical error “could” affect these [38,39,40,41,42,43,44,45,46,47,48,49,50]. Conversely, 4 papers defined a critical error in terms of effectiveness: that is, an error that would make aerosol therapy useless [10, 51,52,53]; and Pascual used a combined definition of deposition and effectiveness: that is, “an error that compromised the potential benefit of the treatment, such as impeding drug deposition or the delivery of an insufficient dose” [54].
Surprisingly, only sixty studies (53%) used a checklist to quantify errors and to enable comparisons between devices. However, these checklists were often created by the authors themselves (either taken from previous studies, or were copied from the instructions provided with the inhaler device), without external validation of the checklist itself for each device type. The number of critical errors described varied by device type and by study (Additional file 1: Table S2).
To further compound matters, there were also differences in the descriptions of the actual errors themselves. For example, one DPI error was described in four different ways: two studies mentioned the critical steps which, if not performed, would be errors: “slide lever as far as possible” [42]; “push lever back completely” [27]; and two gave differing terminology for the critical error: “failure to slide the lever until the ‘click’ sound” [51] and “not sliding back the lever until a click is heard” [30]. Similarly, there were also differences in agreement between the authors of the different studies in the categorization of a critical error versus a non-critical error, once again affecting attempts to compare studies and collectively understand the impact of inhaler errors in daily clinical practice. For example, not holding the inhaler upright whilst using a pMDI was referred to as a critical error or step by three studies [39, 42, 44], but Bryant defined it simply as an “error” [55].
While many studies reported associations between characteristics or patient experiences and errors, these did not specify whether associations existed with critical errors specifically, or with all errors.
Effects of patient characteristics on frequency of inhaler errors
Overall, 41 studies of 114 (36%) investigated the effect of predefined patient characteristics on inhaler error frequency (Table 1), with patient age, gender, level of education, number of devices prescribed, and previous inhaler instruction being the most commonly explored factors.
Of 33 studies which examined the effect of patient age [10, 26, 30, 33, 34, 38, 40, 44, 48, 53, 55,56,57,58,59,60,61,62,63,64,65,66,67,68,69,70,71,72,73,74,75,76,77], 29 were in adults and 4 were paediatric. Only twelve studies (36%) reported age to be significantly associated with worsening frequency of inhaler errors [10, 26, 30, 44, 53, 57, 60, 64, 66, 69, 72, 73], whereas 21 studies found no significant association. In 7 studies, older adults were found to make significantly more errors [10, 30, 44, 57, 60, 64, 66]. Of the 4 paediatric studies [26, 40, 53, 74], two reported a significant association between age and frequency of errors: Deerojanawong reported that younger children made errors significantly more frequently [26], while Capanoglu reported the opposite finding: that older children made errors more frequently [53]. Twenty-five studies of 114 (22%) reported on the effects of gender [10, 30, 34, 38, 40, 44, 48, 53, 55, 56, 59,60,61, 63, 65,66,67, 70, 73, 74, 76,77,78,79,80], where 6 studies concluded a significant impact on inhaler error frequency, but the results were contradictory and inconclusive as to whether male or female gender was associated with poor technique [48, 53, 60, 66, 79, 80]. Of the 22 studies that reported a trend between low education and high inhaler error frequency [10, 34, 38, 44, 48, 53, 56, 59,60,61,62, 64,65,66,67, 70, 73,74,75,76, 80, 81], 10 found the association to be statistically significant [10, 34, 48, 53, 56, 60, 62, 66, 73, 80].
Of the 114 articles, 21 studies (18%) explored the relationship between previous inhaler instruction and inhaler error frequency [10, 25, 26, 30, 36, 39, 40, 44, 48, 53, 61, 62, 66,67,68, 71, 72, 74, 76, 80, 81], where 11 studies found previous education or instruction to be significantly related to better inhaler technique [10, 36, 39, 44, 48, 53, 61, 66, 68, 76, 80]. One study by Al-Jahdali reported a significant relationship between ‘lack of education about medication’ and improper device use [67], and two reported that reduced error frequency among previously instructed patients was dependent on device type, where technique improved only in patients using MDI spacer [26] or Diskus or Turbuhaler. [30] Interestingly, a third of studies (n = 7) reported that previous instruction in inhaler use did not significantly affect inhaler technique [25, 40, 62, 71, 72, 74, 81].
Specifically, we noted a statistically significant relationship was reported between increased error frequency and other patient characteristics such as having the presence of two or more comorbidities [56], obesity [48], heart disease [80], cognitive impairment or neuropathy [79], and lower socioeconomic class [56]. There were contradictory results between three studies that reported significant results for whether a higher or lower number of devices prescribed concurrently impacts error frequency [25, 44, 82].
Effects of educational intervention on frequency of inhaler errors
Educational interventions and their relationship to inhaler errors were addressed in 52 articles [27,28,29, 34, 37, 39, 45, 49,50,51, 54, 57,58,59, 61, 83,84,85,86,87,88,89,90,91,92,93,94,95,96,97,98,99,100,101,102,103,104,105,106,107,108,109,110,111,112,113,114,115,116,117,118,119], but studies varied in how errors were assessed (the tools used), by whom (the healthcare personnel), and in the duration of intervention. Interventions were undertaken by face-to-face consultation with a variety of HCPs involving physicians (n = 5), nurses (n = 5), paramedics (n = 1), and pharmacists (n = 8). In other studies, a video (n = 5), leaflet instructions (n = 17), or an online program were used (n = 2). Thirty-two studies undertook patient assessments before and after the educational intervention [29, 34, 39, 45, 51, 57,58,59, 61, 83,84,85,86,87,88,89,90,91,92, 94, 95, 97, 100,101,102,103,104, 108, 109, 114, 115]. Where 26 studies positively reported a significant improvement in inhaler technique following the intervention [29, 34, 39, 51, 57, 58, 61, 83,84,85,86,87,88,89, 92, 94, 95, 97, 101, 103, 104, 108, 109, 114, 115].
Analysis of interventions noted that the majority of the pharmacist-led studies, seven of the eight, demonstrated a statistically significant improvement in inhaler technique [39, 61, 84, 87, 91, 101, 103]. Of the five nurse-led interventions [34, 58, 85, 90, 99], three succeeded in significantly improving inhaler technique [34, 58, 85], and two reported a decrease in inhaler error frequency but did not include a statistical analysis [90, 99]. A further six HCP studies reported statistically significant improvements: three physician-led interventions, a physician-and therapist-led study, GP assistant study and a paramedic-led study all reported statistically significant improvements [57, 83, 89, 92, 94, 97]. Four studies with unspecified instructor types reported improvement [45, 51, 95, 102], but only two provided statistical analysis [51, 95]. Of the leaflet-based intervention studies (n = 17) [27,28,29, 37, 45, 49, 50, 54, 88, 93, 104, 106, 107, 112, 115, 118, 119], five compared inhaler technique before and after the intervention, of which four reported a significant improvement in inhaler technique [29, 88, 104, 115].
Association between disease outcomes and inhaler errors
Thirty-six of the 114 studies (Table 1) examined disease outcomes in relation to inhaler errors or inhalation technique (see Table 2 for a summary of available odds ratios). In the assessment of asthma control, the most common measurements were the Asthma Control Questionnaire (ACQ) and Asthma Control Test (ACT) instruments. [120, 121] Other measurements included: the Control of Allergic Rhinitis and Asthma Test [122], Asthma Therapy Assessment Questionnaire [123], Test For Respiratory And Asthma Control In Kids scales [124], frequency of exacerbations, emergency healthcare use, or general classification of patients into levels of disease control using the Global Initiative for Asthma (GINA) criteria. For COPD patients, disease outcomes were measured by: Baseline Dyspnoea Index (BDI), rates of exacerbations, hospitalizations, or by degree of dyspnoea using the modified Medical Research Council (MRC) questionnaire.
Full size table
Our systematic analysis revealed 10 studies observed a higher inhaler error frequency was significantly associated with poor disease outcomes, primarily in asthma (n = 9), but also in asthma and COPD (n = 1) [10, 38, 48, 53, 56, 57, 67, 78, 90, 97, 117]. Molimard reported that using a device incorrectly, irrespective of the type, was associated with an increased Asthma Control Score [42], and in another study by Kuprys-Lipinska and Wiacek, over 94% of patients reported an association between improved DPI technique and better disease outcomes in asthma and COPD; however, no statistical analysis was provided [100, 109]. Groot reported that incorrect inhaler technique with unspecified inhalers was the underlying cause of poor asthma control in 7.8% of its population, but again did not provide statistical analysis [125].
We identified eight studies where the inhaler training interventions (including such aspects as physical demonstration, technique labels, and written action plans) led to an improvement in inhaler technique and also a significant increase in disease control, (seven in asthma [39, 83, 84, 87, 94, 96, 111], and one in COPD [88]) while 4 studies reported that their intervention significantly improved disease outcomes or reduced hospital admission frequency, but did not measure inhaler error frequency [98, 105, 116, 117]. Two further studies reported that training significantly improved technique and outcomes in asthma, but not in COPD patients [68, 104]. Eight studies reported no significant relationship between poor inhaler technique or errors with asthma control [34, 40, 58, 59, 70, 86, 89, 126].
Association between quality of life and inhaler errors
Seven of the 114 studies examined any association between QoL and inhaler errors: three in asthma, two in COPD and two in a mixed population.
A significant improvement in QoL was reported in three studies, following interventions which improved inhalation technique [84, 88, 91]. Basheti observed a significant correlation between improvement in DPI technique and improvement in asthma-related QoL following a pharmacist-led training intervention [84]. Goris reported significant improvements in QoL according to the St. George’s Respiratory Questionnaire (SGRQ) in all domains of QoL following intervention (aided by a movie and leaflet) in pMDI and DPI technique in COPD patients [88]. Maazuddin reported a pharmacist-led intervention led to significant improvements in the SGRQ outcomes in patients with COPD for pMDI and aerosol based devices including, Autohaler® and Evohaler®, but not for the three DPIs Revolizer®, Rotahaler® and Starhaler® [91].
A further study by Plaza reported a clinically significant increase in Mini Asthma Quality of Life Questionnaire scores among patients receiving a repeated training intervention (including development of a personalised action plan) delivered by a professional educator, physician or nurse, but the inhaler error frequency was not captured [98].
In contrast, an RCT by Hesselink found no significant impact on QoL in asthma and COPD (measured using the Quality-of-Life for Respiratory Illness Questionnaire) following a family practice assistant intervention (involving a structured consultation and use of checklist), although a significant improvement in inhaler technique was recorded [89]. An observational, retrospective study by Takemura reported unchanged SGRQ scores in asthma patients following intervention at regular intervals of at least 6 months by certified participants in a community-pharmacist educational program [103]. A further study by Pothirat captured a non-significant relationship between inhaler errors and poor quality of life, as judged by the by COPD Assessment Test (CAT) [34].
Economic models investigating the costs associated with inhaler errors
Our analysis identified eight studies [127,128,129,130,131,132,133,134,135], of which one was reported both in manuscript and abstract form [127, 128].
Roggeri reported a modelling study conducted in Italy and calculated the increased healthcare resource use by asthma or COPD patients making one or more critical inhaler error and showed this was associated with an additional yearly cost of €44,104 (asthma) or €23,444 (COPD) per 100 patients [127, 128]. Contextualising this for COPD, 100 patients making at least one inhaler error would require 11.5 additional hospitalisations, 13 emergency room visits, 19.5 courses of antimicrobials, and 47 courses of oral corticosteroids, compared to 100 patients not making any critical errors. Corresponding figures for 100 asthma patients were 19 hospitalisations, 26.5 emergency room visits, 4.5 antimicrobial courses and 21.5 oral corticosteroid courses [127, 128].
Bijos modelled the impact of poor inhaler technique on healthcare resource use in Poland, and concluded that misuse of inhaled corticosteroid and long-acting beta agonist fixed-dose combinations resulted in an annual loss of 378 million PLN (€91.1 million) in direct costs and 20.4 million PLN (€4.9 million) in indirect productivity, costs across asthma and COPD [129].
Torvinen calculated the effect on disease outcomes and the economic impact of a new DPI inhaler reported to reduce inhalation errors through innovative inhaler characteristics, and showed a potential saving of €57.78 million, based on a 10.1% rate of uptake among 701,983 patients with persistent asthma or COPD in Italy when switching to the new device from their existing DPI inhalers of Turbuhaler® or Diskus®, by year 5 of the model [130].
In the UK, Lewis considered the impact of inhaler errors on the economic burden of asthma and COPD with inhaled corticosteroid/long-acting beta-agonist (ICS/LABA) fixed-dose combinations [131]. The authors estimated that 366,000 of the 1.3 million persistent asthma/COPD patients within the UK have poor inhalation technique, and that this was associated with 11.8% (£16.2 million) of unscheduled health care events per year [131].
In a further study, Lewis estimated the additional resource use due to poor inhalation technique in Spain, and calculated a loss of €11.54 million due to unscheduled healthcare events among 563,562 asthma and COPD patients using Turbuhaler® or Accuhaler®. [132] Two similar economic models considered the impact of improved inhalation technique in asthma and COPD and in the UK and Sweden, and concluded that improved technique could save £3.5 million in the UK through reducing the number of unscheduled health events (assuming an update of 25% in years 4 and 5 of the model), and SEK285.4 million (€31.2 million) in Sweden by reducing the number of lost working days [133, 134].
Of note, four out of the 9 studies were related to the same device utilised in studies sponsored by the same company within a year of each other using the same health economic model employing a device switch approach to the study design [130, 132,133,134].
Conversely, a real world study in COPD (n = 108) conducted in Colombia reported that making inhaler errors was associated with a minor increase in monthly cost per patient ($146.9, versus $142.2 for other patients) [135].
Interestingly, no economics-focused studies on a US population were captured.
Generic issues identified
As previously mentioned, several types of inconsistency or heterogeneity between captured studies were seen during the review – each of which made the analysis of the data challenging.
The inconsistency in defining critical errors versus normal errors makes drawing conclusions on associations difficult, as errors were considered critical or non-critical by different researchers using different definitions; this is an important issue identified throughout the systematic review.
Furthermore, as differing checklists were used, containing differing numbers and descriptions of errors, error frequencies are likely not completely comparable between studies. In addition, “poor technique” was defined differently by different researchers, who commonly used differing thresholds for labelling a patient’s technique as incorrect or poor [55, 56].
In addition, although disease outcomes were captured using known measures of control, the variety of different measures used does make it more difficult to draw firm conclusions on the association between error frequency and asthma control.
Discussion
The aim of our article was to define ‘critical’ inhaler errors and their impact on health outcomes and resource use; and by doing so, to bring to the attention of physicians the importance of the inhaler device in their daily prescribing in the management of patients with asthma and COPD. Indeed, both GINA and GOLD now highlight the critical importance of assessing inhaler technique to guide appropriate inhaler prescribing, with a concerted drive to educate professionals and patients about the real impact of inhaler errors on the patients’ disease control, as well as on the financial economics of societal health.
To our knowledge this is the first formally registered evidence-based systematic review with a priori clearly formulated questions that documents the wide discrepancies within the literature regarding definitions and descriptions of inhaler errors and their classification as either ‘critical’ or ‘non-critical’. Previous reviews such as that by Basheti et al. focusing on inhaler error checklists have approached these issues [136], although in a different context.
Astonishingly, we observed 299 different descriptions of critical inhaler errors. Even for the same inhaler device type, different terminology was used between different study authors to describe the same inhaler error, and this may contribute to the confusion observed in clinical practice with regards to best inhaler practice and the limitations in determining associations with inhaler errors [8]. This heterogeneity and lack of consensus fundamentally hampers the ability to interpret studies with respect to the impact of inhaler errors. Indeed, the different definitions of critical error could be a contributing factor to extremely different conclusions even with the same inhaler device type; as exemplified in the Melani study where MDI users were significantly less likely to commit critical errors relative to DPI users [10], in contrast to the Batterink study where MDI users were most likely to make critical errors [25].
The lack of consensus between researchers extends to the use of differing inhaler technique checklists. As the checklists used are not standardized, even within individual inhaler device types, comparing error rates between or within inhaler device types is unfeasible. Future research can and should adopt more consistent inhaler technique checklists, as the manufacturers’ instructions are available to form a basis for a checklist in almost all cases.
We observed several important factors, including older age, education status, lack of previous inhaler instruction, and lower socioeconomic class, which were all associated with high inhaler error frequency. In addition, inhaler technique interventions were found to decrease error frequency, and have positive impacts on disease and patient outcomes, as has previously been described in the literature by Basheti et al. [137].
However these findings were not reflected in all studies, likely due to differences in study design and populations. For example, both interventional and observational studies were included, there were different inhaler devices included (i.e. pMDI or DPI), and wide ranging population sizes (between 46 and 6512 individuals), thereby limiting our ability to directly compare the results.
Interestingly, a significant association with error frequency was found for some comorbidities that are known to be strongly correlated with age, such as obesity, heart disease, or cognitive impairment [48, 79, 80]; but despite this, only around a third of studies that examined age itself reported a significant association with error frequency.
Our systematic review identified studies showing an association between inhaler errors and poor asthma control and COPD disease stability. This is in line with a recent individual study that has demonstrated that inhaler errors affect drug delivery [138]. Sulaiman showed in a laboratory environment that deliberately making certain inhaler errors led to a reduced amount of drug reaching the bloodstream [138]. However, the limited quantity of disclosed research in this area may suggest that the term “critical” is being overused, with only a weak basis for categorising errors as such.
In a recent real-world study by Molimard in 2935 patients an increased risk of COPD exacerbation among patients who made a critical inhaler error, was confirmed [139]. A further study by Price determined that the error of “insufficient respiratory effort” was associated with increased asthma exacerbation rate, as well as decreased control in general [140].
Importantly, we identified eight economic models which linked inhaler errors to economic burden, of which one study by Roggeri demonstrated a specific link between critical errors and resource use, leading to an excess cost of many thousands of Euros per 100 patients making critical errors [127, 128]. Indeed, recently Lewis and colleagues showed that poor inhalation technique led to approximately ¾ billion euros in direct and indirect costs for just two DPI inhalers used over 1 year [18].
Previous literature has also demonstrated that poor disease outcomes are linked with worsened QoL and increased resource use and economic burden through increased physician consultation time and lost productivity (Additional file 1: Table S3) [141,142,143,144,145,146]. Therefore, the issue of inhaler errors is important to address due to the downstream effects on patients, healthcare systems and society.
Our findings clearly illustrate inhaler technique can be affected by the level of instruction from HCPs. It is therefore important to interpret clinical trial results with caution, given that their controlled environment (where all patients are instructed in inhaler use) may not be representative of clinical practice in real life. This issue is especially important in the context of different inhaler devices that may have ergonomic designs and functions, as raised by Scichilone et al. in a 2015 review [147]. The key message here is that in day-to-day practice, it may be an efficient strategy to provide patients at higher risk of errors with additional specifically tailored in-depth support with their inhaler use, to ensure they are confident with the correct technique.
Greater attention is clearly needed on the routine review of inhaler technique in the patient population as a whole, as a recent study by Sanchis reported rates of common inhaler errors to be static over a period of several decades [11], and data also show that despite optimally prescribed inhaled therapy, levels of asthma control and COPD disease stability remain poor [18, 145].
In comparison with a previously published systematic review only on DPI inhaler errors, our review encompasses a wider range of device types including the most commonly used inhaler device, the pMDI [14]. Whilst Lavorini et al. included data on critical errors and provided a definition of a critical error, their study focused on the incidence of errors and the possible implications for clinical effectiveness of inhalers [14]. A key strength of our review is that it integrates the link between inhaler errors and disease outcomes and QoL, and provides a systematic overview of how these critical inhaler errors are being assessed and measured.
Direct comparisons and synthesis of the data were challenging due to mixed methodologies (such as observational cross-sectional, or interventional cross-over designs, and designs intended for descriptive or qualitative analysis), different patient populations, and varied endpoints. Yet, despite these differences we observed clear trends in our data. However, due to the vast differences between studies, this review did not examine clinical outcomes by device, but this is an important area for future research.
Furthermore, only a handful of the reviewed studies directly addressed patient outcomes and the economic burden of inhaler errors. Therefore, further research and potential health-economic modelling to understand the relationship between inhaler technique and disease outcomes, and the subsequent impact on societal healthcare systems, is vitally required.
Although the present study shows associations between inhaler errors and patient outcomes through a review of chronic obstructive respiratory diseases as a whole, future research may be able to probe further into the two diseases (asthma and COPD). For example, the generally older age, poor prognosis and comorbidities of COPD patients may influence the degree to which their QoL is increased by improvements in technique and control [148]. The substantially higher prevalence of comorbidities among COPD patients, relative to asthma patients, also likely impacts inhaler technique and patient QoL [148].
With the variety of definitions identified in our review, difficulties arise in determining whether a particular inhaler type is inherently more vulnerable to critical inhaler errors. Consistent use of our proposed definition and categorization by all researchers internationally would transform this area of research and greatly facilitate quantitative and objective comparison between devices, providing a clearer indication of the associated error rates. This would revolutionise everyday clinical practice, where reliable comparisons of error rates would greatly help physicians and aid informed treatment decisions, ensuring the most appropriate device is prescribed for the individual patient with clear implications for personalised patient management. Further research into the association of patient characteristics with error rate could examine “health literacy”, a patient’s insight into their own treatment and health system, and determine if poor knowledge is a risk factor for poor technique [115, 149,150,151].
It is clear that inhaler errors have an effect on disease outcomes, and ultimately patient outcomes and economic burden. This in turn will have an impact on overall disease management and affect not only patients but also the wider healthcare system. These findings are increasingly important given the plethora of devices available to HCPs and patients, and highlight the importance of inhaler mastery in managing and treating asthma and COPD.
There is increasing evidence to suggest that correct inhaler technique (mastery) is fundamental for effective therapy, and that inhaler device type and mastery play important roles in improving adherence, clinical outcomes, quality of life, and use of healthcare resources. Evidence suggests that prescribers should consider patients’ mastery of technique (or lack thereof) and ease of use before changing the dose of inhaled medications, switching to a different inhaler, or adding other treatments to the regimen of patients with poorly controlled asthma. Recent international asthma guidelines highlight the importance of testing and ensuring mastery, alongside checking adherence, before increasing or changing therapy.
Conclusions
In conclusion, the multitude of definitions cited within the literature indicates that there is an urgent need for a consensus in the way in which critical (and non-critical) inhaler errors are defined. We propose defining a critical inhaler error as an action or inaction that in itself would have a definite detrimental impact on the delivery of the drug to the lung, in contrast to a non-critical error which we would define as an action or inaction that in combination with other factors may, or may not, contribute to ineffective delivery of the drug to the lung.
We advocate that there is a real need for an independent international panel of inhalation experts to collectively determine, through evidence and consensus, the definitions of critical and non-critical inhaler errors. If done for each device type, this would demystify the current confusion within the respiratory community.
We also propose that future studies classify individual errors into categories such as inhalation manoeuvre, dose preparation, inhaler handling, device-specific or generic, in order to make comparison and analysis simpler in order to ultimately help healthcare professionals help their patients.
Abbreviations
- ACQ :
-
Asthma Control Questionnaire
- ACT:
-
Asthma Control Test
- ATAQ:
-
Asthma Therapy Assessment Questionnaire
- BDI:
-
Baseline Dyspnoea Index
- CAT:
-
COPD Assessment Test
- CI:
-
Confidence interval
- COPD:
-
Chronic obstructive pulmonary disease
- DPI:
-
Dry-powder inhaler
- GINA :
-
Global Initiative for Asthma
- GOLD:
-
Global Initiative for Chronic Obstructive Lung Disease
- GP:
-
General Practitioner
- HCP:
-
Healthcare provider
- ICS:
-
Inhaled corticosteroid
- LABA:
-
Long-acting beta agonist
- MDI:
-
Metered-dose inhaler
- mMRC:
-
Modified Medical Research Council (questionnaire)
- pMDI:
-
Pressurized metered-dose inhaler
- PRISMA:
-
Preferred Reporting Items for Systematic Reviews and Meta-Analyses
- QoL:
-
quality of life
- RCT:
-
Randomised controlled trial
- SGRQ:
-
St George’s Respiratory Questionnaire
References
-
Gregory KL, Elliott D, Dunne P. Guide to aerosol delivery devices for physicians, nurses, pharmacists and other health care professionals [https://www.aarc.org/wp-content/uploads/2014/08/aerosol_guide_pro.pdf] Accessed: 10 Nov 2015.
-
Pritchard JN. Industry guidance for the selection of a delivery system for the development of novel respiratory products. Expert Opin Drug Deliv. 2015;12:1755–65.
Article
PubMed
CASGoogle Scholar
-
Lavorini F, Usmani OS. Correct inhalation technique is critical in achieving good asthma control. Prim Care Respir J. 2013;22:385–6.
Article
PubMedGoogle Scholar
-
Wright J, Brocklebank D, Ram F. Inhaler devices for the treatment of asthma and chronic obstructive airways disease (COPD). Qual Saf Health Care. 2002;11:376–82.
Article
CAS
PubMed
PubMed CentralGoogle Scholar
-
Price D, Marshall J, Turner R. Inhaler use in five european countries: analysis of sales data from Q4 2005 to Q4 2011. Value Health. 2012;15:A-PMD92.
Google Scholar
-
Price D, Roche N, Christian Virchow J, Burden A, Ali M, Chisholm A, Lee AJ, Hillyer EV, von Ziegenweidt J. Device type and real-world effectiveness of asthma combination therapy: an observational study. Respir Med. 2011;105:1457–66.
Article
PubMedGoogle Scholar
-
Lavorini F, Fontana GA, Usmani OS. New inhaler devices — the good, the bad and the ugly. Respiration. 2014;88:3–15.
Article
PubMedGoogle Scholar
-
Haughney J, Price D, Barnes N, Virchow J, Roche N, Chrystyn H. Choosing inhaler devices for people with asthma: current knowledge and outstanding research needs. Respir Med. 2010;3:125–31.
Google Scholar
-
Molimard M, Raherison C, Lignot S, Depont F, Abouelfath A, Moore N. Assessment of handling of inhaler devices in real life: an observational study in 3811 patients in primary care. J Aerosol Med. 2003;16:249–54.
Article
CAS
PubMedGoogle Scholar
-
Melani AS, Bonavia M, Cilenti V, Cinti C, Lodi M, Martucci P, Serra M, Scichilone N, Sestini P, Aliani M, Neri M. Inhaler mishandling remains common in real life and is associated with reduced disease control. Respir Med. 2011;105:930–8.
Article
PubMedGoogle Scholar
-
Sanchis J, Gich I, Pedersen S. Systematic review of errors in inhaler use: has patient technique improved over time? Chest. 2016;150:394–406.
Article
PubMedGoogle Scholar
-
Molimard M, Raherison C, Lignot S, Balestra A, Lamarque S, Chartier A, Droz-Perroteau C, Lassalle R, Moore N, Girodet PO. Chronic obstructive pulmonary disease exacerbation and inhaler device handling: real-life assessment of 2935 patients. Eur Respir J. 2017;49. doi:10.1183/13993003.01794-2016.
-
Al-Showair RA, Tarsin WY, Assi KH, Pearson SB, Chrystyn H. Can all patients with COPD use the correct inhalation flow with all inhalers and does training help? Respir Med. 2007;101:2395–401.
Article
PubMedGoogle Scholar
-
Lavorini F, Magnan A, Christophe Dubus J, Voshaar T, Corbetta L, Broeders M, Dekhuijzen R, Sanchis J, Viejo JL, Barnes P, et al. Effect of incorrect use of dry powder inhalers on management of patients with asthma and COPD. Respir Med. 2008;102:593–604.
Article
PubMedGoogle Scholar
-
Price D, Bosnic-Anticevich S, Briggs A, Chrystyn H, Rand C, Scheuch G, Bousquet J. Inhaler competence in asthma: common errors, barriers to use and recommended solutions. Respir Med. 2013;107:37–46.
Article
CAS
PubMedGoogle Scholar
-
van der Palen J, Klein JJ, Kerkhoff AH, van Herwaarden CL, Seydel ER. Evaluation of the long-term effectiveness of three instruction modes for inhaling medicines. Patient Educ Couns. 1997;32:S87–95.
Article
CAS
PubMedGoogle Scholar
-
Price DB, Roman-Rodriguez M, RB MQ, Bosnic-Anticevich S, Carter V, Gruffydd-Jones K, Haughney J, Henrichsen S, Hutton C, Infantino A, et al. Inhaler errors in the CRITIKAL study: type, frequency, and association with asthma outcomes. J Allergy Clin Immunol Pract. 2017;5:1071–1081.e1079.
Article
PubMedGoogle Scholar
-
Lewis A, Torvinen S, Dekhuijzen PN, Chrystyn H, Watson AT, Blackney M, Plich A. The economic burden of asthma and chronic obstructive pulmonary disease and the impact of poor inhalation technique with commonly prescribed dry powder inhalers in three European countries. BMC Health Serv Res. 2016;16:251.
Article
CAS
PubMed
PubMed CentralGoogle Scholar
-
Global initiative for chronic obstructive lung disease: pocket guide to COPD diagnosis, management and prevention [http://goldcopd.org/wp-content/uploads/2016/12/wms-GOLD-2017-Pocket-Guide.pdf] Accessed: 26 May 2017.
-
Global initiative for asthma: pocket guide for asthma management and prevention [http://ginasthma.org/2017-pocket-guide-for-asthma-management-and-prevention/] Accessed: 25 July 2017.
-
Liberati A, Altman DG, Tetzlaff J, Mulrow C, Gøtzsche PC, Ioannidis JPA, Clarke M, Devereaux PJ, Kleijnen J, Moher D. The PRISMA statement for reporting systematic reviews and meta-analyses of studies that evaluate healthcare interventions: explanation and elaboration. Br Med J. 2009;339:b2700.
-
IMS Health: IMS MIDAS Q4 MAT 2016, EU5. 2016.
Google Scholar
-
Lavorini F, Corrigan CJ, Barnes PJ, Dekhuijzen PR, Levy ML, Pedersen S, Roche N, Vincken W, Crompton GK. Aerosol drug management improvement team: retail sales of inhalation devices in European countries: so much for a global policy. Respir Med. 2011;105:1099–103.
Article
CAS
PubMedGoogle Scholar
-
Basheti IA, Qunaibi E, Bosnic-Anticevich SZ, Armour CL, Khater S, Omar M, Reddel HK. User error with diskus and turbuhaler by asthma patients and pharmacists in Jordan and Australia. Respir Care. 2011;56:1916–23.
Article
PubMedGoogle Scholar
-
Batterink J, Dahri K, Aulakh A, Rempel C. Evaluation of the use of inhaled medications by hospital inpatients with chronic obstructive pulmonary disease. Can J Hosp Pharm. 2012;65:111–8.
PubMed
PubMed CentralGoogle Scholar
-
Deerojanawong J, Na Sakolnakorn VP, Prapphal N, Hanrutakorn C, Sritippayawan S. Evaluation of metered-dose inhaler administration technique among asthmatic children and their caregivers in Thailand. Asian Pac J Allergy Immunol. 2009;27:87–93.
PubMed
Google Scholar
-
Van Der Palen J, Van Der Valk P, Goosens M, Groothuis-Oudshoorn K, Brusse-Keizer M. A randomised cross-over trial investigating the ease of use and preference of two dry powder inhalers in patients with asthma or chronic obstructive pulmonary disease. Expert Opin Drug Deliv. 2013;10:1171–8.
Article
PubMedGoogle Scholar
-
Van Der Palen J, Ginko T, Kroker A, Van Der Valk P, Goosens M, Padulles L, Seoane B, Rekeda L, Garcia Gil E. Preference, satisfaction and errors with two dry powder inhalers in patients with COPD. Expert Opin Drug Deliv. 2013;10:1023–31.
Article
PubMedGoogle Scholar
-
Voshaar T, Spinola M, Linnane P, Campanini A, Lock D, Lafratta A, Scuri M, Ronca B, Melani AS. Comparing usability of NEXThaler with other inhaled corticosteroid/long-acting beta2-agonist fixed combination dry powder inhalers in asthma patients. J Aerosol Med Pulm Drug Deliv. 2014;27:363–70.
Article
CAS
PubMed
PubMed CentralGoogle Scholar
-
Wieshammer S, Dreyhaupt J. Dry powder inhalers: which factors determine the frequency of handling errors? Respiration. 2008;75:18–25.
Article
PubMedGoogle Scholar
-
Capstick T, Clifton I, Morgan J, Silcock J, Blenkinsopp A. Inhaler technique: an unmet need in patients with difficult asthma? Eur Respir J. 2013;42:A-4893.
Google Scholar
-
Nama S, Percival M, Harris M, Nolan-Neylan S, Sivakumaran P, Sriram K, Harland K. Evaluation of inhaler technique and medication adherence in COPD patients. Respirology. 2014;19:A-TP146.
Google Scholar
-
Vanderman AJ, Moss JM, Bailey JC, Melnyk SD, Brown JN. Inhaler misuse in an older adult population. Consult Pharm. 2015;30:92–100.
Article
PubMedGoogle Scholar
-
Pothirat C, Chaiwong W, Phetsuk N, Pisalthanapuna S, Chetsadaphan N, Choomuang W. Evaluating inhaler use technique in COPD patients. Int J Chron Obstruct Pulmon Dis. 2015;10:1291–8.
Article
CAS
PubMed
PubMed CentralGoogle Scholar
-
Madkour A, Galal I. Do Egyptian patients use their inhalers correctly? A checklist auditing for inhalation devices usage techniques. Egyptian J Chest Dis Tuberculosis. 2015;64:497–504.
Article
Google Scholar
-
Ozturk C, Aldag Y. Evaluation and importance of different types of inhaler device use in patients with chronic obstructive lung disease (COPD). Respirology. 2015;20(S3):A-471.
-
Chrystyn H, Price DB, Molimard M, Haughney J, Bosnic-Anticevich S, Lavorini F, Efthimiou J, Shan D, Sims E, Burden A. Comparison of serious inhaler technique errors made by device-naïve patients using three different dry powder inhalers: a randomised, crossover, open-label study. BMC Pulm Med. 2016;16:12.
Article
PubMed
PubMed Central
CASGoogle Scholar
-
Coelho ACC, Souza-Machado A, Leite M, Almeida P, Castro L, Cruz CS, Stelmach R, Cruz AA. Use of inhaler devices and asthma control in severe asthma patients at a referral center in the city of Salvador, Brazil. J Bras Pneumol. 2011;37:720–8.
Article
PubMedGoogle Scholar
-
Giraud V, Allaert FA, Roche N. Inhaler technique and asthma: Feasability and acceptability of training by pharmacists. Respir Med. 2011;105:1815–22.
Article
PubMedGoogle Scholar
-
Hagmolen of ten Have W, van de Berg NJ, Bindels PJ, van Aalderen WM, van der Palen J. Assessment of inhalation technique in children in general practice: increased risk of incorrect performance with new device. J Asthma. 2008;45:67–71.
Article
PubMedGoogle Scholar
-
Mehuys E, Boussery K, Adriaens E, van Bortel L, De Bolle L, van Tongelen I, Remon JP, Brusselle G. COPD management in primary care: an observational, community pharmacy-based study. Ann Pharmacother. 2010;44:257–66.
Article
PubMedGoogle Scholar
-
Molimard M, Gros VL. Impact of patient-related factors on asthma control. J Asthma. 2008;45:109–13.
Article
PubMedGoogle Scholar
-
Rajan S, Gogtay J. Ease-of-use, preference, confidence, and satisfaction with Revolizer, a novel dry powder inhaler, in an Indian population. Lung India. 2014;31:366–74.
Article
PubMed
PubMed CentralGoogle Scholar
-
Rootmensen G, Van Keimpema AR, Jansen HM, De Haan RJ. Predictors of incorrect inhalation technique in patients with asthma or COPD. Am J Respir Crit Care Med. 2010;181:A-3812.
Google Scholar
-
Schulte M, Osseiran K, Betz R, Wencker M, Brand P, Meyer T, Haidl P. Handling of and preferences for available dry powder inhaler systems by patients with asthma and COPD. J Aerosol Med Pulm Drug Deliv. 2008;21:321–8.
Article
CAS
PubMedGoogle Scholar
-
Van Der Palen J, Ginko T, Kroker A, Van Der Valk P, Goosens M, Padulles L, Seoane B, Rekeda L, Gil EG. Comparison of the preference, satisfaction, and critical errors made with Genuair and Handihaler in patients with COPD. Chest. 2012;142:A-717A.
Article
Google Scholar
-
Molimard M. How to achieve good compliance and adherence with inhalation therapy. Curr Med Res Opin. 2005;21:S33–7.
Article
PubMedGoogle Scholar
-
Westerik JA, Carter V, Chrystyn H, Burden A, Thompson SL, Ryan D, Gruffydd-Jones K, Haughney J, Roche N, Lavorini F, et al. Characteristics of patients making serious inhaler errors with a dry powder inhaler and association with asthma-related events in a primary care setting. J Asthma. 2016;53:321–9.
Article
PubMed
PubMed CentralGoogle Scholar
-
Chrystyn H, Bosnic-Anticevich S, Roche N, Molimard M, Haughney J, Lavorini F, Shan D, Sims E, Burden A, Ashton VL. Prevalence of serious post-training inhaler technique errors made by device-naïve patients using three different dry powder inhalers (DPIs). Eur Respir J. 2015;46:A-P3927.
Google Scholar
-
Thomas M, Van der Palen J, Chrystyn H, Sharma R, Imber V, Zhu C-Q, Barnes N. Inhaler errors and preference: a comparison of two multi-dose powder asthma inhalers. Respirology. 2015;20:A-573.
Article
Google Scholar
-
Li H, Chen Y, Zhang Z, Dong X, Zhang G, Zhang H. Handling of diskus dry powder inhaler in Chinese chronic obstructive pulmonary disease patients. J Aerosol Med Pulm Drug Deliv. 2014;27:219–27.
Article
PubMedGoogle Scholar
-
Melani AS, Canessa P, Coloretti I, Deangelis G, Detullio R, Del Donno M, Giacobbe R, Scarlato I, Serafini A, Barbato N, et al. Inhaler mishandling is very common in patients with chronic airflow obstruction and long-term home nebuliser use. Respir Med. 2012;106:668–76.
Article
PubMedGoogle Scholar
-
Capanoglu M, Dibek Misirlioglu E, Toyran M, Civelek E, Kocabas CN. Evaluation of inhaler technique, adherence to therapy and their effect on disease control among children with asthma using metered dose or dry powder inhalers. J Asthma. 2015;52:838–45.
Article
PubMed
CASGoogle Scholar
-
Pascual S, Feimer J, De Soyza A, Sauleda Roig J, Haughney J, Padulles L, Seoane B, Rekeda L, Ribera A, Chrystyn H. Preference, satisfaction and critical errors with Genuair and Breezhaler inhalers in patients with COPD: a randomised, cross-over, multicentre study. NPJ Prim Care Respir Med. 2015;25:15018.
Article
PubMed
PubMed CentralGoogle Scholar
-
Bryant L, Bang C, Chew C, Hee Baik S, Wiseman D. Adequacy of inhaler technique used by people with asthma or chronic obstructive pulmonary disease. JJ Prim Health Care. 2013;5:191–8.
Google Scholar
-
Dalcin PTR, Grutcki DM, Laporte PP, de Lima PB, Menegotto SM, Pereira RP. Factors related to the incorrect use of inhalers by asthma patients. J Bras Pneumol. 2014;40:13–20.
Article
PubMed CentralGoogle Scholar
-
Giraud V, Allaert FA, Magnan A. A prospective observational study of patient training in use of the autohaler inhaler device: the sirocco study. Eur Rev Med Pharmacol Sci. 2011;15:563–70.
CAS
PubMedGoogle Scholar
-
Harnett CM, Hunt EB, Bowen BR, O’Connell OJ, Edgeworth DM, Mitchell P, Eustace JA, Henry MT, Kennedy MP, Plant BJ, Murphy DM. A study to assess inhaler technique and its potential impact on asthma control in patients attending an asthma clinic. J Asthma. 2014;51:440–5.
Article
CAS
PubMedGoogle Scholar
-
Loh LC, Teng CL, Teh PN, Koh CN, Vijayasingham P, Thayaparan T. Metered-dose inhaler technique in asthmatic patients — a revisit of the Malaysian scene. Med J Malaysia. 2004;59:335–41.
CAS
PubMedGoogle Scholar
-
Chorao P, Pereira AM, Fonseca JA. Inhaler devices in asthma and COPD — an assessment of inhaler technique and patient preferences. Respir Med. 2014;108:968–75.
Article
PubMedGoogle Scholar
-
Hammerlein A, Muller U, Schulz M. Pharmacist-led intervention study to improve inhalation technique in asthma and COPD patients. J Eval Clin Pract. 2011;17:61–70.
Article
PubMedGoogle Scholar
-
Al-Hassan MI. Assessment of inhaler technique in patients attending a chest hospital in Riyadh City. Int J Pharmacol. 2009;5:232–5.
Article
Google Scholar
-
Komase Y, Asako A, Kobayashi A, Sharma R. Ease-of-use preference for the ELLIPTA dry powder inhaler over a commonly used single-dose capsule dry powder inhaler by inhalation device-naive Japanese volunteers aged 40 years or older. Int J COPD. 2014;9:1365–75.
Article
Google Scholar
-
Ozturk C, Kaya A, Bilgin C, Yucesoy L, Ikidag B, Demirel M, Baslilar S, Saylan B, Senol T, Aganoglu S, et al. Evaluation of inhaler technique and patient satisfaction with fixed-combination budesonide/formoterol dry-powder inhaler in chronic obstructive pulmonary disease (COPD): data on real-life clinical practice in Turkey. Tuberk Toraks. 2012;60:301–13.
Article
PubMedGoogle Scholar
-
Nolan-Neylan S, Harris M, Harland K, Sriram K. Evaluation of inhaler technique in hospitalised COPD patients. Respirology. 2015;20:A-P002.
Google Scholar
-
Lee SM, Chang YS, Kim CW, Kim TB, Kim SH, Kwon YE, Lee JM, Lee SK, Jeong JW, Park JW, et al. Skills in handling Turbuhaler, Diskus, and pressurized metered-dose inhaler in Korean asthmatic patients. Allergy Asthma Immunol Res. 2010;3:46–52.
Article
PubMed
PubMed CentralGoogle Scholar
-
Al-Jahdali H, Ahmed A, Al-Harbi A, Khan M, Baharoon S, Bin Salih S, Halwani R, Al-Muhsen S. Improper inhaler technique is associated with poor asthma control and frequent emergency department visits. Allergy Asthma Clin Immunol. 2013;9:8.
Article
PubMed
PubMed CentralGoogle Scholar
-
Maricoto T, Rodrigues LV, Teixeira G, Valente C, Andrade L, Saraiva A. Assessment of inhalation technique in clinical and functional control of asthma and chronic obstructive pulmonary disease. Acta Med Port. 2015;28:702–7.
Article
PubMedGoogle Scholar
-
Manriquez P, Acuna AM, Munoz L, Reyes A. Study of inhaler technique in asthma patients: differences between pediatric and adult patients. J Bras Pneumol. 2015;41:405–9.
Article
PubMed
PubMed CentralGoogle Scholar
-
Sriram KB, Percival M. Suboptimal inhaler medication adherence and incorrect technique are common among chronic obstructive pulmonary disease patients. Chron Respir Dis. 2015;13:13–22.
Article
PubMed
PubMed CentralGoogle Scholar
-
Buset EMN, Liaaen ED, Roth K, Blix HS. Inhalation technique in hospitalized asthma and COPD patients: should patients be regularly assessed before discharge? Int J Clin Pharm. 2015;37:A-16.
Google Scholar
-
Cayo-Quiñe A, Martínez-Vargas V, Bustamante-Voysest R, Piscoya A, Alberca Y: Incorrect use of metered-dose inhalers in adult patients at a hospital in Callao, Peru, 2014: cross-sectional study. Medwave 2014, 15:e6163-e6163.
-
Sangita P, Gharti KP, Laxman B. Assessment of inhalation techniques in COPD patients using metered-dose inhaler and Rotahaler at a tertiary care hospital in Nepal. Int Res J Pharm. 2015;6:288–93.
Article
Google Scholar
-
Villamil-Osorio M, Medina L, Pernett L, Restrepo SM, Nino G, Rodriguez-Martinez C. Assessment of inhalation technique and predictors of poor inhalation technique in a population of asthmatic children. J Aerosol Med Pulm Drug Deliv. 2015;191:A-3370.
Google Scholar
-
Udwadia ZZ, Kathar S, Shah HD, Pandey K, Rastogi S, Mullerpattan J. Who will teach the teachers: an analysis of the inhaler technique of Indian patients and health care providers. Am J Res Crit Care Med. 2013;187:A5026.
-
Turan P, Itil O, Turan M. Factors effecting inhaler technique in COPD. Am J Res Crit Care Med. 2014;189:A-6000.
-
Wu H, Thomas L, Bime C. An assessment of inhaler technique among patients with chronic obstructive airway diseases in a health professional shortage area. Am Philos Soc. 2013;187:A4208.
-
Baddar S, Jayakrishnan B, Al-Rawas OA. Asthma control: importance of compliance and inhaler technique assessments. J Asthma. 2014;51:429–34.
Article
PubMedGoogle Scholar
-
Sadowski C, Banh H, Cor K, Cave A. Inhaler device technique in community-dwelling older adults. Canadian Journal of. Hosp Pharm. 2013;66(4):269.
Google Scholar
-
Camilleri K, Balzan M, Bardon MP, Schembri E, Sullivan M, Mifsud S, Muscat D, Asciaq R, Montefort S. Predictors of good inhaler technique in asthma and COPD. Eur Respir J. 2015;46:A-P3928.
Google Scholar
-
Ganguly A, Das A, Roy A, Adhikari A, Banerjee J, Sen S. Study of proper use of inhalational devices by bronchial asthma or copd patients attending a tertiary care hospital. J Clin Diagn Res. 2014;8:HC04–7.
PubMed
PubMed CentralGoogle Scholar
-
Khassawneh BY, Al-Ali MK, Alzoubi KH, Batarseh MZ, Al-Safi SA, Sharara AM, Alnasr HM. Handling of inhaler devices in actual pulmonary practice: metered-dose inhaler versus dry powder inhalers. Respir Care. 2008;53:324–8.
PubMed
Google Scholar
-
Barthwal MS, Katoch CDS, Marwah V. Impact of optimal asthma education programme on asthma morbidity, inhalation technique and asthma knowledge. J Assoc Physicians India. 2009;57:574–9.
CAS
PubMedGoogle Scholar
-
Basheti IA, Armour CL, Bosnic-Anticevich SZ, Reddel HK. Evaluation of a novel educational strategy, including inhaler-based reminder labels, to improve asthma inhaler technique. Patient Educ Couns. 2008;72:26–33.
Article
PubMedGoogle Scholar
-
Burkhart PV, Rayens MK, Bowman RK. An evaluation of children’s metered-dose inhaler technique for asthma medications. Nurs Clin N Am. 2005;40:167–82.
Article
Google Scholar
-
Carpenter DM, Lee C, Blalock SJ, Weaver M, Reuland D, Coyne-Beasley T, Mooneyham R, Loughlin C, Geryk LL, Sleath BL. Using videos to teach children inhaler technique: a pilot randomized controlled trial. J Asthma. 2015;52:81–7.
Article
PubMedGoogle Scholar
-
Garcia-Cardenas V, Sabater-Hernandez D, Kenny P, Martinez-Martinez F, Faus MJ, Benrimoj SI. Effect of a pharmacist intervention on asthma control. A cluster randomised trial. Respir Med. 2013;107:1346–55.
Article
PubMedGoogle Scholar
-
Goris S, Tasci S, Elmali F. The effects of training on inhaler technique and quality of life in patients with COPD. J Aerosol Med Pulm Drug Deliv. 2013;26:336–44.
Article
PubMed
CASGoogle Scholar
-
Hesselink AE, Penninx BWJH, Van Der Windt DAWM, Van Duin BJ, De Vries P, Twisk JWR, Bouter LM, Van Eijk JTM. Effectiveness of an education programme by a general practice assistant for asthma and COPD patients: results from a randomised controlled trial. Patient Educ Couns. 2004;55:121–8.
Article
PubMedGoogle Scholar
-
Levy ML, Hardwell A, McKnight E, Holmes J. Asthma patients’ inability to use a pressurised metered-dose inhaler (pMDI) correctly correlates with poor asthma control as defined by the global initiative for asthma (GINA) strategy: a retrospective analysis. Prim Care Res J. 2013;22:406–11.
Google Scholar
-
Maazuddin M, Hazari MAH, Hasan A, Javeedullah M, Nasir Mohiuddin M, Baig MMA. Training in the use of inhalation devices and respiratory improvement in asthma and COPD patients: a before-after experimental study. Pharmanest. 2014;5:2314–20.
Google Scholar
-
Minai BA, Martin JE, Cohn RC. Results of a physician and respiratory therapist collaborative effort to improve long-term metered-dose inhaler technique in a pediatric asthma clinic. Respir Care. 2004;49:600–5.
PubMed
Google Scholar
-
Van Der Palen J, Eijsvogel MM, Kuipers BF, Schipper M, Vermue NA. Comparison of the Diskus inhaler and the Handihaler regarding preference and ease of use. J Aerosol Med. 2007;20:38–44.
Article
PubMedGoogle Scholar
-
Yildiz F, Erbagci A, Demirel YS, Akcali SD, Ekici A, Dursunoglu N, Ediger D, Erdinc M, Cemri SC, Kalyoncu AF, et al. Importance of inhaler device use status in the control of asthma in adults: the asthma inhaler treatment study. Respir Care. 2014;59:223–30.
Article
PubMedGoogle Scholar
-
Elgendy MO, Abdelrahim ME, Eldin RS. Potential benefit of repeated MDI inhalation technique counselling for patients with asthma. Eur J Hosp Pharm. 2015;22:318–22.
Article
Google Scholar
-
Grover C, Goel N, Armour C, Van Asperen P, Gaur S, Moles R, Saini B. Medication education program for Indian children with asthma: a feasibility study. Niger J Clin Pract. 2016;19:76–84.
Article
CAS
PubMedGoogle Scholar
-
Kuna P, Kupryś-Lipińska I, Dębowski T. Control of asthma in adults treated with beclomethasone and formoterol in extrafine particle formulation in a real-life setting in Poland: the CASPER noninterventional, observational trial. Pol Arch Med Wewn. 2015;125:731–40.
PubMed
Google Scholar
-
Plaza V, Peiró M, Torrejón M, Fletcher M, López-Viña A, Ignacio JM, Quintano JA, Bardagí S, Gich I. A repeated short educational intervention improves asthma control and quality of life. Eur Respir J. 2015;46:1298–307.
Article
CAS
PubMedGoogle Scholar
-
Bell D, Mansfield L, Lomax M, Dissanayake S. Patient handling study of fluticasone propionate/formoterol fumarate pressurized metered-dose inhaler. Respirology. 2014;19:A-O016.
Google Scholar
-
Kuprys-Lipinska I, Wiacek K, Przyrowski R, Kuna P. The educational program on the inhalation technique in a group of patients with asthma and COPD using Aerolizer — the effectiveness and the patients’ satisfaction. J Allergy Clin Immunol. 2011;1:A-443.
Google Scholar
-
Lin HL, Ng SP, Chen CH, Chien SY. Pharmacist-led educational interventions to improve inhalation technique in pediatric asthma patients. Pharmacoepidemiol Drug Saf. 2014;23:A-P414.
Google Scholar
-
Shetty F, Gupta R. Improved MDI inhaler technique observed in adult asthma patients with web based education. Eur Respir J. 2013;42:A-4959.
Google Scholar
-
Takemura M, Mitsui K, Ido M, Koyama M, Matsumoto M, Inoue D, Takamatsu K, Itotani R, Ishitoko M, Suzuki S. Clinical impact of a program to educate community pharmacists in providing proper inhalation technique for asthma patients. Eur Respir J. 2011;38:2845.
-
Maricoto T, Madanelo S, Rodrigues L, Teixeira G, Valente C, Andrade L, Saraiva A. Inhalation technique education and its impact in asthma and COPD. Eur Respir J. 2015;46:A-P5019.
Google Scholar
-
Fernandes L, Mesquita A. Improving asthma control with therapeutic education intervention. Eur Respir J. 2011;38:A-P4997.
Google Scholar
-
Barnestein-Fonseca P, Leiva-Fernández F, Vazquez-Alarcon R, Aguiar-Leiva V, Lobnig-Becerra M, Leiva-Fernández J. Can we improve the inhalation techniques in patients with COPD? Tiepoc study. Value Health. 2015;7:A-PRS10.
Google Scholar
-
Van Der Valk P, Goosens M, Groothuis-Oudshoorn K, Brusse-Keizer M, van der Palen J. Comparing the ease of use, preference and satisfaction of Accuhaler/Diskus and Elpenhaler in patients with asthma or chronic obstructive pulmonary disease. Am J Respir Crit Care Med. 2013;187:A2336.
-
Prieto-Centurion V, Bracken NE, Jaffe HA, Hauser J, Norwick L, Krishnan JA, Zaidi F. Reducing avoidable readmissions following COPD exacerbations among US veterans: the importance of teaching appropriate use of respiratory inhalers. Am J Respir Crit Care Med. 2015;191:A6177.
-
Wiacek K, Kuna P, Kuprys-Lipinska I. The clinical effectiveness of the improvement of the inhalation technique in patients using aerolizer-2nd phase of the educational-observational program. American J Res Crit Care Med. 2012:185, A-5625.
-
Lee S-Y, Park H-W, Song W-J, Cho S-H. A multifaceted approach to reduce acute exacerbations in elderly asthmatics. Chest. 2015;148:A-11A.
Article
Google Scholar
-
Ammari W, Al-Hyari N, Obeidat N, Khater M, Sabouba A, Sanders M. Improving paediatrics’ pressurised metered dose inhaler technique and asthma control: inhaler verbal counselling vs. Trainhaler. Thorax. 2015;70:A-P100.
Article
Google Scholar
-
Ronk J, Alarcon L, Loughlin C. Implementing standardized metered-dose-inhaler (MDI) spacer technique checklist for pediatric asthma patients across University of North Carolina (UNC) Children’s hospital. Am J Respir Crit Care Med. 2012;185:A-3359.
Google Scholar
-
Al-Doghim I. Evaluation of inhalation technique of metered dose inhaler (MDI) and dry powder inhaler-Turbuhaler (DPI) among pediatric patients with asthma. J Appl Sci. 2007;9:53–66.
Google Scholar
-
Khan G, Badri P, Parbati T, Anita D, Atul A, Deepak P, Dipendra R, Himal B, Kabita G, Nirmala K. Intervention on inhalation technique of Rotahaler in patients with chronic obstructive pulmonary disease and asthma. Asian J Pharm Sci. 2016;11:81–2.
Article
Google Scholar
-
Alsomali H, Vines DL, Stein BD, EA B: Evaluating the health literacy and effectiveness of written dry powder inhaler instructions in patients diagnosed with chronic obstructive pulmonary disease. Am Assoc Res Care Open Forum 2015, 60:A-2303288.
-
Benjamin JA, Williams R, Bruce K, Jones O, Philips L. A 2 year programme to improve inhaler technique for adult patients with asthma and chronic obstructive pulmonary disease in a welsh university health board. Eur Respir J. 2015;46:A-P3929.
Google Scholar
-
Sulaiman I, MacHale E, Seheult J, D’Arcy S, Rapcan V, Mokoka M, Cushen B, Killane I, Franciosi A, Sahadevan A. Feedback on adherence and inhaler technique using the Inca device: a randomised control trial in severe asthma. Am J Respir Crit Care Med. 2016;193:A-1714.
Google Scholar
-
Thomas M, Van Der Palen J, Chrystyn H, Zhu C, Ghatta S, Svedsater H. Time to achieve correct inhaler use and inhaler preference: a comparison of Ellipta® with three inhaler devices in patients with asthma. Am J Respir Crit Care Med. 2016;193:A-1739.
Google Scholar
-
Van Der Palen J, Thomas M, Chrystyn H, Sharma R, Imber V, Zhu C-Q, Svedsater H. Training and time to achieve correct inhaler use: a comparison between inhalers in patients with COPD. In: AJRCCM conference. San Francisco, CA, US: American Thoracic Society; 2016. p. A-6812.
Google Scholar
-
Juniper EF, O’Byrne PM, Guyatt GH, Ferrie PJ, King DR. Development and validation of a questionnaire to measure asthma control. Eur Respir J. 1999;14:902–7.
Article
CAS
PubMedGoogle Scholar
-
Nathan RA, Sorkness CA, Kosinski M, Schatz M, Li JT, Marcus P, Murray JJ, Pendergraft TB. Development of the asthma control test: a survey for assessing asthma control. J Allergy Clin Immunol. 2004;113:59–65.
Article
PubMedGoogle Scholar
-
Azevedo P, Correia de Sousa J, Bousquet J, Bugalho-Almeida A, Del Giacco SR, Demoly P, Haahtela T, Jacinto T, Garcia-Larsen V, van der Molen T, et al. Control of allergic rhinitis and asthma test (CARAT): dissemination and applications in primary care. Prim Care Res J. 2013;22:112–6.
Google Scholar
-
Skinner EA, Diette GB, Algatt-Bergstrom PJ, Nguyen TT, Clark RD, Markson LE, AW W. The asthma therapy assessment questionnaire (ATAQ) for children and adolescents. Dis Manag. 2004;7:305–13.
Article
PubMedGoogle Scholar
-
Murphy KR, Zeiger RS, Kosinski M, Chipps B, Mellon M, Schatz M, Lampl K, Hanlon JT, Ramachandran S. Test for respiratory and asthma control in kids (TRACK): a caregiver-completed questionnaire for preschool-aged children. J Allergy Clin Immunol. 2009;123:833–9. e839
Article
PubMedGoogle Scholar
-
Groot EP, Kreggemeijer WJ, Brand PL. Getting the basics right resolves most cases of uncontrolled and problematic asthma. Acta Paediatr. 2015;104:916–21.
Article
PubMedGoogle Scholar
-
Zaidi S, Williams J, Monaghan T, Burhan H, Main N. Inhaler Technique: Does Poor Technique Mean More Admissions? Am J Respir Crit Care Med. 2012;185:A-3333.
Google Scholar
-
Roggeri A, Micheletto C, Boarino S, Inzillo V, Roggeri DP. Potential economic impact of inhalation errors due to device switch in patients with chronic obstructive pulmonary disease and asthma. Value Health. 2015;18:A-PMD147.
Google Scholar
-
Roggeri A, Micheletto C, Roggeri DP. Inhalation errors due to device switch in patients with chronic obstructive pulmonary disease and asthma: critical health and economic issues. Int J Chron Obstruct Pulmon Dis. 2016;11:597–602.
Article
PubMed
PubMed CentralGoogle Scholar
-
Bijos P, Kaczynski J, Torvinen S, Lenarczyk E, Wrona W, Plich A, Lewis A, Blackney M. Clinical and economic burden of asthma and chronic obstructive pulmonary disease (COPD) in Poland: estimated impact of poor inhalation technique with inhaled corticosteroid and long-acting beta agonist fixed-dose combinations. Value Health. 2015;18:A-PRS34.
Article
Google Scholar
-
Torvinen S, Nicolai J, Pulimeno S, di Nola L, Bruno G, Colombo G, Di Matteo S, Valentino M, Lewis A, Blackney M. The budget impact of Duoresp® Spiromax® compared with commonly prescribed dry powder inhalers for the management of asthma and chronic obstructive pulmonary disease in Italy: estimated impact of inhalation technique. Value Health. 2015;18:A-PRS16.
Google Scholar
-
Lewis A, Blackney M, Torvinen S, Plich A. Clinical and economic burden of asthma and chronic obstructive pulmonary disease in the UK: impact of critical inhaler errors with inhaled corticosteroid + long-acting beta agonist fixed-dose combinations. Value Health. 2014;17:A-PRS30.
Article
Google Scholar
-
Lewis A, Blackney M, Garcia BL, Sánchez-de la Rosa R, Torvinen S, Plich A. The potential for improved inhalation technique with Duoresp® Spiromax®(budesonide+formoterol fumarate dihydrate) compared with commonly prescribed dry powder inhalers for the management of asthma and chronic obstructive pulmonary disease in Spain: estimated impact on number and cost of unscheduled healthcare events. Value Health. 2015;18:A-PMD37.
Google Scholar
-
Lewis A, Blackney M, Torvinen S, Lindqvist F, Safioti G, Grundstrom J, Polyzoi M, Plich A. The potential societal cost benefits of improved inhalation technique with Duoresp Spiromax (budesonide + formoterol fumarate dihydrate) compared with Symbicort Turbuhaler for the management of asthma and chronic obstructive pulmonary disease in sweden. Value Health. 2014;17:A-PRS62.
Article
Google Scholar
-
Lewis A, Blackney M, Torvinen S, Holmes J, Osborne M, Dale J, Chandler S, Plich A. The budget impact of Duoresp Spiromax (budesonide + formoterol fumarate dihydrate) compared with Symbicort Turbohaler for the management of asthma and chronic obstructive pulmonary disease in the United Kingdom: impact on health care costs and inhalation technique. Value Health. 2014;17:A-PRS19.
Article
Google Scholar
-
Estrada J, Restrepo A, Serna J, Herrera R, Arrieta J, Segura A. Impact of a pharmacotherapeutic follow-up program on the cost-month-patient, stratified by risk-pharmacological type. Value Health. 2015;18:A-PRS14.
Google Scholar
-
Basheti I, Bosnic-Anticevich S, Armour C, Reddel H. Checklists for powder inhaler technique: a review and recommendations. Respir Care. 2014;59:1140–54.
Article
PubMedGoogle Scholar
-
Basheti IA, Reddel HK, Armour CL, Bosnic-Anticevich SZ. Improved asthma outcomes with a simple inhaler technique intervention by community pharmacists. J Allergy Clin Immunol. 2007;119:1537–8.
Article
PubMedGoogle Scholar
-
Sulaiman I, Seheult J, Sadasivuni N, Cushen B, Mokoka M, Costello R. Inhaler technique errors have an impact on drug delivery. Am J Respir Crit Care Med. 2016;193:A-1715.
Google Scholar
-
Molimard M, Raherison C, Lignot S, Balestra A, Lamarque S, Chartier A, Droz-Perroteau C, Lassalle R, Moore N, Girodet P-O. Chronic obstructive pulmonary disease exacerbation and inhaler device handling: real-life assessment of 2935 patients. Eur Respir J. 2016;49
-
Price DB, Roman-Rodriguez M, McQueen RB, Bosnic-Anticevich S, Carter V, Gruffydd-Jones K, Haughney J, Henrichsen S, Hutton C, Infantino A, et al. Inhaler errors in the CRITIKAL study: type, frequency, and association with asthma outcomes. J Allergy Clin Immunol Pract. 2017;5:1071–1081.e1079.
Article
PubMedGoogle Scholar
-
Williams SA, Wagner S, Kannan H, Bolge SC. The association between asthma control and health care utilization, work productivity loss and health-related quality of life. J Occup Environ Med. 2009;51:780–5.
Article
PubMedGoogle Scholar
-
Vervloet D, Williams A, Lloyd A, Clark T. Costs of managing asthma as defined by a derived asthma control TestTM score in seven European countries. Eur Respir Rev. 2006;15:17–23.
Article
Google Scholar
-
Szende A, Svensson K, Ståhl E, Meszaros A, Berta GY. Psychometric and utility-based measures of health status of asthmatic patients with different disease control level. PharmacoEconomics. 2004;22:537–47.
Article
PubMedGoogle Scholar
-
Doz M, Chouaid C, Com-Ruelle L, Calvo E, Brosa M, Robert J, Decuypere L, Pribil C, Huerta A, Detournay B. The association between asthma control, health care costs, and quality of life in France and Spain. BMC Pulm Med. 2013;13:15.
Article
PubMed
PubMed CentralGoogle Scholar
-
Demoly P, Annunziata K, Gubba E, Adamek L. Repeated cross-sectional survey of patient-reported asthma control in Europe in the past 5 years. Eur Respir Rev. 2012;21:66–74.
Article
CAS
PubMedGoogle Scholar
-
Jha A, Heron L, Marshall J, Dunlop W. Device handling errors and the impact on quality of life and health care resource use in asthmatic patients. Value Health. 2014;17:A-PRS64.
Google Scholar
-
Scichilone N, Benfante A, Bocchino M, Braido F, Paggiaro P, Papi A, Santus P, Sanduzzi A. Which factors affect the choice of the inhaler in chronic obstructive respiratory diseases? Pulm Pharmacol Ther. 2015;31:63–7.
Article
CAS
PubMedGoogle Scholar
-
Lavorini F, Mannini C, Chellini E, Fontana GA. Optimising inhaled pharmacotherapy for elderly patients with chronic obstructive pulmonary disease: the importance of delivery devices. Drugs Aging. 2016;33:461–73.
Article
CAS
PubMedGoogle Scholar
-
Perez L, Morales K, Huang J, Ndicu G, Han X, Klusaritz H, Localio A, Apter AJ. Aspects of asthma self-management: inhaler technique, ability to access (navigate) health care, and inhaled steroid knowledge are correlated. Am J Res Crit Care Med. 2016;193:A6426.
-
Kiser K, Jonas D, Warner Z, Scanlon K, Shilliday BB, DeWalt DA. A randomized controlled trial of a literacy-sensitive self-management intervention for chronic obstructive pulmonary disease patients. The. J Gen Intern Med. 2012;27:190–5.
Article
PubMedGoogle Scholar
-
Paasche-Orlow MK, Riekert KA, Bilderback A, Chanmugam A, Hill P, Rand CS, Brancati FL, Krishnan JA. Tailored education may reduce health literacy disparities in asthma self-management. Am J Respir Crit Care Med. 2005;172:980–6.
Article
PubMed
PubMed CentralGoogle Scholar
-
Al Zabadi H, El Sharif N. Factors associated with frequent emergency room attendance by asthma patients in Palestine. Int J Tuberc Lung Dis. 2007;11:920–7.
CAS
PubMedGoogle Scholar
-
Azouz W, Chetcuti P, Hosker H, Saralaya D, Chrystyn H. Objective measurement of inhalation profiles in patients using metered dose inhalers (MDIs). Eur Respir J. 2011;38:A-838.
Google Scholar
-
Baddar S, Al-Rawas O. What is missing in the asthma control test? The relationship between compliance, inhaler technique and level of control. Eur Respir J. 2012;40:A-P513.
Article
Google Scholar
-
Bilal M, Ahmed A, Shah AR, Mirza HA, Anwar AK, Zaidi SBH. Prevalence of the correct technique of using an inhaler among asthmatic patients reporting in tertiary care hospitals of Rawalpindi, Pakistan. J Allergy Clin Immunol. 2012;1:A-159.
Google Scholar
-
Caliskaner Z, Ozturk C, Pekcan S, Yilmaz O, Ozturk S, Ceylan E, Can C, Sener O, Turay U, Ersoy R. The «extreme» errors in inhaler device use: data from the INTEDA-1 study. In: Allergy; 2011. p. 369–70.
Google Scholar
-
Chrystyn H, Pascual S, Feimer J, De Soyza A, Sauleda Roig J, Haughney J, Padulles L, Seoane B, Rekeda L, Ribera A. Preference, satisfaction and critical errors with Genuair and Breezhaler in patients with COPD. Eur Respir J. 2014;44:A-P928.
Google Scholar
-
Deering B, MacCormack N, Kerrigan K, D’Arcy S, Costello RW. Adherence to inhalers after discharge from hospital following an exacerbation of COPD. Ir J Med Sci. 2013;182:S458.
Google Scholar
-
Hass C, Engdahl K, Albert W, Setyawan J, Mateo N. Patient preferences and perceived ease of use in inhaler features: Genuair vs other inhalers. Chest. 2010;138:A-484.
Article
Google Scholar
-
Herscher M, Ray M, Busse PJ, Wolf MS, Wisnivesky JP, Federman A. Characteristics and outcomes of older adults with early versus late onset asthma. Am J Respir Crit Care Med. 2014;189:A-1359.
Article
CASGoogle Scholar
-
Leiva-Fernandez F, Leiva-Fernandez J, Porcel-Martin C, Prados-Torres D, Garcia-Ruiz AJ, Barnestein-Fonseca P. How do patients with chronic obstructive pulmonary disease (COPD) use their inhalers? Common mistakes. Tecepoc study. Value Health. 2013;16:A-PRS45.
Google Scholar
-
Mazankova D, Mendelova I, Saloun J. Identification of error rate in using inhalation devices by asthmatic patients. Int J Clin Pharm. 2013;35(6):1279–80.
Google Scholar
-
Muhammad I, Haque AS, Muhammad N, Khan JA. Real life perspective in outpatient asthma treatment at a tertiary care center of Pakistan. Respirology. 2009;14:A-PD 10-09.
Google Scholar
-
Santos JC, Silveira BF, Rizzatti F. Knowledge of and technique for using inhalation devices among asthma and COPD patients. Am J Res Crit Care Med. 2014;A-4656
-
Souza M, Meneghini A, Ferraz E, Vianna E, Borges M. Knowledge of and technique for using inhalation devices among asthma patients and COPD patients. J Bras Pneumol. 2009;35:824–31.
Article
PubMedGoogle Scholar
-
Tarsin W, Alshamli I, Soussi M. Preference of the inhaler device and assessment of the technique among the asthmatic and COPD patients. Eur Respir J. 2011;38:A-3981.
Google Scholar
-
Williams J, Mault S, Garner N, Burhan H, Zaidi S. Breaking down bad inhaler technique: device specific advice. Am J Respir Crit Care Med. 2012;185:A-3332.
Google Scholar
Download references
Acknowledgements
We would like to thank Alison Saunders, Iván Viejo Viejo and Rebecca Forster for their support in quality checking and co-ordinating this manuscript and Robin Wyn for editorial assistance.
Funding
Funding was provided by Mundipharma International Ltd. to Adelphi Values Ltd. to support this research and the writing of the manuscript. No financial payment was provided to the individual authors of the review.
Availability of data and materials
The datasets used and/or analysed during the current study are available from the corresponding author on reasonable request.
Trademark
® DISKHALER, DISKUS and ROTAHALER are registered trademarks of Glaxo Group Limited.
® ACCUHALER and EVOHALER are registered trademarks (in the European Union) of Glaxo Group Limited.
® REVOLIZER is a registered trade mark (in the United States) of Cipla Limited.
® AUTOHALER is a registered trade mark of 3 M Company.
® STARHALER is a registered trade mark (in India) of Sun Pharma Laboratories Limited.
® TURBUHALER is a registered trade mark (in the European Union) of AstraZeneca AB.
® HANDIHALER and HandiHaler are registered trademarks of Boehringer Ingelheim Pharma GmbH & Co. KG.
® AEROLIZER is a registered trade mark of Novartis AG.
® GENUAIR is a registered trade mark of AstraZeneca AB.
® BREEZHALER is a registered trade mark (in the European Union) of Novartis AG.
® ELPENHALER is a registered trade mark of Elpen Pharmaceutical Co. Inc.
® CYCLOHALER is a registered trade mark (in the European Union) of Pharmachemie B.V.
® EASI-BREATHE is a registered trade mark (in the European Union) of Norton Healthcare Limited.
® PULVINAL is a registered trade mark (in the European Union) of Chiesi Farmaceutici S.p.A.
® PULMOJET is a registered trade mark (in the European Union) of Sanofi S.A.
Author information
Authors and Affiliations
-
Airway Disease, NHLI, Imperial College London & Royal Brompton Hospital, Dovehouse Street, London, SW3 6LY, UK
Omar Sharif Usmani
-
Department of Experimental and Clinical Medicine, Careggi University Hospital, Florence, Italy
Federico Lavorini
-
Mundipharma International Limited, Cambridge Science Park, Cambridge, CB4 0AB, UK
Jonathan Marshall & William Christopher Nigel Dunlop
-
Adelphi Values, Adelphi Mill, Macclesfield, Cheshire, SK10 5JB, UK
Louise Heron & Emily Farrington
-
Radboud University Medical Center, Nijmegen, Netherlands
Richard Dekhuijzen
Authors
- Omar Sharif Usmani
You can also search for this author in
PubMed Google Scholar - Federico Lavorini
You can also search for this author in
PubMed Google Scholar - Jonathan Marshall
You can also search for this author in
PubMed Google Scholar - William Christopher Nigel Dunlop
You can also search for this author in
PubMed Google Scholar - Louise Heron
You can also search for this author in
PubMed Google Scholar - Emily Farrington
You can also search for this author in
PubMed Google Scholar - Richard Dekhuijzen
You can also search for this author in
PubMed Google Scholar
Contributions
All authors have contributed equally to the analysis, review, writing and finalisation of this manuscript. All authors have read and approved the final manuscript.
Corresponding author
Correspondence to
Omar Sharif Usmani.
Ethics declarations
Ethics approval and consent to participate
Not applicable.
Consent for publication
Not applicable.
Competing interests
In the last 5 years, Omar S. Usmani and/or his department received research grants, unrestricted educational grants, and/or fees for lectures and advisory board meetings from Aerocrine, Astra Zeneca, Boehringer Ingelheim, Chiesi, Cipla, Edmond Pharma, GlaxoSmithKline, Napp, Mundipharma International, Prosonix, Sandoz, Takeda, Zentiva.
In the last 5 years, Federico Lavorini received fees for lectures and advisory board meetings from Astra Zeneca, Boehringer Ingelheim, Chiesi, Cipla, Menarini International, TEVA, Zentiva.
In the last 3 years, Richard Dekhuijzen and/or his department received research grants, unrestricted educational grants, and/or fees for lectures and advisory board meetings from AstraZeneca, Boehringer Ingelheim, Chiesi, GSK, Mundipharma International, Novartis, Takeda and Teva.
William Dunlop and Jonathan Marshall are employees of Mundipharma International Ltd., United Kingdom.
Emily Farrington and Louise Heron are employees of Adelphi Values Ltd., UK. Adelphi Values Ltd. received funding from Mundipharma International Ltd. to support this research.
The authors do not report any conflict of interest with regards to the contents of this study other than those stated.
Publisher’s Note
Springer Nature remains neutral with regard to jurisdictional claims in published maps and institutional affiliations.
Additional file
Additional file 1:
One supplementary file is associated with this manuscript: “Online Resource – Critical handling errors in asthma and COPD: A systematic review of impact on health outcomes”. This contains: search strategies and details of the analysis conducted within this literature review (Table S1); a breakdown of grouped critical errors described in the literature for different inhaler device types (Table S2); summaries of pre-existing known publications that show associations between poor disease control, economic burden and poor QoL (Table S3); definitions of a ‘critical’ error provided by studies captured within the literature review (Table S4). This file is named: “Critical handling errors data supplement update v8_0”. (DOCX 588 kb)
Rights and permissions
Open Access This article is distributed under the terms of the Creative Commons Attribution 4.0 International License (http://creativecommons.org/licenses/by/4.0/), which permits unrestricted use, distribution, and reproduction in any medium, provided you give appropriate credit to the original author(s) and the source, provide a link to the Creative Commons license, and indicate if changes were made. The Creative Commons Public Domain Dedication waiver (http://creativecommons.org/publicdomain/zero/1.0/) applies to the data made available in this article, unless otherwise stated.
Reprints and Permissions
About this article
Cite this article
Usmani, O.S., Lavorini, F., Marshall, J. et al. Critical inhaler errors in asthma and COPD: a systematic review of impact on health outcomes.
Respir Res 19, 10 (2018). https://doi.org/10.1186/s12931-017-0710-y
Download citation
-
Received: 07 September 2017
-
Accepted: 21 December 2017
-
Published: 16 January 2018
-
DOI: https://doi.org/10.1186/s12931-017-0710-y
Keywords
- Obstructive lung diseases
- Adherence
- Errors
- Aerosols
- Inhalers
- Review
- Open Access
- Published: 16 January 2018
- Federico Lavorini2,
- Jonathan Marshall3,
- William Christopher Nigel Dunlop3,
- Louise Heron4,
- Emily Farrington4 &
- …
- Richard Dekhuijzen5
Respiratory Research
volume 19, Article number: 10 (2018)
Cite this article
-
22k Accesses
-
153 Citations
-
129 Altmetric
-
Metrics details
Abstract
Background
Inhaled drug delivery is the cornerstone treatment for asthma and chronic obstructive pulmonary disease (COPD). However, use of inhaler devices can be challenging, potentially leading to critical errors in handling that can significantly reduce drug delivery to the lungs and effectiveness of treatment.
Methods
A systematic review was conducted to define ‘critical’ errors and their impact on health outcomes and resource use between 2004 and 2016, using key search terms for inhaler errors in asthma and COPD (Search-1) and associated health-economic and patient burden (Search-2).
Results
Search-1 identified 62 manuscripts, 47 abstracts, and 5 conference proceedings (n = 114 total). Search-2 identified 9 studies. We observed 299 descriptions of critical error. Age, education status, previous inhaler instruction, comorbidities and socioeconomic status were associated with worse handling error frequency. A significant association was found between inhaler errors and poor disease outcomes (exacerbations), and greater health-economic burden.
Conclusions
We have shown wide variations in how critical errors are defined, and the evidence shows an important association between inhaler errors and worsened health outcomes. Given the negative impact diminished disease outcomes impose on resource use, our findings highlight the importance of achieving optimal inhaler technique, and a need for a consensus on defining critical and non-critical errors.
Background
Inhaled drug delivery is the cornerstone of therapy for the treatment of obstructive chronic airway diseases, such as asthma and chronic obstructive pulmonary disease (COPD) [1]. The most common devices used to administer aerosolized medication in day-to-day respiratory practice are the pressurized metered-dose inhaler (pMDI) and the dry powder inhaler (DPI). pMDIs are most often prescribed [2], but patients need to inhale correctly and coordinate breathing and actuation to ensure effective drug delivery [3,4,5,6]. In contrast, DPIs are breath-actuated, with most devices relying on a rapid and powerful inhalation manoeuvre for drug delivery, which can be particularly problematic for patients who struggle to inhale forcefully [6].
Recent advances in inhaler technologies have seen an explosion in the number of devices [7]. This plethora of devices, however, has led to confusion in their use amongst health-care providers (HCPs) and patients, who may not properly understand how to use inhalers [8]. Indeed, mastering an inhaler device involves correct preparation and handling of the device before inhalation, and an optimal inhalation technique; an error in any step of this process may lead to inadequate drug delivery to the lungs.
There is no one ‘perfect device’ and several studies have shown that inhaler technique errors made by patients with asthma and COPD are common in real life with both pMDIs and DPIs despite advances in inhaler device technology [3, 9,10,11,12]. Although study results vary, estimates of those making inhaler errors range up to 90% of patients irrespective of the device type used [13, 14]. Most importantly, it is vital to distinguish between ‘critical’ (sometimes defined as ‘essential’ or ‘crucial’) errors, which are likely to significantly impair the delivery of adequate medication to the lungs, and ‘non-critical’ errors, which are likely to result in a reduced amount of drug reaching the lungs compared with that attained using the correct technique [15, 16].
A recent major cross-sectional study of asthma patients has compared inhaler technique data with data on disease control, in order to determine which errors are most associated with poor health outcomes [17]. The results of this may provide the most coherent basis for defining and identifying critical errors; however, progress towards fully elucidating these errors is slow.
The societal and health-economic burden of poor inhaler technique is increasingly being recognised [10]. Worryingly, in three countries (the UK, Spain and Sweden) poor inhaler technique accounted for over €750 million in direct and indirect costs in 2015, for the two most commonly used DPIs [18]. These cost data, together with the increasing prevalence of obstructive lung diseases and restriction in healthcare spending is propagating the imperative need for inhaler competency (that is, correct and effective inhaler use) [15].
Recent global position documents from the Global Initiative for Asthma (GINA) and Global Initiative for Chronic Obstructive Lung Disease (GOLD) both give significant prominence to assessing and correcting poor inhalation technique before escalating drug therapy [19, 20].
Price et al. proposed the need for policy change and research focusing on current gaps in knowledge: specifically on the association between device errors and health economic and clinical outcomes, and on the patient characteristics associated with a higher frequency of errors [15]. Indeed, clinicians must recognise that the device itself and its characteristics are at least equally as important as the prescribed drug; and that in future, the choice of drug compound may be considered to be of secondary importance [3].
The aim of this study was to define ‘critical’ errors and their impact on health outcomes and resource use between 2004 and 2016. This was accomplished through systematically reviewing the scientific literature on inhaler errors made by patients when using pMDIs and DPIs, and the approaches used to assess them — exploring the relationships between inhaler errors, disease outcomes, quality of life, and healthcare resource use, and associations between patient characteristics and inhaler errors. Given the striking variety of inhaler errors reported in the literature [11], this paper focuses on critical errors, as these are most likely to have a health impact.
Methods
Overview
This systematic review was undertaken in accordance with the methodological and reporting standards recommended by PRISMA [21], and was registered in the PROSPERO international prospective register of systematic reviews (CRD42016036118). The review consisted of two distinct searches: search-1 focused on definitions and descriptions of critical errors, and search-2 aimed to identify the literature regarding economic models on the cost of critical errors and patient burden (see Additional file 1: Table S1).
Inclusion criteria
Studies from search-1 were included if they reported data on inhaler errors with pMDI and/or DPIs in patients with asthma or COPD, and if they related inhaler technique to disease outcomes or quality of life (QoL). Studies from search-2 were included if they reported data on the patient and/or economic burden of inhaler errors. Soft-mist inhalers and nebulisers were not considered in either search, as pMDIs and DPIs are estimated to make up around 99.8% of the global market share of inhaler devices [22].
Both searches were conducted, reviewed, and each article checked, by two authors (LH, EF) in four online databases (Embase, Medline, EconLIT and Evidence-Based Medicine Reviews), limited to studies published in English between 2004 and May 2016. International conference proceedings from 2013 to 2016 were also scanned (see Additional file 1: Table S1). All the authors reviewed the finalized list of selected articles for approval.
Data extraction
The following data were recorded from each selected article: author and contact details; number of patients; patient characteristics including age, gender, education, comorbidities, socioeconomic class, concurrent device use, and previous instruction; type(s) of inhaler; type(s) of inhaler error(s); definition of critical error(s); type of disease (asthma, COPD, or both); and findings on disease outcomes or QoL.
We grouped the emergent themes into 5 domains in our systematic review; (1) patient characteristics, (2) educational aspects, (3) disease outcomes, (4) quality of life, (5) health economics. This qualitative assessment of the study results allowed results to be reported more clearly, in order to help explore the impact of critical errors on health outcomes and resource use.
When studies were examined for evidence of an association between patient characteristics and presence or rate of inhaler errors, an a priori predefined list of characteristics agreed by consensus between the authors was used to focus analysis. This included: patient age, gender, socioeconomic class, education level, inhaler education, comorbidities, and the number of inhaler devices prescribed at the same time.
Additionally, the reference lists of all retrieved papers were reviewed for any potentially relevant studies, and editorials, commentaries, case studies, letters and opinion pieces were excluded. Studies examining nebuliser inhaler errors or those pooling nebulizer inhaler errors data with data for other inhalers were excluded, as our aim was to assess inhaler devices that administer a single discrete dose. Studies that did not specify inhaler types were included, as it was considered likely that pMDIs and DPIs would have been used, due to these of inhaler types comprising the majority of market share [23]. Descriptive methods were used to analyse data for the associations mentioned above.
Results
Search results
Initially (not including grey literature), Search-1 yielded 114 studies: 62 of these were full-text articles and 52 were abstracts. Of these, five abstracts were identified as having an economics focus and were therefore moved to the results of Search-2 (Fig. 1). Following the addition of five grey literature abstracts, the total yield of Search-1 was again 114 studies.
PRISMA diagram. The database search and analysis in Search-1 initially yielded 114 full-text articles or abstracts; give abstracts were removed and incorporated into the results of Search-2 due to being economics-focused; a further five abstracts were added to Search-1 following the grey literature search. Therefore, the final yield of Search-1 was 114
Full size image
All studies (n = 114) in Search-1 reported inhaler error data on pMDIs with or without spacers, and single- or multiple-dose DPIs (Fig. 2a and b). Study details including population age, respiratory disease, and inhaler device type are presented in Table 1.
a. Journal articles reporting critical inhaler errors for pMDIs and DPIs. Note: percentages are calculated as a proportion of total mentions (n = 105) of each inhaler type by all inhaler error studies. Individual studies may mention more than one inhaler type. b. Journal articles reporting critical inhaler errors for specific DPI device types, both multi-dose (blue) and single-dose (red). Note: percentages are calculated as a proportion of total mentions (n = 65) of all device types by all inhaler error studies. Individual studies may mention more than one inhaler type. c. Studies stating a definition of a critical error, separated into categories. Details of each study and the exact wording used by each are presented in Additional file 1: Table S4. Note: In this figure the term “critical error” refers to both critical errors and critical steps that, when performed incorrectly, constitute critical errors
Full size image
Full size table
Search-2 on the health-economic burden of inhaler errors yielded only one full-text article and three abstracts that fulfilled the inclusion criteria, to which five abstracts from Search-1 were added (Fig. 1).
Definition of critical inhaler errors
Among the 36 studies giving specific examples of ‘critical’ errors, 32 included a definition of ‘critical’ inhaler errors, and the definition itself substantially varied between the studies (Fig. 2c). In most cases, studies did not provide information on the origin of their definition of a critical error; however, where this information was provided, definitions were commonly taken from previous studies, rather than being formulated by the study researchers. Astonishingly, our search yielded 299 descriptions of critical errors across the device types.
The most common definition was an action affecting the lung deposition of inhaled drug, resulting in little or no medicine being inhaled or reaching the lungs (n = 27), where 14 definitions stated a critical error “would” certainly affect inhalation and drug delivery [24,25,26,27,28,29,30,31,32,33,34,35,36,37], and 13 others said a critical error “could” affect these [38,39,40,41,42,43,44,45,46,47,48,49,50]. Conversely, 4 papers defined a critical error in terms of effectiveness: that is, an error that would make aerosol therapy useless [10, 51,52,53]; and Pascual used a combined definition of deposition and effectiveness: that is, “an error that compromised the potential benefit of the treatment, such as impeding drug deposition or the delivery of an insufficient dose” [54].
Surprisingly, only sixty studies (53%) used a checklist to quantify errors and to enable comparisons between devices. However, these checklists were often created by the authors themselves (either taken from previous studies, or were copied from the instructions provided with the inhaler device), without external validation of the checklist itself for each device type. The number of critical errors described varied by device type and by study (Additional file 1: Table S2).
To further compound matters, there were also differences in the descriptions of the actual errors themselves. For example, one DPI error was described in four different ways: two studies mentioned the critical steps which, if not performed, would be errors: “slide lever as far as possible” [42]; “push lever back completely” [27]; and two gave differing terminology for the critical error: “failure to slide the lever until the ‘click’ sound” [51] and “not sliding back the lever until a click is heard” [30]. Similarly, there were also differences in agreement between the authors of the different studies in the categorization of a critical error versus a non-critical error, once again affecting attempts to compare studies and collectively understand the impact of inhaler errors in daily clinical practice. For example, not holding the inhaler upright whilst using a pMDI was referred to as a critical error or step by three studies [39, 42, 44], but Bryant defined it simply as an “error” [55].
While many studies reported associations between characteristics or patient experiences and errors, these did not specify whether associations existed with critical errors specifically, or with all errors.
Effects of patient characteristics on frequency of inhaler errors
Overall, 41 studies of 114 (36%) investigated the effect of predefined patient characteristics on inhaler error frequency (Table 1), with patient age, gender, level of education, number of devices prescribed, and previous inhaler instruction being the most commonly explored factors.
Of 33 studies which examined the effect of patient age [10, 26, 30, 33, 34, 38, 40, 44, 48, 53, 55,56,57,58,59,60,61,62,63,64,65,66,67,68,69,70,71,72,73,74,75,76,77], 29 were in adults and 4 were paediatric. Only twelve studies (36%) reported age to be significantly associated with worsening frequency of inhaler errors [10, 26, 30, 44, 53, 57, 60, 64, 66, 69, 72, 73], whereas 21 studies found no significant association. In 7 studies, older adults were found to make significantly more errors [10, 30, 44, 57, 60, 64, 66]. Of the 4 paediatric studies [26, 40, 53, 74], two reported a significant association between age and frequency of errors: Deerojanawong reported that younger children made errors significantly more frequently [26], while Capanoglu reported the opposite finding: that older children made errors more frequently [53]. Twenty-five studies of 114 (22%) reported on the effects of gender [10, 30, 34, 38, 40, 44, 48, 53, 55, 56, 59,60,61, 63, 65,66,67, 70, 73, 74, 76,77,78,79,80], where 6 studies concluded a significant impact on inhaler error frequency, but the results were contradictory and inconclusive as to whether male or female gender was associated with poor technique [48, 53, 60, 66, 79, 80]. Of the 22 studies that reported a trend between low education and high inhaler error frequency [10, 34, 38, 44, 48, 53, 56, 59,60,61,62, 64,65,66,67, 70, 73,74,75,76, 80, 81], 10 found the association to be statistically significant [10, 34, 48, 53, 56, 60, 62, 66, 73, 80].
Of the 114 articles, 21 studies (18%) explored the relationship between previous inhaler instruction and inhaler error frequency [10, 25, 26, 30, 36, 39, 40, 44, 48, 53, 61, 62, 66,67,68, 71, 72, 74, 76, 80, 81], where 11 studies found previous education or instruction to be significantly related to better inhaler technique [10, 36, 39, 44, 48, 53, 61, 66, 68, 76, 80]. One study by Al-Jahdali reported a significant relationship between ‘lack of education about medication’ and improper device use [67], and two reported that reduced error frequency among previously instructed patients was dependent on device type, where technique improved only in patients using MDI spacer [26] or Diskus or Turbuhaler. [30] Interestingly, a third of studies (n = 7) reported that previous instruction in inhaler use did not significantly affect inhaler technique [25, 40, 62, 71, 72, 74, 81].
Specifically, we noted a statistically significant relationship was reported between increased error frequency and other patient characteristics such as having the presence of two or more comorbidities [56], obesity [48], heart disease [80], cognitive impairment or neuropathy [79], and lower socioeconomic class [56]. There were contradictory results between three studies that reported significant results for whether a higher or lower number of devices prescribed concurrently impacts error frequency [25, 44, 82].
Effects of educational intervention on frequency of inhaler errors
Educational interventions and their relationship to inhaler errors were addressed in 52 articles [27,28,29, 34, 37, 39, 45, 49,50,51, 54, 57,58,59, 61, 83,84,85,86,87,88,89,90,91,92,93,94,95,96,97,98,99,100,101,102,103,104,105,106,107,108,109,110,111,112,113,114,115,116,117,118,119], but studies varied in how errors were assessed (the tools used), by whom (the healthcare personnel), and in the duration of intervention. Interventions were undertaken by face-to-face consultation with a variety of HCPs involving physicians (n = 5), nurses (n = 5), paramedics (n = 1), and pharmacists (n = 8). In other studies, a video (n = 5), leaflet instructions (n = 17), or an online program were used (n = 2). Thirty-two studies undertook patient assessments before and after the educational intervention [29, 34, 39, 45, 51, 57,58,59, 61, 83,84,85,86,87,88,89,90,91,92, 94, 95, 97, 100,101,102,103,104, 108, 109, 114, 115]. Where 26 studies positively reported a significant improvement in inhaler technique following the intervention [29, 34, 39, 51, 57, 58, 61, 83,84,85,86,87,88,89, 92, 94, 95, 97, 101, 103, 104, 108, 109, 114, 115].
Analysis of interventions noted that the majority of the pharmacist-led studies, seven of the eight, demonstrated a statistically significant improvement in inhaler technique [39, 61, 84, 87, 91, 101, 103]. Of the five nurse-led interventions [34, 58, 85, 90, 99], three succeeded in significantly improving inhaler technique [34, 58, 85], and two reported a decrease in inhaler error frequency but did not include a statistical analysis [90, 99]. A further six HCP studies reported statistically significant improvements: three physician-led interventions, a physician-and therapist-led study, GP assistant study and a paramedic-led study all reported statistically significant improvements [57, 83, 89, 92, 94, 97]. Four studies with unspecified instructor types reported improvement [45, 51, 95, 102], but only two provided statistical analysis [51, 95]. Of the leaflet-based intervention studies (n = 17) [27,28,29, 37, 45, 49, 50, 54, 88, 93, 104, 106, 107, 112, 115, 118, 119], five compared inhaler technique before and after the intervention, of which four reported a significant improvement in inhaler technique [29, 88, 104, 115].
Association between disease outcomes and inhaler errors
Thirty-six of the 114 studies (Table 1) examined disease outcomes in relation to inhaler errors or inhalation technique (see Table 2 for a summary of available odds ratios). In the assessment of asthma control, the most common measurements were the Asthma Control Questionnaire (ACQ) and Asthma Control Test (ACT) instruments. [120, 121] Other measurements included: the Control of Allergic Rhinitis and Asthma Test [122], Asthma Therapy Assessment Questionnaire [123], Test For Respiratory And Asthma Control In Kids scales [124], frequency of exacerbations, emergency healthcare use, or general classification of patients into levels of disease control using the Global Initiative for Asthma (GINA) criteria. For COPD patients, disease outcomes were measured by: Baseline Dyspnoea Index (BDI), rates of exacerbations, hospitalizations, or by degree of dyspnoea using the modified Medical Research Council (MRC) questionnaire.
Full size table
Our systematic analysis revealed 10 studies observed a higher inhaler error frequency was significantly associated with poor disease outcomes, primarily in asthma (n = 9), but also in asthma and COPD (n = 1) [10, 38, 48, 53, 56, 57, 67, 78, 90, 97, 117]. Molimard reported that using a device incorrectly, irrespective of the type, was associated with an increased Asthma Control Score [42], and in another study by Kuprys-Lipinska and Wiacek, over 94% of patients reported an association between improved DPI technique and better disease outcomes in asthma and COPD; however, no statistical analysis was provided [100, 109]. Groot reported that incorrect inhaler technique with unspecified inhalers was the underlying cause of poor asthma control in 7.8% of its population, but again did not provide statistical analysis [125].
We identified eight studies where the inhaler training interventions (including such aspects as physical demonstration, technique labels, and written action plans) led to an improvement in inhaler technique and also a significant increase in disease control, (seven in asthma [39, 83, 84, 87, 94, 96, 111], and one in COPD [88]) while 4 studies reported that their intervention significantly improved disease outcomes or reduced hospital admission frequency, but did not measure inhaler error frequency [98, 105, 116, 117]. Two further studies reported that training significantly improved technique and outcomes in asthma, but not in COPD patients [68, 104]. Eight studies reported no significant relationship between poor inhaler technique or errors with asthma control [34, 40, 58, 59, 70, 86, 89, 126].
Association between quality of life and inhaler errors
Seven of the 114 studies examined any association between QoL and inhaler errors: three in asthma, two in COPD and two in a mixed population.
A significant improvement in QoL was reported in three studies, following interventions which improved inhalation technique [84, 88, 91]. Basheti observed a significant correlation between improvement in DPI technique and improvement in asthma-related QoL following a pharmacist-led training intervention [84]. Goris reported significant improvements in QoL according to the St. George’s Respiratory Questionnaire (SGRQ) in all domains of QoL following intervention (aided by a movie and leaflet) in pMDI and DPI technique in COPD patients [88]. Maazuddin reported a pharmacist-led intervention led to significant improvements in the SGRQ outcomes in patients with COPD for pMDI and aerosol based devices including, Autohaler® and Evohaler®, but not for the three DPIs Revolizer®, Rotahaler® and Starhaler® [91].
A further study by Plaza reported a clinically significant increase in Mini Asthma Quality of Life Questionnaire scores among patients receiving a repeated training intervention (including development of a personalised action plan) delivered by a professional educator, physician or nurse, but the inhaler error frequency was not captured [98].
In contrast, an RCT by Hesselink found no significant impact on QoL in asthma and COPD (measured using the Quality-of-Life for Respiratory Illness Questionnaire) following a family practice assistant intervention (involving a structured consultation and use of checklist), although a significant improvement in inhaler technique was recorded [89]. An observational, retrospective study by Takemura reported unchanged SGRQ scores in asthma patients following intervention at regular intervals of at least 6 months by certified participants in a community-pharmacist educational program [103]. A further study by Pothirat captured a non-significant relationship between inhaler errors and poor quality of life, as judged by the by COPD Assessment Test (CAT) [34].
Economic models investigating the costs associated with inhaler errors
Our analysis identified eight studies [127,128,129,130,131,132,133,134,135], of which one was reported both in manuscript and abstract form [127, 128].
Roggeri reported a modelling study conducted in Italy and calculated the increased healthcare resource use by asthma or COPD patients making one or more critical inhaler error and showed this was associated with an additional yearly cost of €44,104 (asthma) or €23,444 (COPD) per 100 patients [127, 128]. Contextualising this for COPD, 100 patients making at least one inhaler error would require 11.5 additional hospitalisations, 13 emergency room visits, 19.5 courses of antimicrobials, and 47 courses of oral corticosteroids, compared to 100 patients not making any critical errors. Corresponding figures for 100 asthma patients were 19 hospitalisations, 26.5 emergency room visits, 4.5 antimicrobial courses and 21.5 oral corticosteroid courses [127, 128].
Bijos modelled the impact of poor inhaler technique on healthcare resource use in Poland, and concluded that misuse of inhaled corticosteroid and long-acting beta agonist fixed-dose combinations resulted in an annual loss of 378 million PLN (€91.1 million) in direct costs and 20.4 million PLN (€4.9 million) in indirect productivity, costs across asthma and COPD [129].
Torvinen calculated the effect on disease outcomes and the economic impact of a new DPI inhaler reported to reduce inhalation errors through innovative inhaler characteristics, and showed a potential saving of €57.78 million, based on a 10.1% rate of uptake among 701,983 patients with persistent asthma or COPD in Italy when switching to the new device from their existing DPI inhalers of Turbuhaler® or Diskus®, by year 5 of the model [130].
In the UK, Lewis considered the impact of inhaler errors on the economic burden of asthma and COPD with inhaled corticosteroid/long-acting beta-agonist (ICS/LABA) fixed-dose combinations [131]. The authors estimated that 366,000 of the 1.3 million persistent asthma/COPD patients within the UK have poor inhalation technique, and that this was associated with 11.8% (£16.2 million) of unscheduled health care events per year [131].
In a further study, Lewis estimated the additional resource use due to poor inhalation technique in Spain, and calculated a loss of €11.54 million due to unscheduled healthcare events among 563,562 asthma and COPD patients using Turbuhaler® or Accuhaler®. [132] Two similar economic models considered the impact of improved inhalation technique in asthma and COPD and in the UK and Sweden, and concluded that improved technique could save £3.5 million in the UK through reducing the number of unscheduled health events (assuming an update of 25% in years 4 and 5 of the model), and SEK285.4 million (€31.2 million) in Sweden by reducing the number of lost working days [133, 134].
Of note, four out of the 9 studies were related to the same device utilised in studies sponsored by the same company within a year of each other using the same health economic model employing a device switch approach to the study design [130, 132,133,134].
Conversely, a real world study in COPD (n = 108) conducted in Colombia reported that making inhaler errors was associated with a minor increase in monthly cost per patient ($146.9, versus $142.2 for other patients) [135].
Interestingly, no economics-focused studies on a US population were captured.
Generic issues identified
As previously mentioned, several types of inconsistency or heterogeneity between captured studies were seen during the review – each of which made the analysis of the data challenging.
The inconsistency in defining critical errors versus normal errors makes drawing conclusions on associations difficult, as errors were considered critical or non-critical by different researchers using different definitions; this is an important issue identified throughout the systematic review.
Furthermore, as differing checklists were used, containing differing numbers and descriptions of errors, error frequencies are likely not completely comparable between studies. In addition, “poor technique” was defined differently by different researchers, who commonly used differing thresholds for labelling a patient’s technique as incorrect or poor [55, 56].
In addition, although disease outcomes were captured using known measures of control, the variety of different measures used does make it more difficult to draw firm conclusions on the association between error frequency and asthma control.
Discussion
The aim of our article was to define ‘critical’ inhaler errors and their impact on health outcomes and resource use; and by doing so, to bring to the attention of physicians the importance of the inhaler device in their daily prescribing in the management of patients with asthma and COPD. Indeed, both GINA and GOLD now highlight the critical importance of assessing inhaler technique to guide appropriate inhaler prescribing, with a concerted drive to educate professionals and patients about the real impact of inhaler errors on the patients’ disease control, as well as on the financial economics of societal health.
To our knowledge this is the first formally registered evidence-based systematic review with a priori clearly formulated questions that documents the wide discrepancies within the literature regarding definitions and descriptions of inhaler errors and their classification as either ‘critical’ or ‘non-critical’. Previous reviews such as that by Basheti et al. focusing on inhaler error checklists have approached these issues [136], although in a different context.
Astonishingly, we observed 299 different descriptions of critical inhaler errors. Even for the same inhaler device type, different terminology was used between different study authors to describe the same inhaler error, and this may contribute to the confusion observed in clinical practice with regards to best inhaler practice and the limitations in determining associations with inhaler errors [8]. This heterogeneity and lack of consensus fundamentally hampers the ability to interpret studies with respect to the impact of inhaler errors. Indeed, the different definitions of critical error could be a contributing factor to extremely different conclusions even with the same inhaler device type; as exemplified in the Melani study where MDI users were significantly less likely to commit critical errors relative to DPI users [10], in contrast to the Batterink study where MDI users were most likely to make critical errors [25].
The lack of consensus between researchers extends to the use of differing inhaler technique checklists. As the checklists used are not standardized, even within individual inhaler device types, comparing error rates between or within inhaler device types is unfeasible. Future research can and should adopt more consistent inhaler technique checklists, as the manufacturers’ instructions are available to form a basis for a checklist in almost all cases.
We observed several important factors, including older age, education status, lack of previous inhaler instruction, and lower socioeconomic class, which were all associated with high inhaler error frequency. In addition, inhaler technique interventions were found to decrease error frequency, and have positive impacts on disease and patient outcomes, as has previously been described in the literature by Basheti et al. [137].
However these findings were not reflected in all studies, likely due to differences in study design and populations. For example, both interventional and observational studies were included, there were different inhaler devices included (i.e. pMDI or DPI), and wide ranging population sizes (between 46 and 6512 individuals), thereby limiting our ability to directly compare the results.
Interestingly, a significant association with error frequency was found for some comorbidities that are known to be strongly correlated with age, such as obesity, heart disease, or cognitive impairment [48, 79, 80]; but despite this, only around a third of studies that examined age itself reported a significant association with error frequency.
Our systematic review identified studies showing an association between inhaler errors and poor asthma control and COPD disease stability. This is in line with a recent individual study that has demonstrated that inhaler errors affect drug delivery [138]. Sulaiman showed in a laboratory environment that deliberately making certain inhaler errors led to a reduced amount of drug reaching the bloodstream [138]. However, the limited quantity of disclosed research in this area may suggest that the term “critical” is being overused, with only a weak basis for categorising errors as such.
In a recent real-world study by Molimard in 2935 patients an increased risk of COPD exacerbation among patients who made a critical inhaler error, was confirmed [139]. A further study by Price determined that the error of “insufficient respiratory effort” was associated with increased asthma exacerbation rate, as well as decreased control in general [140].
Importantly, we identified eight economic models which linked inhaler errors to economic burden, of which one study by Roggeri demonstrated a specific link between critical errors and resource use, leading to an excess cost of many thousands of Euros per 100 patients making critical errors [127, 128]. Indeed, recently Lewis and colleagues showed that poor inhalation technique led to approximately ¾ billion euros in direct and indirect costs for just two DPI inhalers used over 1 year [18].
Previous literature has also demonstrated that poor disease outcomes are linked with worsened QoL and increased resource use and economic burden through increased physician consultation time and lost productivity (Additional file 1: Table S3) [141,142,143,144,145,146]. Therefore, the issue of inhaler errors is important to address due to the downstream effects on patients, healthcare systems and society.
Our findings clearly illustrate inhaler technique can be affected by the level of instruction from HCPs. It is therefore important to interpret clinical trial results with caution, given that their controlled environment (where all patients are instructed in inhaler use) may not be representative of clinical practice in real life. This issue is especially important in the context of different inhaler devices that may have ergonomic designs and functions, as raised by Scichilone et al. in a 2015 review [147]. The key message here is that in day-to-day practice, it may be an efficient strategy to provide patients at higher risk of errors with additional specifically tailored in-depth support with their inhaler use, to ensure they are confident with the correct technique.
Greater attention is clearly needed on the routine review of inhaler technique in the patient population as a whole, as a recent study by Sanchis reported rates of common inhaler errors to be static over a period of several decades [11], and data also show that despite optimally prescribed inhaled therapy, levels of asthma control and COPD disease stability remain poor [18, 145].
In comparison with a previously published systematic review only on DPI inhaler errors, our review encompasses a wider range of device types including the most commonly used inhaler device, the pMDI [14]. Whilst Lavorini et al. included data on critical errors and provided a definition of a critical error, their study focused on the incidence of errors and the possible implications for clinical effectiveness of inhalers [14]. A key strength of our review is that it integrates the link between inhaler errors and disease outcomes and QoL, and provides a systematic overview of how these critical inhaler errors are being assessed and measured.
Direct comparisons and synthesis of the data were challenging due to mixed methodologies (such as observational cross-sectional, or interventional cross-over designs, and designs intended for descriptive or qualitative analysis), different patient populations, and varied endpoints. Yet, despite these differences we observed clear trends in our data. However, due to the vast differences between studies, this review did not examine clinical outcomes by device, but this is an important area for future research.
Furthermore, only a handful of the reviewed studies directly addressed patient outcomes and the economic burden of inhaler errors. Therefore, further research and potential health-economic modelling to understand the relationship between inhaler technique and disease outcomes, and the subsequent impact on societal healthcare systems, is vitally required.
Although the present study shows associations between inhaler errors and patient outcomes through a review of chronic obstructive respiratory diseases as a whole, future research may be able to probe further into the two diseases (asthma and COPD). For example, the generally older age, poor prognosis and comorbidities of COPD patients may influence the degree to which their QoL is increased by improvements in technique and control [148]. The substantially higher prevalence of comorbidities among COPD patients, relative to asthma patients, also likely impacts inhaler technique and patient QoL [148].
With the variety of definitions identified in our review, difficulties arise in determining whether a particular inhaler type is inherently more vulnerable to critical inhaler errors. Consistent use of our proposed definition and categorization by all researchers internationally would transform this area of research and greatly facilitate quantitative and objective comparison between devices, providing a clearer indication of the associated error rates. This would revolutionise everyday clinical practice, where reliable comparisons of error rates would greatly help physicians and aid informed treatment decisions, ensuring the most appropriate device is prescribed for the individual patient with clear implications for personalised patient management. Further research into the association of patient characteristics with error rate could examine “health literacy”, a patient’s insight into their own treatment and health system, and determine if poor knowledge is a risk factor for poor technique [115, 149,150,151].
It is clear that inhaler errors have an effect on disease outcomes, and ultimately patient outcomes and economic burden. This in turn will have an impact on overall disease management and affect not only patients but also the wider healthcare system. These findings are increasingly important given the plethora of devices available to HCPs and patients, and highlight the importance of inhaler mastery in managing and treating asthma and COPD.
There is increasing evidence to suggest that correct inhaler technique (mastery) is fundamental for effective therapy, and that inhaler device type and mastery play important roles in improving adherence, clinical outcomes, quality of life, and use of healthcare resources. Evidence suggests that prescribers should consider patients’ mastery of technique (or lack thereof) and ease of use before changing the dose of inhaled medications, switching to a different inhaler, or adding other treatments to the regimen of patients with poorly controlled asthma. Recent international asthma guidelines highlight the importance of testing and ensuring mastery, alongside checking adherence, before increasing or changing therapy.
Conclusions
In conclusion, the multitude of definitions cited within the literature indicates that there is an urgent need for a consensus in the way in which critical (and non-critical) inhaler errors are defined. We propose defining a critical inhaler error as an action or inaction that in itself would have a definite detrimental impact on the delivery of the drug to the lung, in contrast to a non-critical error which we would define as an action or inaction that in combination with other factors may, or may not, contribute to ineffective delivery of the drug to the lung.
We advocate that there is a real need for an independent international panel of inhalation experts to collectively determine, through evidence and consensus, the definitions of critical and non-critical inhaler errors. If done for each device type, this would demystify the current confusion within the respiratory community.
We also propose that future studies classify individual errors into categories such as inhalation manoeuvre, dose preparation, inhaler handling, device-specific or generic, in order to make comparison and analysis simpler in order to ultimately help healthcare professionals help their patients.
Abbreviations
- ACQ :
-
Asthma Control Questionnaire
- ACT:
-
Asthma Control Test
- ATAQ:
-
Asthma Therapy Assessment Questionnaire
- BDI:
-
Baseline Dyspnoea Index
- CAT:
-
COPD Assessment Test
- CI:
-
Confidence interval
- COPD:
-
Chronic obstructive pulmonary disease
- DPI:
-
Dry-powder inhaler
- GINA :
-
Global Initiative for Asthma
- GOLD:
-
Global Initiative for Chronic Obstructive Lung Disease
- GP:
-
General Practitioner
- HCP:
-
Healthcare provider
- ICS:
-
Inhaled corticosteroid
- LABA:
-
Long-acting beta agonist
- MDI:
-
Metered-dose inhaler
- mMRC:
-
Modified Medical Research Council (questionnaire)
- pMDI:
-
Pressurized metered-dose inhaler
- PRISMA:
-
Preferred Reporting Items for Systematic Reviews and Meta-Analyses
- QoL:
-
quality of life
- RCT:
-
Randomised controlled trial
- SGRQ:
-
St George’s Respiratory Questionnaire
References
-
Gregory KL, Elliott D, Dunne P. Guide to aerosol delivery devices for physicians, nurses, pharmacists and other health care professionals [https://www.aarc.org/wp-content/uploads/2014/08/aerosol_guide_pro.pdf] Accessed: 10 Nov 2015.
-
Pritchard JN. Industry guidance for the selection of a delivery system for the development of novel respiratory products. Expert Opin Drug Deliv. 2015;12:1755–65.
Article
PubMed
CASGoogle Scholar
-
Lavorini F, Usmani OS. Correct inhalation technique is critical in achieving good asthma control. Prim Care Respir J. 2013;22:385–6.
Article
PubMedGoogle Scholar
-
Wright J, Brocklebank D, Ram F. Inhaler devices for the treatment of asthma and chronic obstructive airways disease (COPD). Qual Saf Health Care. 2002;11:376–82.
Article
CAS
PubMed
PubMed CentralGoogle Scholar
-
Price D, Marshall J, Turner R. Inhaler use in five european countries: analysis of sales data from Q4 2005 to Q4 2011. Value Health. 2012;15:A-PMD92.
Google Scholar
-
Price D, Roche N, Christian Virchow J, Burden A, Ali M, Chisholm A, Lee AJ, Hillyer EV, von Ziegenweidt J. Device type and real-world effectiveness of asthma combination therapy: an observational study. Respir Med. 2011;105:1457–66.
Article
PubMedGoogle Scholar
-
Lavorini F, Fontana GA, Usmani OS. New inhaler devices — the good, the bad and the ugly. Respiration. 2014;88:3–15.
Article
PubMedGoogle Scholar
-
Haughney J, Price D, Barnes N, Virchow J, Roche N, Chrystyn H. Choosing inhaler devices for people with asthma: current knowledge and outstanding research needs. Respir Med. 2010;3:125–31.
Google Scholar
-
Molimard M, Raherison C, Lignot S, Depont F, Abouelfath A, Moore N. Assessment of handling of inhaler devices in real life: an observational study in 3811 patients in primary care. J Aerosol Med. 2003;16:249–54.
Article
CAS
PubMedGoogle Scholar
-
Melani AS, Bonavia M, Cilenti V, Cinti C, Lodi M, Martucci P, Serra M, Scichilone N, Sestini P, Aliani M, Neri M. Inhaler mishandling remains common in real life and is associated with reduced disease control. Respir Med. 2011;105:930–8.
Article
PubMedGoogle Scholar
-
Sanchis J, Gich I, Pedersen S. Systematic review of errors in inhaler use: has patient technique improved over time? Chest. 2016;150:394–406.
Article
PubMedGoogle Scholar
-
Molimard M, Raherison C, Lignot S, Balestra A, Lamarque S, Chartier A, Droz-Perroteau C, Lassalle R, Moore N, Girodet PO. Chronic obstructive pulmonary disease exacerbation and inhaler device handling: real-life assessment of 2935 patients. Eur Respir J. 2017;49. doi:10.1183/13993003.01794-2016.
-
Al-Showair RA, Tarsin WY, Assi KH, Pearson SB, Chrystyn H. Can all patients with COPD use the correct inhalation flow with all inhalers and does training help? Respir Med. 2007;101:2395–401.
Article
PubMedGoogle Scholar
-
Lavorini F, Magnan A, Christophe Dubus J, Voshaar T, Corbetta L, Broeders M, Dekhuijzen R, Sanchis J, Viejo JL, Barnes P, et al. Effect of incorrect use of dry powder inhalers on management of patients with asthma and COPD. Respir Med. 2008;102:593–604.
Article
PubMedGoogle Scholar
-
Price D, Bosnic-Anticevich S, Briggs A, Chrystyn H, Rand C, Scheuch G, Bousquet J. Inhaler competence in asthma: common errors, barriers to use and recommended solutions. Respir Med. 2013;107:37–46.
Article
CAS
PubMedGoogle Scholar
-
van der Palen J, Klein JJ, Kerkhoff AH, van Herwaarden CL, Seydel ER. Evaluation of the long-term effectiveness of three instruction modes for inhaling medicines. Patient Educ Couns. 1997;32:S87–95.
Article
CAS
PubMedGoogle Scholar
-
Price DB, Roman-Rodriguez M, RB MQ, Bosnic-Anticevich S, Carter V, Gruffydd-Jones K, Haughney J, Henrichsen S, Hutton C, Infantino A, et al. Inhaler errors in the CRITIKAL study: type, frequency, and association with asthma outcomes. J Allergy Clin Immunol Pract. 2017;5:1071–1081.e1079.
Article
PubMedGoogle Scholar
-
Lewis A, Torvinen S, Dekhuijzen PN, Chrystyn H, Watson AT, Blackney M, Plich A. The economic burden of asthma and chronic obstructive pulmonary disease and the impact of poor inhalation technique with commonly prescribed dry powder inhalers in three European countries. BMC Health Serv Res. 2016;16:251.
Article
CAS
PubMed
PubMed CentralGoogle Scholar
-
Global initiative for chronic obstructive lung disease: pocket guide to COPD diagnosis, management and prevention [http://goldcopd.org/wp-content/uploads/2016/12/wms-GOLD-2017-Pocket-Guide.pdf] Accessed: 26 May 2017.
-
Global initiative for asthma: pocket guide for asthma management and prevention [http://ginasthma.org/2017-pocket-guide-for-asthma-management-and-prevention/] Accessed: 25 July 2017.
-
Liberati A, Altman DG, Tetzlaff J, Mulrow C, Gøtzsche PC, Ioannidis JPA, Clarke M, Devereaux PJ, Kleijnen J, Moher D. The PRISMA statement for reporting systematic reviews and meta-analyses of studies that evaluate healthcare interventions: explanation and elaboration. Br Med J. 2009;339:b2700.
-
IMS Health: IMS MIDAS Q4 MAT 2016, EU5. 2016.
Google Scholar
-
Lavorini F, Corrigan CJ, Barnes PJ, Dekhuijzen PR, Levy ML, Pedersen S, Roche N, Vincken W, Crompton GK. Aerosol drug management improvement team: retail sales of inhalation devices in European countries: so much for a global policy. Respir Med. 2011;105:1099–103.
Article
CAS
PubMedGoogle Scholar
-
Basheti IA, Qunaibi E, Bosnic-Anticevich SZ, Armour CL, Khater S, Omar M, Reddel HK. User error with diskus and turbuhaler by asthma patients and pharmacists in Jordan and Australia. Respir Care. 2011;56:1916–23.
Article
PubMedGoogle Scholar
-
Batterink J, Dahri K, Aulakh A, Rempel C. Evaluation of the use of inhaled medications by hospital inpatients with chronic obstructive pulmonary disease. Can J Hosp Pharm. 2012;65:111–8.
PubMed
PubMed CentralGoogle Scholar
-
Deerojanawong J, Na Sakolnakorn VP, Prapphal N, Hanrutakorn C, Sritippayawan S. Evaluation of metered-dose inhaler administration technique among asthmatic children and their caregivers in Thailand. Asian Pac J Allergy Immunol. 2009;27:87–93.
PubMed
Google Scholar
-
Van Der Palen J, Van Der Valk P, Goosens M, Groothuis-Oudshoorn K, Brusse-Keizer M. A randomised cross-over trial investigating the ease of use and preference of two dry powder inhalers in patients with asthma or chronic obstructive pulmonary disease. Expert Opin Drug Deliv. 2013;10:1171–8.
Article
PubMedGoogle Scholar
-
Van Der Palen J, Ginko T, Kroker A, Van Der Valk P, Goosens M, Padulles L, Seoane B, Rekeda L, Garcia Gil E. Preference, satisfaction and errors with two dry powder inhalers in patients with COPD. Expert Opin Drug Deliv. 2013;10:1023–31.
Article
PubMedGoogle Scholar
-
Voshaar T, Spinola M, Linnane P, Campanini A, Lock D, Lafratta A, Scuri M, Ronca B, Melani AS. Comparing usability of NEXThaler with other inhaled corticosteroid/long-acting beta2-agonist fixed combination dry powder inhalers in asthma patients. J Aerosol Med Pulm Drug Deliv. 2014;27:363–70.
Article
CAS
PubMed
PubMed CentralGoogle Scholar
-
Wieshammer S, Dreyhaupt J. Dry powder inhalers: which factors determine the frequency of handling errors? Respiration. 2008;75:18–25.
Article
PubMedGoogle Scholar
-
Capstick T, Clifton I, Morgan J, Silcock J, Blenkinsopp A. Inhaler technique: an unmet need in patients with difficult asthma? Eur Respir J. 2013;42:A-4893.
Google Scholar
-
Nama S, Percival M, Harris M, Nolan-Neylan S, Sivakumaran P, Sriram K, Harland K. Evaluation of inhaler technique and medication adherence in COPD patients. Respirology. 2014;19:A-TP146.
Google Scholar
-
Vanderman AJ, Moss JM, Bailey JC, Melnyk SD, Brown JN. Inhaler misuse in an older adult population. Consult Pharm. 2015;30:92–100.
Article
PubMedGoogle Scholar
-
Pothirat C, Chaiwong W, Phetsuk N, Pisalthanapuna S, Chetsadaphan N, Choomuang W. Evaluating inhaler use technique in COPD patients. Int J Chron Obstruct Pulmon Dis. 2015;10:1291–8.
Article
CAS
PubMed
PubMed CentralGoogle Scholar
-
Madkour A, Galal I. Do Egyptian patients use their inhalers correctly? A checklist auditing for inhalation devices usage techniques. Egyptian J Chest Dis Tuberculosis. 2015;64:497–504.
Article
Google Scholar
-
Ozturk C, Aldag Y. Evaluation and importance of different types of inhaler device use in patients with chronic obstructive lung disease (COPD). Respirology. 2015;20(S3):A-471.
-
Chrystyn H, Price DB, Molimard M, Haughney J, Bosnic-Anticevich S, Lavorini F, Efthimiou J, Shan D, Sims E, Burden A. Comparison of serious inhaler technique errors made by device-naïve patients using three different dry powder inhalers: a randomised, crossover, open-label study. BMC Pulm Med. 2016;16:12.
Article
PubMed
PubMed Central
CASGoogle Scholar
-
Coelho ACC, Souza-Machado A, Leite M, Almeida P, Castro L, Cruz CS, Stelmach R, Cruz AA. Use of inhaler devices and asthma control in severe asthma patients at a referral center in the city of Salvador, Brazil. J Bras Pneumol. 2011;37:720–8.
Article
PubMedGoogle Scholar
-
Giraud V, Allaert FA, Roche N. Inhaler technique and asthma: Feasability and acceptability of training by pharmacists. Respir Med. 2011;105:1815–22.
Article
PubMedGoogle Scholar
-
Hagmolen of ten Have W, van de Berg NJ, Bindels PJ, van Aalderen WM, van der Palen J. Assessment of inhalation technique in children in general practice: increased risk of incorrect performance with new device. J Asthma. 2008;45:67–71.
Article
PubMedGoogle Scholar
-
Mehuys E, Boussery K, Adriaens E, van Bortel L, De Bolle L, van Tongelen I, Remon JP, Brusselle G. COPD management in primary care: an observational, community pharmacy-based study. Ann Pharmacother. 2010;44:257–66.
Article
PubMedGoogle Scholar
-
Molimard M, Gros VL. Impact of patient-related factors on asthma control. J Asthma. 2008;45:109–13.
Article
PubMedGoogle Scholar
-
Rajan S, Gogtay J. Ease-of-use, preference, confidence, and satisfaction with Revolizer, a novel dry powder inhaler, in an Indian population. Lung India. 2014;31:366–74.
Article
PubMed
PubMed CentralGoogle Scholar
-
Rootmensen G, Van Keimpema AR, Jansen HM, De Haan RJ. Predictors of incorrect inhalation technique in patients with asthma or COPD. Am J Respir Crit Care Med. 2010;181:A-3812.
Google Scholar
-
Schulte M, Osseiran K, Betz R, Wencker M, Brand P, Meyer T, Haidl P. Handling of and preferences for available dry powder inhaler systems by patients with asthma and COPD. J Aerosol Med Pulm Drug Deliv. 2008;21:321–8.
Article
CAS
PubMedGoogle Scholar
-
Van Der Palen J, Ginko T, Kroker A, Van Der Valk P, Goosens M, Padulles L, Seoane B, Rekeda L, Gil EG. Comparison of the preference, satisfaction, and critical errors made with Genuair and Handihaler in patients with COPD. Chest. 2012;142:A-717A.
Article
Google Scholar
-
Molimard M. How to achieve good compliance and adherence with inhalation therapy. Curr Med Res Opin. 2005;21:S33–7.
Article
PubMedGoogle Scholar
-
Westerik JA, Carter V, Chrystyn H, Burden A, Thompson SL, Ryan D, Gruffydd-Jones K, Haughney J, Roche N, Lavorini F, et al. Characteristics of patients making serious inhaler errors with a dry powder inhaler and association with asthma-related events in a primary care setting. J Asthma. 2016;53:321–9.
Article
PubMed
PubMed CentralGoogle Scholar
-
Chrystyn H, Bosnic-Anticevich S, Roche N, Molimard M, Haughney J, Lavorini F, Shan D, Sims E, Burden A, Ashton VL. Prevalence of serious post-training inhaler technique errors made by device-naïve patients using three different dry powder inhalers (DPIs). Eur Respir J. 2015;46:A-P3927.
Google Scholar
-
Thomas M, Van der Palen J, Chrystyn H, Sharma R, Imber V, Zhu C-Q, Barnes N. Inhaler errors and preference: a comparison of two multi-dose powder asthma inhalers. Respirology. 2015;20:A-573.
Article
Google Scholar
-
Li H, Chen Y, Zhang Z, Dong X, Zhang G, Zhang H. Handling of diskus dry powder inhaler in Chinese chronic obstructive pulmonary disease patients. J Aerosol Med Pulm Drug Deliv. 2014;27:219–27.
Article
PubMedGoogle Scholar
-
Melani AS, Canessa P, Coloretti I, Deangelis G, Detullio R, Del Donno M, Giacobbe R, Scarlato I, Serafini A, Barbato N, et al. Inhaler mishandling is very common in patients with chronic airflow obstruction and long-term home nebuliser use. Respir Med. 2012;106:668–76.
Article
PubMedGoogle Scholar
-
Capanoglu M, Dibek Misirlioglu E, Toyran M, Civelek E, Kocabas CN. Evaluation of inhaler technique, adherence to therapy and their effect on disease control among children with asthma using metered dose or dry powder inhalers. J Asthma. 2015;52:838–45.
Article
PubMed
CASGoogle Scholar
-
Pascual S, Feimer J, De Soyza A, Sauleda Roig J, Haughney J, Padulles L, Seoane B, Rekeda L, Ribera A, Chrystyn H. Preference, satisfaction and critical errors with Genuair and Breezhaler inhalers in patients with COPD: a randomised, cross-over, multicentre study. NPJ Prim Care Respir Med. 2015;25:15018.
Article
PubMed
PubMed CentralGoogle Scholar
-
Bryant L, Bang C, Chew C, Hee Baik S, Wiseman D. Adequacy of inhaler technique used by people with asthma or chronic obstructive pulmonary disease. JJ Prim Health Care. 2013;5:191–8.
Google Scholar
-
Dalcin PTR, Grutcki DM, Laporte PP, de Lima PB, Menegotto SM, Pereira RP. Factors related to the incorrect use of inhalers by asthma patients. J Bras Pneumol. 2014;40:13–20.
Article
PubMed CentralGoogle Scholar
-
Giraud V, Allaert FA, Magnan A. A prospective observational study of patient training in use of the autohaler inhaler device: the sirocco study. Eur Rev Med Pharmacol Sci. 2011;15:563–70.
CAS
PubMedGoogle Scholar
-
Harnett CM, Hunt EB, Bowen BR, O’Connell OJ, Edgeworth DM, Mitchell P, Eustace JA, Henry MT, Kennedy MP, Plant BJ, Murphy DM. A study to assess inhaler technique and its potential impact on asthma control in patients attending an asthma clinic. J Asthma. 2014;51:440–5.
Article
CAS
PubMedGoogle Scholar
-
Loh LC, Teng CL, Teh PN, Koh CN, Vijayasingham P, Thayaparan T. Metered-dose inhaler technique in asthmatic patients — a revisit of the Malaysian scene. Med J Malaysia. 2004;59:335–41.
CAS
PubMedGoogle Scholar
-
Chorao P, Pereira AM, Fonseca JA. Inhaler devices in asthma and COPD — an assessment of inhaler technique and patient preferences. Respir Med. 2014;108:968–75.
Article
PubMedGoogle Scholar
-
Hammerlein A, Muller U, Schulz M. Pharmacist-led intervention study to improve inhalation technique in asthma and COPD patients. J Eval Clin Pract. 2011;17:61–70.
Article
PubMedGoogle Scholar
-
Al-Hassan MI. Assessment of inhaler technique in patients attending a chest hospital in Riyadh City. Int J Pharmacol. 2009;5:232–5.
Article
Google Scholar
-
Komase Y, Asako A, Kobayashi A, Sharma R. Ease-of-use preference for the ELLIPTA dry powder inhaler over a commonly used single-dose capsule dry powder inhaler by inhalation device-naive Japanese volunteers aged 40 years or older. Int J COPD. 2014;9:1365–75.
Article
Google Scholar
-
Ozturk C, Kaya A, Bilgin C, Yucesoy L, Ikidag B, Demirel M, Baslilar S, Saylan B, Senol T, Aganoglu S, et al. Evaluation of inhaler technique and patient satisfaction with fixed-combination budesonide/formoterol dry-powder inhaler in chronic obstructive pulmonary disease (COPD): data on real-life clinical practice in Turkey. Tuberk Toraks. 2012;60:301–13.
Article
PubMedGoogle Scholar
-
Nolan-Neylan S, Harris M, Harland K, Sriram K. Evaluation of inhaler technique in hospitalised COPD patients. Respirology. 2015;20:A-P002.
Google Scholar
-
Lee SM, Chang YS, Kim CW, Kim TB, Kim SH, Kwon YE, Lee JM, Lee SK, Jeong JW, Park JW, et al. Skills in handling Turbuhaler, Diskus, and pressurized metered-dose inhaler in Korean asthmatic patients. Allergy Asthma Immunol Res. 2010;3:46–52.
Article
PubMed
PubMed CentralGoogle Scholar
-
Al-Jahdali H, Ahmed A, Al-Harbi A, Khan M, Baharoon S, Bin Salih S, Halwani R, Al-Muhsen S. Improper inhaler technique is associated with poor asthma control and frequent emergency department visits. Allergy Asthma Clin Immunol. 2013;9:8.
Article
PubMed
PubMed CentralGoogle Scholar
-
Maricoto T, Rodrigues LV, Teixeira G, Valente C, Andrade L, Saraiva A. Assessment of inhalation technique in clinical and functional control of asthma and chronic obstructive pulmonary disease. Acta Med Port. 2015;28:702–7.
Article
PubMedGoogle Scholar
-
Manriquez P, Acuna AM, Munoz L, Reyes A. Study of inhaler technique in asthma patients: differences between pediatric and adult patients. J Bras Pneumol. 2015;41:405–9.
Article
PubMed
PubMed CentralGoogle Scholar
-
Sriram KB, Percival M. Suboptimal inhaler medication adherence and incorrect technique are common among chronic obstructive pulmonary disease patients. Chron Respir Dis. 2015;13:13–22.
Article
PubMed
PubMed CentralGoogle Scholar
-
Buset EMN, Liaaen ED, Roth K, Blix HS. Inhalation technique in hospitalized asthma and COPD patients: should patients be regularly assessed before discharge? Int J Clin Pharm. 2015;37:A-16.
Google Scholar
-
Cayo-Quiñe A, Martínez-Vargas V, Bustamante-Voysest R, Piscoya A, Alberca Y: Incorrect use of metered-dose inhalers in adult patients at a hospital in Callao, Peru, 2014: cross-sectional study. Medwave 2014, 15:e6163-e6163.
-
Sangita P, Gharti KP, Laxman B. Assessment of inhalation techniques in COPD patients using metered-dose inhaler and Rotahaler at a tertiary care hospital in Nepal. Int Res J Pharm. 2015;6:288–93.
Article
Google Scholar
-
Villamil-Osorio M, Medina L, Pernett L, Restrepo SM, Nino G, Rodriguez-Martinez C. Assessment of inhalation technique and predictors of poor inhalation technique in a population of asthmatic children. J Aerosol Med Pulm Drug Deliv. 2015;191:A-3370.
Google Scholar
-
Udwadia ZZ, Kathar S, Shah HD, Pandey K, Rastogi S, Mullerpattan J. Who will teach the teachers: an analysis of the inhaler technique of Indian patients and health care providers. Am J Res Crit Care Med. 2013;187:A5026.
-
Turan P, Itil O, Turan M. Factors effecting inhaler technique in COPD. Am J Res Crit Care Med. 2014;189:A-6000.
-
Wu H, Thomas L, Bime C. An assessment of inhaler technique among patients with chronic obstructive airway diseases in a health professional shortage area. Am Philos Soc. 2013;187:A4208.
-
Baddar S, Jayakrishnan B, Al-Rawas OA. Asthma control: importance of compliance and inhaler technique assessments. J Asthma. 2014;51:429–34.
Article
PubMedGoogle Scholar
-
Sadowski C, Banh H, Cor K, Cave A. Inhaler device technique in community-dwelling older adults. Canadian Journal of. Hosp Pharm. 2013;66(4):269.
Google Scholar
-
Camilleri K, Balzan M, Bardon MP, Schembri E, Sullivan M, Mifsud S, Muscat D, Asciaq R, Montefort S. Predictors of good inhaler technique in asthma and COPD. Eur Respir J. 2015;46:A-P3928.
Google Scholar
-
Ganguly A, Das A, Roy A, Adhikari A, Banerjee J, Sen S. Study of proper use of inhalational devices by bronchial asthma or copd patients attending a tertiary care hospital. J Clin Diagn Res. 2014;8:HC04–7.
PubMed
PubMed CentralGoogle Scholar
-
Khassawneh BY, Al-Ali MK, Alzoubi KH, Batarseh MZ, Al-Safi SA, Sharara AM, Alnasr HM. Handling of inhaler devices in actual pulmonary practice: metered-dose inhaler versus dry powder inhalers. Respir Care. 2008;53:324–8.
PubMed
Google Scholar
-
Barthwal MS, Katoch CDS, Marwah V. Impact of optimal asthma education programme on asthma morbidity, inhalation technique and asthma knowledge. J Assoc Physicians India. 2009;57:574–9.
CAS
PubMedGoogle Scholar
-
Basheti IA, Armour CL, Bosnic-Anticevich SZ, Reddel HK. Evaluation of a novel educational strategy, including inhaler-based reminder labels, to improve asthma inhaler technique. Patient Educ Couns. 2008;72:26–33.
Article
PubMedGoogle Scholar
-
Burkhart PV, Rayens MK, Bowman RK. An evaluation of children’s metered-dose inhaler technique for asthma medications. Nurs Clin N Am. 2005;40:167–82.
Article
Google Scholar
-
Carpenter DM, Lee C, Blalock SJ, Weaver M, Reuland D, Coyne-Beasley T, Mooneyham R, Loughlin C, Geryk LL, Sleath BL. Using videos to teach children inhaler technique: a pilot randomized controlled trial. J Asthma. 2015;52:81–7.
Article
PubMedGoogle Scholar
-
Garcia-Cardenas V, Sabater-Hernandez D, Kenny P, Martinez-Martinez F, Faus MJ, Benrimoj SI. Effect of a pharmacist intervention on asthma control. A cluster randomised trial. Respir Med. 2013;107:1346–55.
Article
PubMedGoogle Scholar
-
Goris S, Tasci S, Elmali F. The effects of training on inhaler technique and quality of life in patients with COPD. J Aerosol Med Pulm Drug Deliv. 2013;26:336–44.
Article
PubMed
CASGoogle Scholar
-
Hesselink AE, Penninx BWJH, Van Der Windt DAWM, Van Duin BJ, De Vries P, Twisk JWR, Bouter LM, Van Eijk JTM. Effectiveness of an education programme by a general practice assistant for asthma and COPD patients: results from a randomised controlled trial. Patient Educ Couns. 2004;55:121–8.
Article
PubMedGoogle Scholar
-
Levy ML, Hardwell A, McKnight E, Holmes J. Asthma patients’ inability to use a pressurised metered-dose inhaler (pMDI) correctly correlates with poor asthma control as defined by the global initiative for asthma (GINA) strategy: a retrospective analysis. Prim Care Res J. 2013;22:406–11.
Google Scholar
-
Maazuddin M, Hazari MAH, Hasan A, Javeedullah M, Nasir Mohiuddin M, Baig MMA. Training in the use of inhalation devices and respiratory improvement in asthma and COPD patients: a before-after experimental study. Pharmanest. 2014;5:2314–20.
Google Scholar
-
Minai BA, Martin JE, Cohn RC. Results of a physician and respiratory therapist collaborative effort to improve long-term metered-dose inhaler technique in a pediatric asthma clinic. Respir Care. 2004;49:600–5.
PubMed
Google Scholar
-
Van Der Palen J, Eijsvogel MM, Kuipers BF, Schipper M, Vermue NA. Comparison of the Diskus inhaler and the Handihaler regarding preference and ease of use. J Aerosol Med. 2007;20:38–44.
Article
PubMedGoogle Scholar
-
Yildiz F, Erbagci A, Demirel YS, Akcali SD, Ekici A, Dursunoglu N, Ediger D, Erdinc M, Cemri SC, Kalyoncu AF, et al. Importance of inhaler device use status in the control of asthma in adults: the asthma inhaler treatment study. Respir Care. 2014;59:223–30.
Article
PubMedGoogle Scholar
-
Elgendy MO, Abdelrahim ME, Eldin RS. Potential benefit of repeated MDI inhalation technique counselling for patients with asthma. Eur J Hosp Pharm. 2015;22:318–22.
Article
Google Scholar
-
Grover C, Goel N, Armour C, Van Asperen P, Gaur S, Moles R, Saini B. Medication education program for Indian children with asthma: a feasibility study. Niger J Clin Pract. 2016;19:76–84.
Article
CAS
PubMedGoogle Scholar
-
Kuna P, Kupryś-Lipińska I, Dębowski T. Control of asthma in adults treated with beclomethasone and formoterol in extrafine particle formulation in a real-life setting in Poland: the CASPER noninterventional, observational trial. Pol Arch Med Wewn. 2015;125:731–40.
PubMed
Google Scholar
-
Plaza V, Peiró M, Torrejón M, Fletcher M, López-Viña A, Ignacio JM, Quintano JA, Bardagí S, Gich I. A repeated short educational intervention improves asthma control and quality of life. Eur Respir J. 2015;46:1298–307.
Article
CAS
PubMedGoogle Scholar
-
Bell D, Mansfield L, Lomax M, Dissanayake S. Patient handling study of fluticasone propionate/formoterol fumarate pressurized metered-dose inhaler. Respirology. 2014;19:A-O016.
Google Scholar
-
Kuprys-Lipinska I, Wiacek K, Przyrowski R, Kuna P. The educational program on the inhalation technique in a group of patients with asthma and COPD using Aerolizer — the effectiveness and the patients’ satisfaction. J Allergy Clin Immunol. 2011;1:A-443.
Google Scholar
-
Lin HL, Ng SP, Chen CH, Chien SY. Pharmacist-led educational interventions to improve inhalation technique in pediatric asthma patients. Pharmacoepidemiol Drug Saf. 2014;23:A-P414.
Google Scholar
-
Shetty F, Gupta R. Improved MDI inhaler technique observed in adult asthma patients with web based education. Eur Respir J. 2013;42:A-4959.
Google Scholar
-
Takemura M, Mitsui K, Ido M, Koyama M, Matsumoto M, Inoue D, Takamatsu K, Itotani R, Ishitoko M, Suzuki S. Clinical impact of a program to educate community pharmacists in providing proper inhalation technique for asthma patients. Eur Respir J. 2011;38:2845.
-
Maricoto T, Madanelo S, Rodrigues L, Teixeira G, Valente C, Andrade L, Saraiva A. Inhalation technique education and its impact in asthma and COPD. Eur Respir J. 2015;46:A-P5019.
Google Scholar
-
Fernandes L, Mesquita A. Improving asthma control with therapeutic education intervention. Eur Respir J. 2011;38:A-P4997.
Google Scholar
-
Barnestein-Fonseca P, Leiva-Fernández F, Vazquez-Alarcon R, Aguiar-Leiva V, Lobnig-Becerra M, Leiva-Fernández J. Can we improve the inhalation techniques in patients with COPD? Tiepoc study. Value Health. 2015;7:A-PRS10.
Google Scholar
-
Van Der Valk P, Goosens M, Groothuis-Oudshoorn K, Brusse-Keizer M, van der Palen J. Comparing the ease of use, preference and satisfaction of Accuhaler/Diskus and Elpenhaler in patients with asthma or chronic obstructive pulmonary disease. Am J Respir Crit Care Med. 2013;187:A2336.
-
Prieto-Centurion V, Bracken NE, Jaffe HA, Hauser J, Norwick L, Krishnan JA, Zaidi F. Reducing avoidable readmissions following COPD exacerbations among US veterans: the importance of teaching appropriate use of respiratory inhalers. Am J Respir Crit Care Med. 2015;191:A6177.
-
Wiacek K, Kuna P, Kuprys-Lipinska I. The clinical effectiveness of the improvement of the inhalation technique in patients using aerolizer-2nd phase of the educational-observational program. American J Res Crit Care Med. 2012:185, A-5625.
-
Lee S-Y, Park H-W, Song W-J, Cho S-H. A multifaceted approach to reduce acute exacerbations in elderly asthmatics. Chest. 2015;148:A-11A.
Article
Google Scholar
-
Ammari W, Al-Hyari N, Obeidat N, Khater M, Sabouba A, Sanders M. Improving paediatrics’ pressurised metered dose inhaler technique and asthma control: inhaler verbal counselling vs. Trainhaler. Thorax. 2015;70:A-P100.
Article
Google Scholar
-
Ronk J, Alarcon L, Loughlin C. Implementing standardized metered-dose-inhaler (MDI) spacer technique checklist for pediatric asthma patients across University of North Carolina (UNC) Children’s hospital. Am J Respir Crit Care Med. 2012;185:A-3359.
Google Scholar
-
Al-Doghim I. Evaluation of inhalation technique of metered dose inhaler (MDI) and dry powder inhaler-Turbuhaler (DPI) among pediatric patients with asthma. J Appl Sci. 2007;9:53–66.
Google Scholar
-
Khan G, Badri P, Parbati T, Anita D, Atul A, Deepak P, Dipendra R, Himal B, Kabita G, Nirmala K. Intervention on inhalation technique of Rotahaler in patients with chronic obstructive pulmonary disease and asthma. Asian J Pharm Sci. 2016;11:81–2.
Article
Google Scholar
-
Alsomali H, Vines DL, Stein BD, EA B: Evaluating the health literacy and effectiveness of written dry powder inhaler instructions in patients diagnosed with chronic obstructive pulmonary disease. Am Assoc Res Care Open Forum 2015, 60:A-2303288.
-
Benjamin JA, Williams R, Bruce K, Jones O, Philips L. A 2 year programme to improve inhaler technique for adult patients with asthma and chronic obstructive pulmonary disease in a welsh university health board. Eur Respir J. 2015;46:A-P3929.
Google Scholar
-
Sulaiman I, MacHale E, Seheult J, D’Arcy S, Rapcan V, Mokoka M, Cushen B, Killane I, Franciosi A, Sahadevan A. Feedback on adherence and inhaler technique using the Inca device: a randomised control trial in severe asthma. Am J Respir Crit Care Med. 2016;193:A-1714.
Google Scholar
-
Thomas M, Van Der Palen J, Chrystyn H, Zhu C, Ghatta S, Svedsater H. Time to achieve correct inhaler use and inhaler preference: a comparison of Ellipta® with three inhaler devices in patients with asthma. Am J Respir Crit Care Med. 2016;193:A-1739.
Google Scholar
-
Van Der Palen J, Thomas M, Chrystyn H, Sharma R, Imber V, Zhu C-Q, Svedsater H. Training and time to achieve correct inhaler use: a comparison between inhalers in patients with COPD. In: AJRCCM conference. San Francisco, CA, US: American Thoracic Society; 2016. p. A-6812.
Google Scholar
-
Juniper EF, O’Byrne PM, Guyatt GH, Ferrie PJ, King DR. Development and validation of a questionnaire to measure asthma control. Eur Respir J. 1999;14:902–7.
Article
CAS
PubMedGoogle Scholar
-
Nathan RA, Sorkness CA, Kosinski M, Schatz M, Li JT, Marcus P, Murray JJ, Pendergraft TB. Development of the asthma control test: a survey for assessing asthma control. J Allergy Clin Immunol. 2004;113:59–65.
Article
PubMedGoogle Scholar
-
Azevedo P, Correia de Sousa J, Bousquet J, Bugalho-Almeida A, Del Giacco SR, Demoly P, Haahtela T, Jacinto T, Garcia-Larsen V, van der Molen T, et al. Control of allergic rhinitis and asthma test (CARAT): dissemination and applications in primary care. Prim Care Res J. 2013;22:112–6.
Google Scholar
-
Skinner EA, Diette GB, Algatt-Bergstrom PJ, Nguyen TT, Clark RD, Markson LE, AW W. The asthma therapy assessment questionnaire (ATAQ) for children and adolescents. Dis Manag. 2004;7:305–13.
Article
PubMedGoogle Scholar
-
Murphy KR, Zeiger RS, Kosinski M, Chipps B, Mellon M, Schatz M, Lampl K, Hanlon JT, Ramachandran S. Test for respiratory and asthma control in kids (TRACK): a caregiver-completed questionnaire for preschool-aged children. J Allergy Clin Immunol. 2009;123:833–9. e839
Article
PubMedGoogle Scholar
-
Groot EP, Kreggemeijer WJ, Brand PL. Getting the basics right resolves most cases of uncontrolled and problematic asthma. Acta Paediatr. 2015;104:916–21.
Article
PubMedGoogle Scholar
-
Zaidi S, Williams J, Monaghan T, Burhan H, Main N. Inhaler Technique: Does Poor Technique Mean More Admissions? Am J Respir Crit Care Med. 2012;185:A-3333.
Google Scholar
-
Roggeri A, Micheletto C, Boarino S, Inzillo V, Roggeri DP. Potential economic impact of inhalation errors due to device switch in patients with chronic obstructive pulmonary disease and asthma. Value Health. 2015;18:A-PMD147.
Google Scholar
-
Roggeri A, Micheletto C, Roggeri DP. Inhalation errors due to device switch in patients with chronic obstructive pulmonary disease and asthma: critical health and economic issues. Int J Chron Obstruct Pulmon Dis. 2016;11:597–602.
Article
PubMed
PubMed CentralGoogle Scholar
-
Bijos P, Kaczynski J, Torvinen S, Lenarczyk E, Wrona W, Plich A, Lewis A, Blackney M. Clinical and economic burden of asthma and chronic obstructive pulmonary disease (COPD) in Poland: estimated impact of poor inhalation technique with inhaled corticosteroid and long-acting beta agonist fixed-dose combinations. Value Health. 2015;18:A-PRS34.
Article
Google Scholar
-
Torvinen S, Nicolai J, Pulimeno S, di Nola L, Bruno G, Colombo G, Di Matteo S, Valentino M, Lewis A, Blackney M. The budget impact of Duoresp® Spiromax® compared with commonly prescribed dry powder inhalers for the management of asthma and chronic obstructive pulmonary disease in Italy: estimated impact of inhalation technique. Value Health. 2015;18:A-PRS16.
Google Scholar
-
Lewis A, Blackney M, Torvinen S, Plich A. Clinical and economic burden of asthma and chronic obstructive pulmonary disease in the UK: impact of critical inhaler errors with inhaled corticosteroid + long-acting beta agonist fixed-dose combinations. Value Health. 2014;17:A-PRS30.
Article
Google Scholar
-
Lewis A, Blackney M, Garcia BL, Sánchez-de la Rosa R, Torvinen S, Plich A. The potential for improved inhalation technique with Duoresp® Spiromax®(budesonide+formoterol fumarate dihydrate) compared with commonly prescribed dry powder inhalers for the management of asthma and chronic obstructive pulmonary disease in Spain: estimated impact on number and cost of unscheduled healthcare events. Value Health. 2015;18:A-PMD37.
Google Scholar
-
Lewis A, Blackney M, Torvinen S, Lindqvist F, Safioti G, Grundstrom J, Polyzoi M, Plich A. The potential societal cost benefits of improved inhalation technique with Duoresp Spiromax (budesonide + formoterol fumarate dihydrate) compared with Symbicort Turbuhaler for the management of asthma and chronic obstructive pulmonary disease in sweden. Value Health. 2014;17:A-PRS62.
Article
Google Scholar
-
Lewis A, Blackney M, Torvinen S, Holmes J, Osborne M, Dale J, Chandler S, Plich A. The budget impact of Duoresp Spiromax (budesonide + formoterol fumarate dihydrate) compared with Symbicort Turbohaler for the management of asthma and chronic obstructive pulmonary disease in the United Kingdom: impact on health care costs and inhalation technique. Value Health. 2014;17:A-PRS19.
Article
Google Scholar
-
Estrada J, Restrepo A, Serna J, Herrera R, Arrieta J, Segura A. Impact of a pharmacotherapeutic follow-up program on the cost-month-patient, stratified by risk-pharmacological type. Value Health. 2015;18:A-PRS14.
Google Scholar
-
Basheti I, Bosnic-Anticevich S, Armour C, Reddel H. Checklists for powder inhaler technique: a review and recommendations. Respir Care. 2014;59:1140–54.
Article
PubMedGoogle Scholar
-
Basheti IA, Reddel HK, Armour CL, Bosnic-Anticevich SZ. Improved asthma outcomes with a simple inhaler technique intervention by community pharmacists. J Allergy Clin Immunol. 2007;119:1537–8.
Article
PubMedGoogle Scholar
-
Sulaiman I, Seheult J, Sadasivuni N, Cushen B, Mokoka M, Costello R. Inhaler technique errors have an impact on drug delivery. Am J Respir Crit Care Med. 2016;193:A-1715.
Google Scholar
-
Molimard M, Raherison C, Lignot S, Balestra A, Lamarque S, Chartier A, Droz-Perroteau C, Lassalle R, Moore N, Girodet P-O. Chronic obstructive pulmonary disease exacerbation and inhaler device handling: real-life assessment of 2935 patients. Eur Respir J. 2016;49
-
Price DB, Roman-Rodriguez M, McQueen RB, Bosnic-Anticevich S, Carter V, Gruffydd-Jones K, Haughney J, Henrichsen S, Hutton C, Infantino A, et al. Inhaler errors in the CRITIKAL study: type, frequency, and association with asthma outcomes. J Allergy Clin Immunol Pract. 2017;5:1071–1081.e1079.
Article
PubMedGoogle Scholar
-
Williams SA, Wagner S, Kannan H, Bolge SC. The association between asthma control and health care utilization, work productivity loss and health-related quality of life. J Occup Environ Med. 2009;51:780–5.
Article
PubMedGoogle Scholar
-
Vervloet D, Williams A, Lloyd A, Clark T. Costs of managing asthma as defined by a derived asthma control TestTM score in seven European countries. Eur Respir Rev. 2006;15:17–23.
Article
Google Scholar
-
Szende A, Svensson K, Ståhl E, Meszaros A, Berta GY. Psychometric and utility-based measures of health status of asthmatic patients with different disease control level. PharmacoEconomics. 2004;22:537–47.
Article
PubMedGoogle Scholar
-
Doz M, Chouaid C, Com-Ruelle L, Calvo E, Brosa M, Robert J, Decuypere L, Pribil C, Huerta A, Detournay B. The association between asthma control, health care costs, and quality of life in France and Spain. BMC Pulm Med. 2013;13:15.
Article
PubMed
PubMed CentralGoogle Scholar
-
Demoly P, Annunziata K, Gubba E, Adamek L. Repeated cross-sectional survey of patient-reported asthma control in Europe in the past 5 years. Eur Respir Rev. 2012;21:66–74.
Article
CAS
PubMedGoogle Scholar
-
Jha A, Heron L, Marshall J, Dunlop W. Device handling errors and the impact on quality of life and health care resource use in asthmatic patients. Value Health. 2014;17:A-PRS64.
Google Scholar
-
Scichilone N, Benfante A, Bocchino M, Braido F, Paggiaro P, Papi A, Santus P, Sanduzzi A. Which factors affect the choice of the inhaler in chronic obstructive respiratory diseases? Pulm Pharmacol Ther. 2015;31:63–7.
Article
CAS
PubMedGoogle Scholar
-
Lavorini F, Mannini C, Chellini E, Fontana GA. Optimising inhaled pharmacotherapy for elderly patients with chronic obstructive pulmonary disease: the importance of delivery devices. Drugs Aging. 2016;33:461–73.
Article
CAS
PubMedGoogle Scholar
-
Perez L, Morales K, Huang J, Ndicu G, Han X, Klusaritz H, Localio A, Apter AJ. Aspects of asthma self-management: inhaler technique, ability to access (navigate) health care, and inhaled steroid knowledge are correlated. Am J Res Crit Care Med. 2016;193:A6426.
-
Kiser K, Jonas D, Warner Z, Scanlon K, Shilliday BB, DeWalt DA. A randomized controlled trial of a literacy-sensitive self-management intervention for chronic obstructive pulmonary disease patients. The. J Gen Intern Med. 2012;27:190–5.
Article
PubMedGoogle Scholar
-
Paasche-Orlow MK, Riekert KA, Bilderback A, Chanmugam A, Hill P, Rand CS, Brancati FL, Krishnan JA. Tailored education may reduce health literacy disparities in asthma self-management. Am J Respir Crit Care Med. 2005;172:980–6.
Article
PubMed
PubMed CentralGoogle Scholar
-
Al Zabadi H, El Sharif N. Factors associated with frequent emergency room attendance by asthma patients in Palestine. Int J Tuberc Lung Dis. 2007;11:920–7.
CAS
PubMedGoogle Scholar
-
Azouz W, Chetcuti P, Hosker H, Saralaya D, Chrystyn H. Objective measurement of inhalation profiles in patients using metered dose inhalers (MDIs). Eur Respir J. 2011;38:A-838.
Google Scholar
-
Baddar S, Al-Rawas O. What is missing in the asthma control test? The relationship between compliance, inhaler technique and level of control. Eur Respir J. 2012;40:A-P513.
Article
Google Scholar
-
Bilal M, Ahmed A, Shah AR, Mirza HA, Anwar AK, Zaidi SBH. Prevalence of the correct technique of using an inhaler among asthmatic patients reporting in tertiary care hospitals of Rawalpindi, Pakistan. J Allergy Clin Immunol. 2012;1:A-159.
Google Scholar
-
Caliskaner Z, Ozturk C, Pekcan S, Yilmaz O, Ozturk S, Ceylan E, Can C, Sener O, Turay U, Ersoy R. The «extreme» errors in inhaler device use: data from the INTEDA-1 study. In: Allergy; 2011. p. 369–70.
Google Scholar
-
Chrystyn H, Pascual S, Feimer J, De Soyza A, Sauleda Roig J, Haughney J, Padulles L, Seoane B, Rekeda L, Ribera A. Preference, satisfaction and critical errors with Genuair and Breezhaler in patients with COPD. Eur Respir J. 2014;44:A-P928.
Google Scholar
-
Deering B, MacCormack N, Kerrigan K, D’Arcy S, Costello RW. Adherence to inhalers after discharge from hospital following an exacerbation of COPD. Ir J Med Sci. 2013;182:S458.
Google Scholar
-
Hass C, Engdahl K, Albert W, Setyawan J, Mateo N. Patient preferences and perceived ease of use in inhaler features: Genuair vs other inhalers. Chest. 2010;138:A-484.
Article
Google Scholar
-
Herscher M, Ray M, Busse PJ, Wolf MS, Wisnivesky JP, Federman A. Characteristics and outcomes of older adults with early versus late onset asthma. Am J Respir Crit Care Med. 2014;189:A-1359.
Article
CASGoogle Scholar
-
Leiva-Fernandez F, Leiva-Fernandez J, Porcel-Martin C, Prados-Torres D, Garcia-Ruiz AJ, Barnestein-Fonseca P. How do patients with chronic obstructive pulmonary disease (COPD) use their inhalers? Common mistakes. Tecepoc study. Value Health. 2013;16:A-PRS45.
Google Scholar
-
Mazankova D, Mendelova I, Saloun J. Identification of error rate in using inhalation devices by asthmatic patients. Int J Clin Pharm. 2013;35(6):1279–80.
Google Scholar
-
Muhammad I, Haque AS, Muhammad N, Khan JA. Real life perspective in outpatient asthma treatment at a tertiary care center of Pakistan. Respirology. 2009;14:A-PD 10-09.
Google Scholar
-
Santos JC, Silveira BF, Rizzatti F. Knowledge of and technique for using inhalation devices among asthma and COPD patients. Am J Res Crit Care Med. 2014;A-4656
-
Souza M, Meneghini A, Ferraz E, Vianna E, Borges M. Knowledge of and technique for using inhalation devices among asthma patients and COPD patients. J Bras Pneumol. 2009;35:824–31.
Article
PubMedGoogle Scholar
-
Tarsin W, Alshamli I, Soussi M. Preference of the inhaler device and assessment of the technique among the asthmatic and COPD patients. Eur Respir J. 2011;38:A-3981.
Google Scholar
-
Williams J, Mault S, Garner N, Burhan H, Zaidi S. Breaking down bad inhaler technique: device specific advice. Am J Respir Crit Care Med. 2012;185:A-3332.
Google Scholar
Download references
Acknowledgements
We would like to thank Alison Saunders, Iván Viejo Viejo and Rebecca Forster for their support in quality checking and co-ordinating this manuscript and Robin Wyn for editorial assistance.
Funding
Funding was provided by Mundipharma International Ltd. to Adelphi Values Ltd. to support this research and the writing of the manuscript. No financial payment was provided to the individual authors of the review.
Availability of data and materials
The datasets used and/or analysed during the current study are available from the corresponding author on reasonable request.
Trademark
® DISKHALER, DISKUS and ROTAHALER are registered trademarks of Glaxo Group Limited.
® ACCUHALER and EVOHALER are registered trademarks (in the European Union) of Glaxo Group Limited.
® REVOLIZER is a registered trade mark (in the United States) of Cipla Limited.
® AUTOHALER is a registered trade mark of 3 M Company.
® STARHALER is a registered trade mark (in India) of Sun Pharma Laboratories Limited.
® TURBUHALER is a registered trade mark (in the European Union) of AstraZeneca AB.
® HANDIHALER and HandiHaler are registered trademarks of Boehringer Ingelheim Pharma GmbH & Co. KG.
® AEROLIZER is a registered trade mark of Novartis AG.
® GENUAIR is a registered trade mark of AstraZeneca AB.
® BREEZHALER is a registered trade mark (in the European Union) of Novartis AG.
® ELPENHALER is a registered trade mark of Elpen Pharmaceutical Co. Inc.
® CYCLOHALER is a registered trade mark (in the European Union) of Pharmachemie B.V.
® EASI-BREATHE is a registered trade mark (in the European Union) of Norton Healthcare Limited.
® PULVINAL is a registered trade mark (in the European Union) of Chiesi Farmaceutici S.p.A.
® PULMOJET is a registered trade mark (in the European Union) of Sanofi S.A.
Author information
Authors and Affiliations
-
Airway Disease, NHLI, Imperial College London & Royal Brompton Hospital, Dovehouse Street, London, SW3 6LY, UK
Omar Sharif Usmani
-
Department of Experimental and Clinical Medicine, Careggi University Hospital, Florence, Italy
Federico Lavorini
-
Mundipharma International Limited, Cambridge Science Park, Cambridge, CB4 0AB, UK
Jonathan Marshall & William Christopher Nigel Dunlop
-
Adelphi Values, Adelphi Mill, Macclesfield, Cheshire, SK10 5JB, UK
Louise Heron & Emily Farrington
-
Radboud University Medical Center, Nijmegen, Netherlands
Richard Dekhuijzen
Authors
- Omar Sharif Usmani
You can also search for this author in
PubMed Google Scholar - Federico Lavorini
You can also search for this author in
PubMed Google Scholar - Jonathan Marshall
You can also search for this author in
PubMed Google Scholar - William Christopher Nigel Dunlop
You can also search for this author in
PubMed Google Scholar - Louise Heron
You can also search for this author in
PubMed Google Scholar - Emily Farrington
You can also search for this author in
PubMed Google Scholar - Richard Dekhuijzen
You can also search for this author in
PubMed Google Scholar
Contributions
All authors have contributed equally to the analysis, review, writing and finalisation of this manuscript. All authors have read and approved the final manuscript.
Corresponding author
Correspondence to
Omar Sharif Usmani.
Ethics declarations
Ethics approval and consent to participate
Not applicable.
Consent for publication
Not applicable.
Competing interests
In the last 5 years, Omar S. Usmani and/or his department received research grants, unrestricted educational grants, and/or fees for lectures and advisory board meetings from Aerocrine, Astra Zeneca, Boehringer Ingelheim, Chiesi, Cipla, Edmond Pharma, GlaxoSmithKline, Napp, Mundipharma International, Prosonix, Sandoz, Takeda, Zentiva.
In the last 5 years, Federico Lavorini received fees for lectures and advisory board meetings from Astra Zeneca, Boehringer Ingelheim, Chiesi, Cipla, Menarini International, TEVA, Zentiva.
In the last 3 years, Richard Dekhuijzen and/or his department received research grants, unrestricted educational grants, and/or fees for lectures and advisory board meetings from AstraZeneca, Boehringer Ingelheim, Chiesi, GSK, Mundipharma International, Novartis, Takeda and Teva.
William Dunlop and Jonathan Marshall are employees of Mundipharma International Ltd., United Kingdom.
Emily Farrington and Louise Heron are employees of Adelphi Values Ltd., UK. Adelphi Values Ltd. received funding from Mundipharma International Ltd. to support this research.
The authors do not report any conflict of interest with regards to the contents of this study other than those stated.
Publisher’s Note
Springer Nature remains neutral with regard to jurisdictional claims in published maps and institutional affiliations.
Additional file
Additional file 1:
One supplementary file is associated with this manuscript: “Online Resource – Critical handling errors in asthma and COPD: A systematic review of impact on health outcomes”. This contains: search strategies and details of the analysis conducted within this literature review (Table S1); a breakdown of grouped critical errors described in the literature for different inhaler device types (Table S2); summaries of pre-existing known publications that show associations between poor disease control, economic burden and poor QoL (Table S3); definitions of a ‘critical’ error provided by studies captured within the literature review (Table S4). This file is named: “Critical handling errors data supplement update v8_0”. (DOCX 588 kb)
Rights and permissions
Open Access This article is distributed under the terms of the Creative Commons Attribution 4.0 International License (http://creativecommons.org/licenses/by/4.0/), which permits unrestricted use, distribution, and reproduction in any medium, provided you give appropriate credit to the original author(s) and the source, provide a link to the Creative Commons license, and indicate if changes were made. The Creative Commons Public Domain Dedication waiver (http://creativecommons.org/publicdomain/zero/1.0/) applies to the data made available in this article, unless otherwise stated.
Reprints and Permissions
About this article
Cite this article
Usmani, O.S., Lavorini, F., Marshall, J. et al. Critical inhaler errors in asthma and COPD: a systematic review of impact on health outcomes.
Respir Res 19, 10 (2018). https://doi.org/10.1186/s12931-017-0710-y
Download citation
-
Received: 07 September 2017
-
Accepted: 21 December 2017
-
Published: 16 January 2018
-
DOI: https://doi.org/10.1186/s12931-017-0710-y
Keywords
- Obstructive lung diseases
- Adherence
- Errors
- Aerosols
- Inhalers
Неправильное использование ингаляторов: оценка ингаляционной техники и предпочтений пациентов при сравнении семи различных ингаляционных устройств
https://doi.org/10.18093/0869-0189-2005-0-4-80-84
Полный текст:
- Аннотация
- Об авторах
- Список литературы
Аннотация
Неправильная техника ингаляций — частая проблема, приводящая к плохой доставке лекарства в дыхательные пути, снижающая контроль над болезнью и увеличивающая частоту применения ингаляторов. Цель данного исследования — оценить технику использования больными ингаляционных устройств различных видов и сделать вывод, являются ли предпочтения пациентов в выборе ингалятора показателем правильности его использования, и влияет ли постоянное применение ингалятора на технику ингаляций и предпочтения пациента. Мы также хотели определить наиболее приемлемый способ подбора ингалятора для конкретного больного с учетом техники использования и стоимости ингалятора. 100 пациентам в рандомизированном порядке были даны инструкции по применению 7 различных ингаляционных устройств. Затем была оценена техника ингаляций по заранее определенным критериям. Далее пациентам было предложено выбрать 3 наиболее предпочитаемых ими ингалятора, и задан вопрос, какими ингаляторами они пользуются постоянно. Лучшая техника ингаляций наблюдалась при использовании активируемых вдохом ингаляционных устройств, ингаляционной системы «Легкое Дыхание» и Аутохалера — 91 % больных показали хорошую технику их применения. Техника использования дозированных аэрозольных ингаляторов (ДАИ) была на последнем месте — только 79 % больных показали хорошую технику ингаляций, несмотря на то, что эти ингаляторы назначаются наиболее часто. Ингалятор «Легкое Дыхание» был наиболее популярным среди пациентов. Аутохалер занял второе место, близко к нему оказались Кликхалер и Аккухалер.
Большинство больных (55 %) постоянно пользуются обычными дозированными аэрозольными ингаляторами (ДАИ), но не отдают им предпочтения перед другими ингаляционными устройствами. Только 79 % обследованных пациентов могли эффективно использовать ДАИ даже после инструкции экспертов, хотя эти ингаляторы остаются наиболее часто назначаемыми. Это имеет большое значение для доставки лекарства в дыхательные пути и, следовательно, контроля над болезнью. Назначение больному того ингалятора, который он предпочитает, увеличивает стоимость, но зато может улучшить эффективность лечения и, таким образом, стать экономически более выгодным при длительном применении. Использование недорогих ингаляционных устройств ДАИ целесообразно при хорошей технике ингаляций и положительном отношении больного к этим ингаляторам; в противном случае необходимо оптимизировать доставку лекарства в дыхательные пути, что также может снизить стоимость лечения.
Об авторах
Дж. Ленней
Респираторное функциональное отделение, блок респираторной медицины; Вестерн Дженерал госпиталь
Великобритания
Эдинбург
Дж. А. Иннс
Респираторное функциональное отделение, блок респираторной медицины; Вестерн Дженерал госпиталь
Великобритания
Эдинбург
Дж. К. Кромптон
Респираторное функциональное отделение, блок респираторной медицины; Вестерн Дженерал госпиталь
Великобритания
Эдинбург
Список литературы
1. Crompton G.K. Problems patients have using their pressurised aerosol inhalers. Eur. J. Respir. Dis. 1982; 63 (suppl. 119): 101–104.
2. King D., Earnshaw S.M., Delaney J.C. Pressurised aerosol inhalers: the cost of misuse. Br. J. Clin. Pract. 1991; 45: 48–49.
3. Hardy J.G., Jasuja A.K., Frier M., Perkins A.C. A small volume spacer for use with a breath-operated pressurized metered dose inhaler. Int. J. Pharmaceut. 1996; 142: 129–133.
4. Fergusson R.J., Lenney J., McHardy G.J., Crompton G.K. The use of a new breath-actuated inhaler by patients with severe airflow obstruction. Eur. Respir. J. 1991; 4: 172–174.
5. Crompton G.K., Duncan J. Clinical assessment of a new breath-actuated inhaler. Practitioner 1989; 233: 268–269.
6. Newman S.P., Weisz A.W., Talaee N., Clarke S.W. Improvement of drug delivery with a breath-actuated pressurised aerosol for patients with poor inhaler technique. Thorax 1991; 46: 712–716.
7. Chapman K.R., Love L., Brubaker H. A comparison of breath-actuated and conventional metered-dose inhaler inhalation techniques in elderly subjects. Chest 1993; 104: 1332–1337.
8. Monthly Index of Medical Specialities. 1999; Jan.
Рецензия
Для цитирования:
Ленней Д., Иннс Д.А., Кромптон Д.К. Неправильное использование ингаляторов: оценка ингаляционной техники и предпочтений пациентов при сравнении семи различных ингаляционных устройств. Пульмонология. 2005;(4):80-84. https://doi.org/10.18093/0869-0189-2005-0-4-80-84
For citation:
Lenney J., Innes J.A., Crompton G.K. Inappropriate inhaler use: assessment of use and patient preference of seven inhalation devices. PULMONOLOGIYA. 2005;(4):80-84.
(In Russ.)
https://doi.org/10.18093/0869-0189-2005-0-4-80-84
Просмотров: 292
Критические ошибки в технике ингаляции при бронхиальной астме

Распространенность ошибок во время проведения ингаляции у детей, страдающих от бронхиальной астмы, по-прежнему высока.
Правильная техника ингаляции позволит большинству детей, страдающих от бронхиальной астмы (БА) достичь значительного улучшения контроля заболевания. Данные исследований свидетельствуют о том, что биодоступность лекарственных средств в форме дозированных аэрозольных ингаляторов увеличивается с 34% до 83% при использовании специального аксессуара — спейсера. Это улучшение связано с уменьшением депозиции действующего вещества в ротоглотке. Учитывая эти данные, использование спейсера было рекомендовано всем пациентам педиатрического профиля с БА. Однако, в настоящее время не удалось достичь правильной техники использования ингалятора у большинства детей.
Целью нового исследования, опубликованного в Journal of Hospital Medicine, была оценка техники ингаляции у пациентов, госпитализированных по поводу БА и выявление факторов риска, которые приводят к неправильному применению ингалятора.
В проспективном перекрестном исследовании приняли участие 113 пациентов с БА в возрасте от 2 до 16 лет. В ходе исследования пациентов или, при необходимости, их родителей попросили продемонстрировать технику использования ингалятора вместе со спейсером с маской и со спейсером с мундштуком.
Результаты исследования показали, что почти половина пациентов (42%) пропускает хотя бы один важный шаг в технике проведения ингаляции. При использовании спейсера с мундштуком большее количество пациентов пропускают важный шаг по сравнению с использованием спейсера с маской (75% [51%-90%] и 36% [27%-46%] соответственно; P=0,003). Наиболее распространенными ошибками при использовании спейсера с маской были — недостаточно плотное прижатие маски к лицу во время ингаляции и несоблюдение интервала в 30–60 секунд перед повторным применением ингалятора. При использовании спейсера с мундштуком — отсутствие глубокого выдоха перед использованием спейсера и недостаточно медленный и плавный вдох во время ингаляции.
Отмечается, что дети, которые совершали ошибки во время ингаляции были значительно старше (7,8 [6,7–8,9] и 5,8 [5,1–6,5] лет; P = 0,002). Возможно, это связано с переходом к самостоятельному проведению ингаляций, когда дополнительный контроль со стороны родителей уменьшается.
Результаты исследования подтверждают, что ошибки при ингаляции распространены у детей с БА, особенно при использовании спейсера с мундштуком. Образовательные мероприятия как в стационарных, так и в амбулаторных условиях помогут улучшить технику ингаляции у пациентов, и, следовательно, качество доставки лекарства и контроль БА.
https://europepmc.org/abstract/med/30986181
- 0
Исследование выявило главные ошибки в пользовании ингаляторами, связанные с неблагоприятным развитием астмы.
Исследование, получившее название CRITIKAL (CRITical Inhaler mistaKes and Asthma controL – «Критические ошибки при пользовании ингалятором и контроль над астмой»), носило наблюдательный характер. Его проводили совместно международный Observational and Pragmatic Research Institute (Институт обсервационных и практических исследований) со штаб-квартирой в Сингапуре и международный некоммерческий проект Respiratory Effectiveness Group (Группа респираторной эффективности) со штаб-квартирой в Кембридже (Великобритания). Частичное финансирование осуществляла компания по разработке лекарств Mundipharma Research Limited, офисы которой расположены в Кембридже и Лимбурге (ФРГ).
К проекту привлекли 3660 пациентов – участников iHARP (британская инициатива «Помощь в лечении астмы пациентам в реальной жизни») – кросс-секционного исследования, в котором с 2011 по 2014 год приняли участие более 5000 астматиков из 8 стран. Среди них две группы использовали порошковые ингаляторы Symbicort Turbuhaler и Seretide Diskus, одна применяла дозирующее устройство Seretide MDI.
Технику пользования ингаляторами отслеживал квалифицированный медперсонал; результаты заносились в специальную форму. Уровень контроля над астмой определялся с помощью опросника. Кроме того, фиксировались имевшие место в предыдущие 12 месяцев случаи осложнений: экстренной госпитализации, лечения в стационаре из-за проблем с дыханием или органами грудной клетки, курсового приема пероральных стероидов из-за ухудшения симптомов астмы.
Как выяснили специалисты, самая распространенная ошибка при пользовании порошковыми ингаляторами – недостаточное усилие при вдохе: она была отмечена у 32–38% испытуемых. Эта ошибка была связана с 30-процентным ростом риска неконтролируемой астмы среди использовавших Turbuhaler и 56-процентным – у применявших Diskus. Кроме того, в обеих группах у пациентов, совершавших эту ошибку, повышался процент осложнений.
А вот недостаточно сильный выдох, освобождающий легкие перед ингаляцией (ошибка, встречающаяся примерно у четверти больных), не ведет к неконтролируемой астме.
Для дозирующих ингаляторов актуация (нажатие на соответствующий клапан, чтобы выпустить дозу препарата) перед ингаляцией связана с 55-процентным ростом риска неконтролируемой астмы. При этом самая распространенная ошибка – недостаточно медленный и глубокий вдох – не приводит к неконтролируемой астме. Кроме того, ни одна из ошибок при пользовании дозирующим ингалятором не вызывает серьезных осложнений.
Другие специфические ошибки, связанные с неблагоприятным течением астмы, для пользователей Turbohaler включают неснятый колпачок и сниженную дозу препарата после того, как ингалятор встряхнули или перевернули, что в высокой степени сопряжено с неконтролируемой астмой. У пользователей дозирующих ингаляторов к неконтролируемой астме приводит недостаточно высокий подъем подбородка.
В своем отечете, опубликованном в онлайн-версии Journal of Allergy and Clinical Immunology: In Practice, исследователи отмечают, что это первая попытка разобраться во влиянии индивидуальных, специфических ошибок на неблагоприятное течение астмы. «Ценность нашего исследования в том, что мы не выискивали новые ошибки в пользовании ингаляторами, а выявляли те, которые по-настоящему существенны,– объясняет главный автор исследования Дэвид Прайс, завотделением первичной помощи при респираторных заболеваниях Абердинского университета.– Зато некоторые из ошибок, которые люди считали важными, в реальной жизни оказались совсем не такими значительными».
По словам ученых, результаты показывают, что искоренение ключевых ошибок в ходе обучения пользованию ингалятором может серьезно улучшить течение астмы. «Наши выводы указывают фармацевтам и работникам здравоохранения, на каких вопросах необходимо сосредоточиться»,– отмечает Прайс.
Комментируя результаты исследования, Анна Мёрфи, фармацевт-консультант в области респираторных заболеваний университетских клиник Лестерского траста Национальной службы здравоохранения Великобритании, заявила, что исследование подчеркивает важность индивидуального подхода к лечению астматиков. «Исследование еще раз показало, что необходимо всячески совершенствовать технику пользования ингалятором и прописывать пациентам те устройства, которыми им удобно пользоваться».
Необходимо, чтобы все медработники осознали, что правильное пользование ингаляторами – залог успешного лечения астмы, уверена Мёрфи. «К этому методу терапии нужно относиться крайне серьезно,– говорит она.– Если мы, работники здравоохранения, поймем, насколько важен ингалятор и его правильное использование, то не только поможем лечению пациентов, уменьшению побочных эффектов и сокращению расходов системы медицинского страхования, но и облегчим состояние больных, вынужденных длительное время находиться на препаратах».
Источник: The Pharmaceutical Journal
Программа занятий Школы профилактики бронхиальной астмы
Что такое бронхиальная астма?
Почему возникает приступ бронхиальной астмы? Аллергия и бронхиальная астма.
Хроническое воспаление и бронхиальная астма. Механизмы обструкции при бронхиальной астме.
Неаллергические причины бронхиальной астмы.
Пикфлоуметрия. Бронхолитический тест. Правила построения графиков пикфлоуметрии. Индивидуальные зоны контроля.
Ингаляционная терапия бронхиальной астмы. Симптоматическое лечение бронхиальной астмы.
Лечение хронического воспаления при бронхиальной астме.
Глюкокортикостероидная терапия при бронхиальной астме.
Лечение обострения бронхиальной астмы.
Лечение и профилактика вирусной и бактериальной инфекции.
Занятие № 1
Тема: Общие понятия.
План занятия:
- Что такое Школа здоровья для больных бронхиальной астмой?
- Определение бронхиальной астмы.
- Бронхиальная астма — хроническое воспаление.
- Строение дыхательных путей.
- Что происходит при приступе бронхиальной астмы?
- Аллергические и неаллергические причины бронхиальной астмы.
Реквизит: плакат «Строение дыхательных путей», «Бронхи вне приступа и при приступе астмы», буклеты.
На первом занятии больные знакомятся друг с другом и с преподавателем. Занятие начинается с того, что преподаватель представляется слушателям и записывает присутствующих. Затем кратко рассказывает о том, что такое Школа здоровья и как будет организована программа обучения; после чего переходит к теме первого занятия — «Что такое бронхиальная астма».
Бронхиальная астма — это хроническое воспалительное заболевание бронхов, при котором периодически возникает обратимое сужение дыхательных путей — бронхоспазм.
Пациентам следует объяснить, что бронхиальная астма, так же как и сахарный диабет, гипертоническая болезнь — заболевание хроническое. У детей бронхиальная астма может исчезнуть, но у взрослых можно говорить о длительной ремиссии, а не о полном излечении. Поэтому главная задача больного — научиться контролировать свою болезнь, не допускать обострений.
Для того чтобы контролировать свою болезнь, каждому пациенту надо хорошо представлять анатомию бронхиального дерева и те механизмы, которые лежат в основе приступа бронхиальной астмы.
Врач или средний медицинский работник рассказывает слушателям:
- о внешнем строении дыхательных путей, о связи заболевания верхних и нижних дыхательных путей, о ветвлении бронхов и о понятии бронхиального дерева, о дыхательном акте и роли диафрагмы в дыхательном акте.
- о внутреннем строении дыхательных путей, о механизмах самоочищения бронхиального дерева, о мукоцилиарном клиренсе, о губительном влиянии курения на защитные процессы в дыхательных путях, о бронхиальном секрете — его составе и защитных свойствах.
- о механизмах развития приступа бронхиальной астмы: о понятии бронхоспазма, об отеке слизистой, о гиперсекреции мокроты; демонстрируется различие между бронхами во время и вне приступа астмы.
- об аллергических причинах бронхиальной астмы.
Аллергия — это повышенная чувствительность организма к воздействию некоторых факторов окружающей среды: химических веществ, микроорганизмов и продуктов их жизнедеятельности, пищевых продуктов, лекарственных средств, физических явлений; это состояние, имеющее наследственную предрасположенность, при котором в организме в ответ на воздействие аллергенов вырабатывается целая группа специфических веществ (в том числе иммуноглобулины). Наиболее распространены такие проявления аллергии, как бронхиальная астма, поллинозы (аллергия на пыльцу растений), крапивница.
Среди аллергенов самые распространенные — бытовая пыль, шерсть животных, пыльца растений, домашний клещ, лекарства, препараты бытовой химии, пищевые продукты. Сюда же относятся различные бактерии, вирусы и грибки, продукты их жизнедеятельности. Иногда аллергеном является рачок-дафния, который используется в качестве корма для рыб. Среди факторов, способствующих росту числа аллергических заболеваний, большое место занимает и ухудшение экологической обстановки, в частности загрязнение атмосферы выхлопными газами автомобилей.
Очень важно акцентировать внимание пациентов на профилактике бытовой аллергии, которая включает: регулярную влажную уборку, проветривание квартиры, избавление от вещей, накапливающих пыль — мягкой мебели, ковров, тяжелых штор; застекление книжных полок и т.д.
Необходимо детально рассказать о домашней пыли, которая содержит много органических и неорганических компонентов, в частности, остатки насекомых, перхоть животных, остатки пищи, бактерии, грибы. Еще один компонент домашней пыли — домашний клещ (Dermatophagoides pteronissimus), питающийся перхотью и остатками пищи. Часто домашний клещ является основным аллергеном. В коврах, мягкой мебели, шерстяных вещах, перьевых подушках содержится огромное количество клещей. Ложась спать на перовую подушку и укрываясь шерстяным одеялом, больной бронхиальной астмой подвергается массивному воздействию аллергена.
Вследствие этого выработаны специальные требования к помещению, в котором живет больной бронхиальной астмой (особо строгие правила должны соблюдаться в отношении спальни):
В спальне должно быть минимум мебели. Украшения на стенах (в том числе и картины) и ковровые покрытия являются коллектором пыли, желательно от них избавиться. Занавески должны быть из легкого материала и стираться. В спальне не должно быть книжных полок.
Стенной шкаф необходимо мыть и держать в нем только сезонную одежду. Одежда должна быть убрана в шкаф, а не развешана по стульям и лежать на кровати. Дверцы шкафа должны быть плотно закрыты.
Необходимо проводить влажную уборку не реже 3-4 раз в неделю. Желательно, чтобы уборкой занимались родственники, а не сам больной астмой. Уборку помещения необходимо осуществлять специальным пылесосом с водным фильтром и сепаратором, который изолирует всю пыль в водной среде и предотвращает увеличение её содержания в воздухе после уборки обычным пылесосом.
На матрасы необходимо надевать специальные пыленепроницаемые чехлы. Под кроватью нельзя хранить старые газеты и книги.
Перьевые и пуховые подушки следует заменить на ватные или сделанные из полиэстера. На подушках также должны быть пыленепроницаемые чехлы.
На кровати должно лежать покрывало, чтобы в течение дня пыль не накапливалась на постели.
Дети, болеющие астмой, не должны спать с мягкими игрушками.
Запрещается заводить домашних животных. Необходимо разъяснить, что если у больного астмой есть аллергия на кошку, то заводить собаку также нельзя. При бронхиальной астме расширяется спектр аллергенов. Больные должны знать, что нет «гипоаллергенных животных».
Больному астмой, у которого выявляется пыльцевая аллергия, важно знать календарь цветения растений в данной местности и принимать меры по избеганию контакта с аллергенами: не ходить в лес, на луг, в определенные месяцы придерживаться городского образа жизни, по возможности в месяц цветения растения — аллергена уезжать в отпуск и т.д. При аллергии к пищевым продуктам — создание индивидуальных диет.
Кратко необходимо остановиться на том, какие лекарственные препараты нельзя принимать больным с аспириновой бронхиальной астмой, а также какой они должны придерживаться диеты.
Кроме того, необходимо рассказать о методе специфической иммунотерапии, о показаниях и противопоказаниях к этому методу — вид аллергии, стадия заболевания, возраст больного и т.д.
Неаллергические причины бронхиальной астмы
К неаллергическим причинам, вызывающим приступ удушья у больных бронхиальной астмой, относятся: эмоциональный стресс, резкая перемена погоды, выход на холодный воздух, вирусная инфекция, физическая нагрузка, резкие запахи, высокая влажность и др. Одним из характерных признаков бронхиальной астмы является повышенная чувствительность бронхиального дерева отвечать сужением просвета бронхов на воздействие различных неаллергических стимулов, при этом возникает приступ удушья. С гиперреактивностью дыхательных путей бороться очень сложно, и главный метод лечения — стараться избегать ситуаций, при которых возникает приступ удушья.
Известно, что нервный стресс может стать причиной длительного приступа удушья, а у некоторых больных только эмоции поддерживают болезнь. Можно дать советы общего порядка: стараться избегать стрессовых ситуаций, заниматься физкультурой, закаливаться. Существует и ряд больных, которым нужно конфиденциально рекомендовать обратиться к психотерапевту или медицинскому психологу.
Больным, у которых возникает приступ удушья при выходе на холод, рекомендуется за 20-30 минут сделать ингаляцию сальбутамола. Такая же рекомендация относится к профилактике удушья, вызываемого физической нагрузкой. Больным необходимо объяснить, что при астме можно заниматься спортом. Бронхиальная астма не является противопоказанием для занятий спортом, наоборот, физическая активность способствует улучшению течения болезни. Особенно полезным для больных астмой является плаванье.
Занятие № 2
Тема: Медицинская техника.
План занятия:
- Что такое пикфлоуметр? Цели и задачи пикфлоуметрии
- Методика использования пикфлоуметра.
- Методика самоконтроля бронхиальной астмы с помощью пикфлоуметра.
- Правила использования дозированного ингалятора.
- Правила использования спейсера.
- Правила проведения бронхолитического теста.
Цели второго занятия:
- научить слушателей пользоваться пикфлоуметром, дозированным ингалятором и спейсером;
- научить осуществлять полноценный контроль за бронхиальной астмой, используя график пикфлоуметрии.
Реквизит: ингаляторы, пикфлоуметр, спейсер, плакаты с вариантами построения графиков пикфлоуметрии, дневник самоконтроля.
В начале второго занятия необходимо кратко повторить те вопросы, которые обсуждались на предыдущем. Желательно предложить ответить группе на вопросы, касающиеся определения бронхиальной астмы и причин и механизмов развития приступа бронхиальной астмы.
Пикфлоуметр — это прибор для измерения максимальной (пиковой) скорости выдоха (ПСВ). Во всем мире больные бронхиальной астмой утром и вечером измеряют этот показатель, контролируя состояние своего здоровья. Показатель пикфлоуметрии напрямую зависит от того, насколько сужены бронхи.
Техника измерения пиковой скорости выдоха:
Выдох осуществляется в положении стоя, чтобы во время выдоха активно работала диафрагма.
Необходимо сделать глубокий вдох.
Плотно обхватить мундштук прибора губами.
Сделать полный и резкий выдох.
Отметить показания прибора.
Повторить измерения ещё два раза и выбрать лучший.
Занести его в дневник, сравнить с предыдущими показателями.
Больных необходимо обучить технике самоконтроля бронхиальной астмы с помощью пикфлоуметра. Для этого надо научить ведению суточного и недельного дневника пикфлоуметрии.
Цели и задачи дневника пикфлоуметрии:
С помощью динамической пикфлоуметрии можно выявить причинный аллерген (по падению ПСВ в течение дня).
Определить степень бронхиальной обструкции (сравнивая показатель ПСВ с установленной для данного больного нормой).
Определить суточные колебания проходимости дыхательных путей.
Распознать начинающееся обострение бронхиальной астмы.
Оценить эффективность проводимого лечения.
На занятии пациентам дается понятие о разграничении зон контроля на графике пикфлоуметрии, что крайне важно для своевременного распознавания обострения заболевания. Приблизительная схема поведения больного при обострении астмы обсуждается на занятии и записывается каждым слушателем индивидуально, после серийных измерений ПСВ.
Схема разграничения зон контроля
Общепринятым считается разграничение на 3 зоны, в соответствии с цветами светофора: зеленая, желтая и красная зона.
Зеленая зона: показатели ПСВ более 80% от лучших значений. При этом самочувствие хорошее. Рекомендация: использовать свое обычное лечение.
Желтая зона: усиление одышки, появление ночных приступов удушья, увеличение потребности в использовании бронхорасширяющих средств, усиление одышки при небольших физических нагрузках. ПСВ — 60-80% от лучшего значения. Рекомендация: удвоить дозу базисного препарата. Необходимо проконсультироваться с врачом.
Красная зона: выраженная одышка, в том числе при обычной физической нагрузке. Каждую ночь приступы удушья. Резко возрастает кратность применения бронхорасширяющих средств. ПСВ — 40-60%, чаще ниже 50% от лучших значений. Рекомендация: нужна срочная консультация врача, вызвать скорую помощь.
Следовать этой схеме рекомендуется после согласования с пульмонологом.
На занятии подчеркивается, что основным принципом поведения больного при обострении бронхиальной астмы является усиление базисного лечения и обязательное внимательное наблюдение за своим состоянием для того, чтобы вовремя распознать угрожающую жизни ситуацию.
Если больной научится грамотно использовать пикфлоуметр, он сможет самостоятельно контролировать свою болезнь и более сознательно сотрудничать с врачом.
Правила использования дозированного ингалятора
На занятии пациенты обучаются технике применения дозированных ингаляторов. В начале занятия одному — двум больным предлагается продемонстрировать технику пользования ингалятором. Как показывает практика, только единичные больные могли правильно продемонстрировать технику использования ингалятора. Как правило, больные делают одни и те же принципиальные ошибки: не делают предварительный выдох, не четко синхронизируют начало вдоха и нажатие на дно баллончика и т. д. После этого преподаватель рассказывает правильную технику ингаляций и сам её демонстрирует (с этой целью используется плацебо).
Важно, чтобы больные освоили правильную технику ингаляции:
- встряхнуть ингалятор;
- снять защитный колпачок;
- повернуть ингалятор вверх дном;
- сделать полный выдох через слегка сомкнутые губы;
- плотно обхватить мундштук ингалятора губами;
- начиная делать вдох, нажать на дно ингалятора и глубоко вдохнуть лекарство (при этом должно возникнуть ощущение, что лекарство не осталось во рту, а попало в бронхи);
- задержать дыхание на 10 секунд;
- сделать спокойный выдох;
- надеть на ингалятор защитный колпачок.
В настоящее время рекомендуется использовать пластиковые камеры — спейсеры, особенно тем, кто плохо синхронизирует вдох и нажатие на дно баллончика.
Правила пользования спейсером:
- удалить защитный колпачок, встряхнуть ингалятор и вставить его в спейсер;
- обхватить губами ротовой конец спейсера;
- нажать на ингалятор, чтобы лекарство попало в спейсер;
- глубоко и медленно сделать вдох;
- задержать дыхание на 10 секунд, затем выдохнуть через ротовой конец;
- повторить вдох, не нажимая на ингалятор;
- отсоединиться от спейсера;
- выждать 30 секунд, затем (при необходимости) впрыснуть вторую дозу аэрозоля и повторить все вышеперечисленные действия.
В конце занятия больных обучают проведению бронхолитического теста. Для этого предлагается тем пациентам, у кого имеется пикфлоуметр, провести трехкратное измерение ПСВ, при этом оценивая правильность выполнения маневра. Затем, при наличии сниженных показателей проводится ингаляция бронхолитического препарата (беротек или сальбутамол) с использованием спейсера. Повторное измерение ПСВ осуществляется через 15 минут и вычисляется прироста ПСВ. Если прирост скорости составил 15% и более, считается, что тест положительный, который свидетельствует о наличии у пациента бронхоспазма, что требует применения бронхорасширяющего средства. Всем пациентам рекомендуется проводить такой тест каждое утро, отмечая показатели на графике пикфлоуметрии для того, чтобы оценить степень бронхоспазма и необходимость применения бронхолитика.
Занятие № 3
План занятия:
Тема: Ингаляторы.
- Основные группы препаратов, использующиеся в ингаляторах.
- Симптоматическая бронхолитическая терапия.
- Принципы подбора ингалятора.
- Применяемые дозы и симптомы передозировки.
Реквизит:
- ингаляторы дозированные: вентолин, беротек Н, атровент, беродуал Н;
- дискхалеры: вентолин, серевент;
- турбухалер:
- аэролайзер: форадил.
Для того чтобы слушателям были понятны механизмы действия бронхолитических препаратов, необходимо дать краткую информацию о механизмах регуляции тонуса бронхов у человека; рассказать о симпатическом и парасимпатическом отделе вегетативной нервной системы, о медиаторах адреналине и ацетилхолине и тех клинических эффектах, которые они вызывают при воздействии на бронхи и сердечно-сосудистую систему. Исходя из этих механизмов, приводятся сведения о группах бронхолитических средств, которые применяются на сегодняшний день.
Важно подчеркнуть, что при бронхиальной астме существует два вида лечения:
- симптоматическое, применяющееся главным образом для купирования приступа (симпатомиметики, холинолитики и ксантины);
- базовое — противовоспалительное (ингаляционные стероиды, антагонисты лейкотриеновых рецепторов и кромоны).
Обычно у пациентов сразу возникает множество вопросов по названиям препаратов. Надо сразу отвечать, не вдаваясь в подробности и не давая индивидуальных рекомендаций по лечению, так как это дело лечащего врача. Необходимо донести до каждого больного принципиальное отличие базисных противовоспалительных препаратов от бронходилататоров. Опыт показывает, что не весь материал, изложенный на предыдущих занятиях, одинаково хорошо усваивается всеми больными, поэтому надо чаще возвращаться к тем вопросам, которые вызвали непонимание с первого раза.
Больной должен знать, что подбирать лечение больному должен врач. Вредно пользоваться советами окружающих, т.к. существуют разные формы бронхиальной астмы и, соответственно, используется разное лечение. Однако, если трудно вовремя получить совет врача или при дефиците лекарств в аптеках, больные должны знать, какие ингаляторы являются взаимозаменяемыми.
Желательно, чтобы больные записали группы ингаляторов по механизму действия. Симпатомиметики: ФЕНОТЕРОЛ (беротек), САЛЬБУТАМОЛ (вентолин, саламол).
Холинолитики: ипратропиум бромид — АТРОВЕН, ТРОВЕНТОЛ.
Комбинированный препарат: БЕРОДУАЛ, КОМБИВЕНТ.
Препараты продленного действия — САЛЬМЕТЕРОЛ (СЕРЕВЕНТ), ФОРМОТЕРОЛ (ФОРАДИЛ, ОКСИС), ТИОТРОПИЯ БРОМИД (СПИРИВА).
Понимание — какие ингаляторы являются взаимозаменяемыми — достигается путем тренинга. Эффект от применения дозированного ингалятора больной может самостоятельно оценить с помощью динамической пикфлоуметрии и бронхолитического теста.
На этом же занятии больным необходимо рассказать о бесфреоновых формах ингаляционных средств, о том, что в составе БЕРОТЕКА Н И БЕРОДУАЛА Н содержится другой носитель лекарства, который в отличие от фреона не разрушает защитный озоновый слой земли и имеет необычный запах, напоминающий алкоголь, хотя по механизму действия и эффективности не отличается от обычного беротека и беродуала. К использованию новых форм лекарств следует привыкать, так как на фреоновой основе препараты в ближайшее время выпускаться не будут.
Каждый больной использует индивидуально подобранную дозировку лекарственных препаратов. Важно подчеркнуть, что повышение кратности применения бронхорасширяющего препарата свидетельствует об обострении болезни или неадекватно подобранном лечении.
Основные побочные действия бронходилататоров: тахикардия, мышечный тремор, психомоторное возбуждение. Побочные действия больше выражены у симпатомиметиков неселективного действия: ИЗАДРИНА, АЛУПЕНТА, АСТМОПЕНТА. При проявлении таких эффектов желательно снизить дозу или поменять дозированный ингалятор.
Побочные действия атровента, связанные с его атропиноподобным действием, встречаются редко. Важно все время акцентировать внимание слушателей на соблюдении правильной техники ингаляций и наиболее частых ошибках при использовании дозированных аэрозолей:
- делают два нажатия ингалятора подряд, после этого вдыхая препарат один раз;
- не задерживают дыхание на вдохе.
Рекомендуется постоянно напоминать о том, насколько они правильно пользуются карманным ингалятором, ведь от этого зависит его эффективность.
Слушатели часто задают вопрос о том, существует ли привыкание к ингалятору и не может ли возникнуть ситуация, когда без него уже невозможно будет обойтись?
На этот вопрос следует отвечать следующим образом. Лекарства, которые находятся в ингаляторах, привыкания не вызывают. Другое дело, что течение бронхиальной астмы при неполном, неправильном лечении может быть таково, что постоянные обострения вынуждают больного прибегать к помощи ингалятора слишком часто. Частое использование ингалятора (больше 3-4 ингаляций в сутки) говорит о том, что контроль над астмой неполный, и является сигналом, что следует обратиться к врачу, чтобы пересмотреть программу лечения.
Другой частый вопрос: чем ингаляторы лучше других препаратов, например эуфиллина или теофедрина?
Эуфиллин и содержащий эуфиллин препарат теофедрин также относятся к препаратам, расширяющим бронхи, но применяются либо в виде инъекций (эуфиллин).Современные ингаляционные препараты попадают при ингаляции непосредственно в легкие. Вследствие этого:
- именно в легких создается высокая концентрация лекарства;
- они быстрее оказывают свое действие;
- концентрируясь в легких, эти препараты при правильном применении практически не оказывают влияния на другие органы.
Принятой таблетке, чтобы подействовать, надо попасть в желудок, там раствориться, всосаться, с током крови попасть в легкие — причем туда попадает только маленькая её часть, а основная масса разнесется по всему организму. Эуфиллин в инъекциях применяют для лечения приступа астмы, но эту процедуру, в отличие от ингаляции, сам больной выполнить не может.
Однако это не значит, что эти препараты в лечении бронхиальной астмы не стоит использовать. Эуфиллин в виде таблеток, особенно его пролонгированные (длительнодействующие) препараты (теопэк, теотард, ретафил и др.) успешно применяются для постоянной терапии астмы, однако при лечении острого приступа ингаляторы предпочтительнее. Ведь для того, чтобы таблетка оказала свое действие, требуется время.
На занятии демонстрируются различные формы доставки лекарственных бронхолитических препаратов. Так, препарат ВЕНТОЛИН (сальбутамол) выпускается в виде порошка. Упакованный в виде дисков, он называется ВЕНТОДИСК, вдыхается через специальное распыляющее устройство — ДИСКХАЛЕР. При использовании этого устройства необходим активный вдох, только при таком условии препарат попадет в легкие. Существует форма вентолина в таблетках, выпускаемая под названием ВОЛЬМАКС, для детей в дозе 4 мг, а для взрослых 8 мг. Применяется 2 раза в день.
Продленного действия лекарственный препарат САЛЬМЕТЕРОЛ выпускается как в виде ингалятора, так и в виде порошка — дискхалера. ФОРМОТЕРОЛ или ФОРАДИЛ — бронхолитик длительного действия, применяется в виде порошка, доставка которого осуществляется с помощью АЭРОЛАЙЗЕРА. Двукратный прием в течение суток помогает успешно контролировать бронхиальную астму.
В конце занятия пациентам рассказывается о принципах более интенсивной терапии бронхоспастического синдрома с помощью небулайзерного ингалятора, о понятии небулизации (способ превращения жидкой лекарственной формы с помощью струи воздуха или ультразвука в туманообразное состояние). Представляются жидкие лекарственные формы для небулайзерной терапии: БЕРОДУАЛ, АТРОВЕНТ, БЕРОТЕК, ВЕНТОЛИН — НЕБУЛЫ.
Занятие № 4
Тема: Лечение хронического воспаления при бронхиальной астме.
План занятия:
- Бронхиальная астма — хроническое воспалительное заболевание.
- Базисное лечение бронхиальной астмы.
- Интал, тайлед, дитек — механизмы действия, правила приема, применяемые дозы.
- Необходимость и обоснованность глюкокортикостероидов при бронхиальной астме.
- Показания для использования таблетированных и внутривенных стероидов.
- Показания и необходимость использования ингаляционных стероидных препаратов.
Реквизит: спинхалер, интал, тайлед, турбухалеры, дискхалеры, изихейлеры; ингаляторы «легкое дыхание», активируемые вдохом, мультидиск.
Бронхиальная астма — это хроническое воспалительное заболевание бронхиального дерева. В отличие от других хронических заболеваний воспаление при бронхиальной астме аллергическое. Каждый больной, прошедший обучение, должен это четко понимать. Также как и при любом другом хроническом заболевании (сахарный диабет, гипертоническая болезнь), обязательно соблюдение определенных мероприятий практически постоянно.
Базисное лечение астмы включает использование двух групп препаратов:
- ДИНАТРИЯ КРОМОГЛИКАТ (ИНТАЛ), НЕДОКРОМИЛ НАТРИЯ (ТАЙЛЕД), ДИТЭК — комбинированный препарат динатрия кромогликата и фенотерола, а также ингибиторы лейкотриеновых рецепторов:
- МОНТЕЛУКАСТ И ЗАФИРЛУКАСТ.
- ингаляционные и таблетированные глюкокортикостероиды.
Натрия кромогликат — препарат, применяемый для базисного лечения бронхиальной астмы. Он обладает мембраностабилизирующим действием (стабилизирует мембраны тучных клеток). Препарат выпускается в виде капсул, содержащих порошок интала, дозированного аэрозоля, глазных капель и капсул для перорального применения. Для ингаляций используют порошковую форму с помощью устройства СПИНХАЛЕР и ингаляторы с дозированными аэрозолями. Препарат эффективен при атопической астме и астме физического усилия. Если больной не находится в состоянии стойкой ремиссии, за 15-20 минут до приема интала необходимо сделать вдох бронходилятатора. Больным необходимо объяснять, что ИНТАЛ не применяется для снятия бронхоспазма.
Дитек (фенотерола гидробромид + динатрия кромогликат) комбинированный препарат, обладающий одновременно бронхолитическим и противовоспалительным действием. Применяется как для купирования приступа удушья, так и для профилактического лечения. Используется по 2 дозы 4 раза в день.
Тайлед (недокромил натрия) — препарат близкий по своей структуре к динатрию кромогликату, но обладающий более высокой противовоспалительной активностью. Выпускается в форме аэрозоля. Применяется по 2 дозы 2 раза в сутки.
Препараты зафирлукаст (АКОЛАТ) и монтелукаст (СИНГУЛЯР) выпускаются в таблетках и применяются в зависимости от степени тяжести течения бронхиальной астмы, чаще по 1 таблетке 2 раза в день. Они не являются гормональными препаратами.
По вопросам назначения гормональных препаратов всегда возникает множество вопросов. Часто назначение глюкокортикостероидов вызывает противодействие со стороны пациентов. Наиболее частые причины, которые называютпациенты: «Если я начну применять гормоны, то…
- окажусь привязанным к ним на всю жизнь и без них обходиться не смогу;
- растолстею;
- возможно развитие различных осложнений;
- не смогу оставаться нормальной женщиной, родить полноценного здорового ребенка;
- их прием скажется на моих мужских способностях».
И вытекающее из всего этого заблуждение — «Моя болезнь еще не так тяжела, и я вполне могу обходиться без гормонов». В основе подобного страха лежит незнание.
Прежде чем говорить о гормональных препаратах, необходимо рассказать больным о том, что гормоны вырабатываются в организме человека железами внутренней секреции и регулируют нормальное течение всех жизненных процессов. Избыток или недостаток разных гормонов приводит к тяжелым заболеваниям. Недостаток инсулина ведет к сахарному диабету, при избытке гормонов щитовидной железы развивается одна из форм зоба.
Из всех многочисленных видов гормонов, вырабатываемых организмом, для лечения бронхиальной астмы используется только одна группа — синтезируемые в надпочечниках КОРТИКОСТЕРОИДЫ. Глюкокортикоидные гормоны являются важнейшим средством лечения бронхиальной астмы, поскольку обладают мощным противовоспалительным действием. Здесь важно напомнить слушателям, что в основе астмы лежит воспаление. Необходимо продемонстрировать плакат и показать, что происходит с бронхами во время приступа бронхиальной астмы: сужение просвета за счет спазма, отека и образования секрета. На все компоненты воспаления гормоны оказывают влияние, поэтому их широко применяют в лечении астмы. В настоящее время рекомендуют использовать гормональные препараты уже на самых ранних стадиях заболевания, так как на поздних стадиях, несмотря на высокие дозы препаратов, не удается достичь желаемого результата. Причиной этого является гипертрофия мышц стенок бронхов на поздних стадиях течения бронхиальной астмы. Следовательно, целью лечения является предупреждение развития этих процессов путем длительного и эффективного снижения интенсивности воспаления в бронхах.
Правильность применения гормональных препаратов
При лечении бронхиальной астмы используют различные лекарственные формы гормональных препаратов.
Таблетки — в таблетированной форме выпускаются следующие наиболее часто используемые препараты: ПРЕДНИЗОЛОН, ПРЕДНИЗОН, ТРИАМЦИНОЛОН (полькортолон, берликорт, кенакорт), МЕТИЛПРЕДНИЗОЛОН (медрол, метипред), ДЕКСАМЕТАЗОН, ЦЕЛЕСТОН.
Эти препараты применяются в виде 2-х схем:
- назначают короткий курс при обострении астмы как правило в течение 7 — 10 дней в дозе от 4 до 8 таблеток в зависимости от массы больного и степени обострения. Короткие курсы, проводимые обычно при необходимости до 3-4 раз в год, практически не дают осложнений.
- длительный ежедневный прием таблеток назначают для постоянного контроля астмы в тех случаях, когда другие препараты неэффективны. Риск осложнений, связанный с лечением, в этом случае выше, чем при кратковременном приеме. Такой способ лечения применяется все реже, так как появились безопасные ингаляционные гормоны.
Инъекции гормональных препаратов — назначаются в условиях стационара при лечении острого тяжелого приступа астмы. Показания для пролонгированных гормонов при астме очень ограничены.
Ингаляционные препараты — созданы специально для лечения бронхиальной астмы. Это эффективные и безопасные средства для постоянного контроля симптомов заболевания. Их преимущества перед другими лекарственными формами гормонов в следующем: попадая непосредственно в легкие, оказывают местное действие, сконцентрированное только в легких, что, во-первых, повышает их эффективность, а во-вторых, в отличие от таблеток и инъекций, не действуют на другие органы и системы, то есть риск развития характерных для системного приема осложнений (прибавка в весе, повышение давления и др.) практически отсутствует.
Среди ингаляционных препаратов дольше всех применяется БЕКОТИД (беклометазона дипропионат) — около 30 лет. Это подтверждает его безопасность. Появились более современные и эффективные препараты, такие как ПУЛЬМИКОРТ, ФЛЮТИКАЗОН (ФЛИКСОТИД). В связи с большей эффективностью они применяются 1 — 2 раза в сутки.
Важно помнить, что в отличие от ингаляторов, содержащих бронхолитики (вентолин, беротек), ингаляционные препараты гормонов не помогают при остром приступе удушья, поэтому использовать их с этой целью не следует.
В последние годы появились комбинированные препараты для лечения бронхиальной астмы, которые содержат как бронхорасширяющее средство так и базисное, т.е. противовоспалительное. К таким препаратам относятся СЕРЕТИД МУЛЬТИДИСК (содержит серевент — бронхолитик продленного действия и гормональное средство — флютиказона пропионат — фликсотид). Специальное средство доставки — МУЛЬТИДИСК, в котором помещено 60 ингаляционных доз. Использование данного препарата с успехом контролирует течение тяжелой астмы, при этом назначение его осуществляется 2 раза в сутки.
Другим подобным препаратом является СИМБИКОРТ ТУРБУХАЛЕР (содержит ФОРМОТЕРОЛ — бронхолитик продленного действия и будесонид — гормональное средство).
При приеме ингаляционных препаратов для повышения эффективности их применения и снижения риска некоторых побочных эффектов также следует соблюдать определенные правила:
При наличии затрудненного дыхания или хрипов за 15-20 минут до приема предписанной врачом дозы препарата гормона рекомендуется сделать одну ингаляцию бронхолитика. Это расширит бронхи и приведет к более глубокому проникновению аэрозоля гормона в легкие.
После каждого применения ингаляционного гормона следует прополоскать рот и горло водой.
Идеальным является использование спейсера, облегчающего сам процесс ингаляции и способствующего лучшему проникновению препарата в легкие.
Осложнения при использовании ингаляционных гормонов очень редки. Это возникающая иногда осиплость голоса, а также очень редко — кандидоз (молочница). Клинические проявления кандидоза: чувство зуда, появление белесоватой пленки во рту. Это осложнение легко лечится, и, как правило, не требует отмены препарата. Использование спейсера и тщательное полоскание рта после ингаляции гормона сводят риск этих осложнений к минимальному.
Правильный прием ингаляционных препаратов гормонов в большинстве случаев позволяет успешно контролировать течение астмы, обходясь без назначения таблетированных гормонов, а при их приеме — снизить дозу, и даже полностью отказаться от их применения. Однако все манипуляции по снижению дозы и отмене препаратов должны проводиться под строгим врачебным контролем.
Применение гормональных препаратов у беременных с бронхиальной астмой
Как показывает практика, для развивающегося плода наибольшую опасность представляет недостаток кислорода, который развивается в том случае, если астма у беременной женщины плохо контролируется. Предпочтение при лечении астмы у беременных отдается ингаляционным препаратам гормонов, среди которых доказана безопасность бекотида, который при назначении в терапевтических дозах не оказывает повреждающего действия на плод.
Из таблетированных форм при беременности противопоказаны препараты триамцинолона, а также дексаметазон и бетаметазон. Однако окончательное решение о необходимости назначения, препарате и схеме лечения астмы у беременных — за врачом.
Занятие № 5
Тема: Лечение и профилактика вирусной инфекции
План занятия:
- Что такое вирусная инфекция? Виды вирусных инфекций.
- Лечение вирусных инфекций.
- Антибиотики в лечении бронхиальной астмы.
- Принципы профилактики вирусных инфекций.
- Причины обострений бронхиальной астмы.
- Симптомы обострения бронхиальной астмы.
- Принципы лечения и критерии обращения к врачу.
Реквизит: сумамед, рулид, клацид, макропен, спарфлоксацин, таваник, лазолван, амброгексал, халиксол, ИРС-19, бронхомунал, рибомунил.
Вирусная инфекция — частая причина обострения бронхиальной астмы, в связи с этим важно знать, как правильно лечиться во время вирусной инфекции, чтобы избежать обострения астмы. Пациентов рекомендуется познакомить с понятием «вирус» и «бактерия», перечислить основные виды вирусной инфекции — грипп, парагрипп, аденовирусная инфекция и т.д.
Следует рассказать об отличиях гриппа от других инфекций. Начало гриппа характеризуется высокой температурой (до 39-40°С), сильной головной болью, болью в глазных яблоках и мышцах. Затем присоединяются катаральные явления. Для других вирусных инфекций более характерно одновременное повышение температуры и появление катаральных явлений, а также менее выраженный интоксикационный синдром. Лечение гриппа проводится РЕМАНТАДИНОМ и эффективно только, если начато в первые 24 часа от появления первых симптомов гриппа. Во всех других случаях лечение данным препаратом не проводится. Среди других противовирусных препаратов можно назвать: амиксин, арбидол, зовиракс.
Необходимо напомнить слушателям, что при бронхиальной астме в стенке бронха постоянно протекает аллергическое воспаление, которое приводит к бронхоспазму, отеку стенки бронха и выделению густой слизи, что приводит к появлению одышки или удушья. Вирусы стимулируют этот процесс, и течение болезни может ухудшиться. Очень часто аллергическая или, как её часто называют, атопическая астма начинается именно с ОРВИ. Почему так происходит? Главной причиной является вирус, который способен проникать внутрь клеток, покрывающих стенки бронхов, вызывать гибель клеток и воспаление бронхов. На фоне уже протекающей астмы вирус приводит к обострению последней.
Какие необходимо дать советы человеку, болеющему астмой, если начался сезон ОРВИ?
Вирус передается воздушно-капельным путем. Обязательно носить марлевую маску, чтобы уберечь себя от попадания вируса в верхние дыхательные пути. Необходимо смазывать слизистую носа оксолиновой мазью перед выходом на улицу, чтобы помешать осесть вирусам на слизистую. После прихода домой необходимо прополоскать горло и нос водой.
Если в семье появился больной ОРВИ, необходимо изолировать его, поместив в отдельную комнату. Часто проветривать её, проводить влажную уборку. Пользоваться специально выделенной посудой.
Если у больного астмой возникло ОРВИ или грипп, необходимо рекомендовать следующее:
Удвоить дозу принимаемого ингаляционного противоастматического препарата, не дожидаясь обострения болезни. Проконсультироваться с врачом.
Необходимо вовремя распознать обострение болезни. Для этого надо регулярно проводить пикфлоуметрию, знать свой лучший результат. Снижение его свидетельствует о наступающем обострении. Другие признаки обострения болезни:
- постепенно усиливается чувство затрудненного дыхания, заложенности в грудной клетке, которые перерастают в одышку и удушье;
- появляются ночные симптомы болезни;
- ухудшается переносимость физических нагрузок;
- увеличивается потребность в бронхорасширяющих препаратах.
Во время гриппа и ОРВИ необходимо потребление повышенного количества жидкости. Следует подчеркнуть, что больным с аспириновой бронхиальной астмой нельзя принимать аспирин, анальгин и другие жаропонижающие и противовоспалительные средства. Не следует употреблять малину, мед, вишню и варенье из них.
Нельзя самостоятельно принимать антибиотики. Решение об их назначении принимает врач. При возникшей необходимости в приеме антибиотиков, когда появляется большое количество гнойной мокроты, назначаются антибиотики. Однако надо помнить, что больным с астмой, как правило, не следует назначать пенициллиновый ряд, так они могут вызвать серьезные аллергические реакции. Чаще рекомендуется назначение макролидов или фторхинолонов с антипневмококковой активностью.
При наличии трудноотделяемой вязкой мокроты рекомендуется использование муколитиков типа АМБРОКСОЛ (лазолван, амброгексал, халиксол). Их применение возможно с помощью небулайзерного ингалятора «Омрон», «Пари» и др.
Для специфической профилактики вирусных и бактериальных инфекций рекомендуется вакцинация против гриппа, а также бактериальные вакцины, такие как РИБОМУНИЛ, БРОНХОМУНАЛ, ИРС-19.
На данном занятии пациентам рассказывается о причинах обострения астмы. Они следующие и о них каждый больной астмой должен хорошо знать:
- Контакт с аллергеном вызывает приступ астмы (контакт с кошкой в гостях, приезд в сельский дом и т.д.);
- Инфекция вирусная или бактериальная;
- Снижение дозы гормональных ингаляционных препаратов или их самовольная отмена при хорошем самочувствии;
- Неадекватно подобранная терапия;
- Физическая нагрузка;
- Смена климата;
- Прием лекарственных средств (НПВС, антибиотики);
- Нервный стресс.
Если больной прошел занятия в астма-школе, он может грамотно воспользоваться полученными знаниями, реже обращается за помощью к врачу.
Критериями посещения врача являются:
- Частые обострения.
- Снижение показателей пикфлоуметрии.
- Необходимость замены лекарственных препаратов.
Правила использования дозированного ингалятора
На
занятии пациенты обучаются технике
применения дозированных ингаляторов.
В начале занятия одному – двум больным
предлагается продемонстрировать технику
пользования ингалятором. Как показывает
практика, только единичные больные
могли правильно продемонстрировать
технику использования ингалятора. Как
правило, больные делают одни и те же
принципиальные ошибки: не делают
предварительный выдох, не четко
синхронизируют начало вдоха и нажатие
на дно баллончика и т. д. После этого
преподаватель рассказывает правильную
технику ингаляций и сам её демонстрирует
(с этой целью используется плацебо).
Важно,
чтобы больные освоили правильную
технику ингаляции:
-
встряхнуть
ингалятор; -
снять
защитный колпачок; -
повернуть
ингалятор вверх дном; -
сделать
полный выдох через слегка сомкнутые
губы; -
плотно
обхватить мундштук ингалятора губами; -
начиная
делать вдох, нажать на дно ингалятора
и глубоко вдохнуть лекарство (при этом
должно возникнуть ощущение, что лекарство
не осталось во рту, а попало в бронхи); -
задержать
дыхание на 10 секунд; -
сделать
спокойный выдох; -
надеть
на ингалятор защитный колпачок.
В
настоящее время рекомендуется использовать
пластиковые камеры – спейсеры,
особенно тем, кто плохо синхронизирует
вдох и нажатие на дно баллончика.
Правила пользования спейсером:
-
удалить
защитный колпачок, встряхнуть ингалятор
и вставить его в спейсер; -
обхватить
губами ротовой конец спейсера; -
нажать
на ингалятор, чтобы лекарство попало
в спейсер; -
глубоко
и медленно сделать вдох; -
задержать
дыхание на 10 секунд, затем выдохнуть
через ротовой конец; -
повторить
вдох, не нажимая на ингалятор; -
отсоединиться
от спейсера; -
выждать
30 секунд, затем (при необходимости)
впрыснуть вторую дозу аэрозоля и
повторить все вышеперечисленные
действия.
В
конце занятия больных обучают проведению
бронхолитического теста. Для этого
предлагается тем пациентам, у кого
имеется пикфлоуметр, провести трехкратное
измерение ПСВ, при этом оценивая
правильность выполнения маневра. Затем,
при наличии сниженных показателей
проводится ингаляция бронхолитического
препарата (беротек или сальбутамол) с
использованием спейсера. Повторное
измерение ПСВ осуществляется через 15
минут и вычисляется прироста ПСВ. Если
прирост скорости составил 15% и более,
считается, что тест положительный,
который свидетельствует о наличии у
пациента бронхоспазма, что требует
применения бронхорасширяющего средства.
Всем пациентам рекомендуется проводить
такой тест каждое утро, отмечая показатели
на графике пикфлоуметрии для того, чтобы
оценить степень бронхоспазма и
необходимость применения бронхолитика.
Занятие № 3
План
занятия:
-
Основные
группы препаратов, использующиеся в
ингаляторах. -
Симптоматическая
бронхолитическая терапия. -
Принципы
подбора ингалятора. -
Применяемые
дозы и симптомы передозировки.
Реквизит:
ингаляторы
дозированные:
вентолин, беротек Н, атровент, беродуал
Н;
дискхалеры:
вентолин, серевент;
турбухалер:
бриканил;
аэролайзер:
форадил, небулайзер.
Для
того чтобы слушателям были понятны
механизмы действия бронхолитических
препаратов, необходимо дать краткую
информацию о механизмах регуляции
тонуса бронхов у человека; рассказать
о симпатическом и парасимпатическом
отделе вегетативной нервной системы,
о медиаторах адреналине и ацетилхолине
и тех клинических эффектах, которые они
вызывают при воздействии на бронхи и
сердечно-сосудистую систему. Исходя из
этих механизмов, приводятся сведения
о группах бронхолитических средств,
которые применяются на сегодняшний
день.
Важно
подчеркнуть, что при
бронхиальной астме существует два вида
лечения:
-
симптоматическое,
применяющееся главным образом для
купирования приступа (симпатомиметики,
холинолитики и ксантины); -
базовое
– противовоспалительное
(ингаляционные стероиды, антагонисты
лейкотриеновых рецепторов и кромоны).
Обычно
у пациентов сразу возникает множество
вопросов по названиям препаратов. Надо
сразу отвечать, не вдаваясь в подробности
и не давая индивидуальных рекомендаций
по лечению, так как это дело лечащего
врача. Необходимо донести до каждого
больного принципиальное отличие базисных
противовоспалительных препаратов от
бронходилататоров. Опыт показывает,
что не весь материал, изложенный на
предыдущих занятиях, одинаково хорошо
усваивается всеми больными, поэтому
надо чаще возвращаться к тем вопросам,
которые вызвали непонимание с первого
раза.
Больной
должен знать, что подбирать лечение
больному должен врач. Вредно пользоваться
советами окружающих, т.к. существуют
разные формы бронхиальной астмы и,
соответственно, используется разное
лечение. Однако, если трудно вовремя
получить совет врача или при дефиците
лекарств в аптеках, больные должны
знать, какие ингаляторы являются
взаимозаменяемыми.
Желательно,
чтобы больные записали группы ингаляторов
по механизму действия. Симпатомиметики:
ФЕНОТЕРОЛ
(беротек), САЛЬБУТАМОЛ
(вентолин, саламол), ТЕРБУТАЛИН
(бриканил).
Холинолитики:
ипратропиум бромид –
АТРОВЕН, ТРОВЕНТОЛ.
Комбинированный
препарат:
БЕРОДУАЛ,
КОМБИВЕНТ.
Препараты
продленного действия
– САЛЬМЕТЕРОЛ
(СЕРЕВЕНТ), ФОРМОТЕРОЛ (ФОРАДИЛ, ОКСИС),
ТИОТРОПИЯ БРОМИД (СПИРИВА).
Понимание
– какие ингаляторы являются
взаимозаменяемыми – достигается путем
тренинга. Эффект от применения
дозированного ингалятора больной может
самостоятельно оценить с помощью
динамической пикфлоуметрии и
бронхолитического теста.
На
этом же занятии больным необходимо
рассказать о бесфреоновых формах
ингаляционных средств, о том, что в
составе БЕРОТЕКА
Н И БЕРОДУАЛА Н
содержится другой носитель лекарства,
который в отличие от фреона не разрушает
защитный озоновый слой земли и имеет
необычный запах, напоминающий алкоголь,
хотя по механизму действия и эффективности
не отличается от обычного беротека и
беродуала. К использованию новых форм
лекарств следует привыкать, так как на
фреоновой основе препараты в ближайшее
время выпускаться не будут.
Каждый
больной использует индивидуально
подобранную дозировку лекарственных
препаратов. Важно
подчеркнуть, что повышение кратности
применения бронхорасширяющего препарата
свидетельствует об обострении болезни
или неадекватно подобранном лечении.
Основные
побочные действия бронходилататоров:
тахикардия,
мышечный тремор, психомоторное
возбуждение. Побочные действия больше
выражены у симпатомиметиков неселективного
действия: ИЗАДРИНА,
АЛУПЕНТА, АСТМОПЕНТА.
При проявлении таких эффектов желательно
снизить
дозу
или
поменять
дозированный ингалятор.
Побочные
действия атровента, связанные с его
атропиноподобным действием, встречаются
редко. Важно все время акцентировать
внимание слушателей на соблюдении
правильной техники ингаляций и наиболее
частых ошибках при использовании
дозированных аэрозолей:
-
делают
два нажатия ингалятора подряд, после
этого вдыхая препарат один раз; -
не
задерживают дыхание на вдохе.
Рекомендуется
постоянно напоминать о том, насколько
они правильно пользуются карманным
ингалятором, ведь от этого зависит его
эффективность.
Слушатели
часто задают вопрос о том, существует
ли привыкание к ингалятору и не может
ли возникнуть ситуация, когда без него
уже невозможно будет обойтись?
На
этот вопрос следует отвечать следующим
образом. Лекарства,
которые находятся в ингаляторах,
привыкания не вызывают.
Другое дело, что течение бронхиальной
астмы при неполном, неправильном лечении
может быть таково, что постоянные
обострения вынуждают больного прибегать
к помощи ингалятора слишком часто.
Частое использование ингалятора (больше
3-4 ингаляций в сутки) говорит о том, что
контроль над астмой неполный, и является
сигналом, что следует обратиться к
врачу, чтобы пересмотреть программу
лечения.
Другой
частый вопрос: чем ингаляторы лучше
других препаратов, например эуфиллина
или теофедрина?
Эуфиллин
и содержащий эуфиллин препарат теофедрин
также относятся к препаратам, расширяющим
бронхи, но применяются либо в виде
инъекций (эуфиллин), либо таблеток
(эуфиллин и теофедрин). Современные
ингаляционные препараты попадают при
ингаляции непосредственно в легкие.
Вследствие этого:
-
именно
в легких создается высокая концентрация
лекарства; -
они
быстрее оказывают свое действие; -
концентрируясь
в легких, эти препараты при правильном
применении практически не оказывают
влияния на другие органы.
Принятой
таблетке, чтобы подействовать, надо
попасть в желудок, там раствориться,
всосаться, с током крови попасть в легкие
– причем туда попадает только маленькая
её часть, а основная масса разнесется
по всему организму. Эуфиллин в инъекциях
применяют для лечения приступа астмы,
но эту процедуру, в отличие от ингаляции,
сам больной выполнить не может.
Однако
это не значит, что эти препараты в лечении
бронхиальной астмы не стоит использовать.
Эуфиллин в виде таблеток, особенно его
пролонгированные (длительнодействующие)
препараты (теопэк, теотард, ретафил и
др.) успешно применяются для постоянной
терапии астмы, однако при лечении острого
приступа ингаляторы предпочтительнее.
Ведь для того, чтобы таблетка оказала
свое действие, требуется время.
На
занятии демонстрируются различные
формы доставки лекарственных
бронхолитических препаратов. Так,
препарат ВЕНТОЛИН
(сальбутамол)
выпускается в виде порошка. Упакованный
в виде дисков, он называется
ВЕНТОДИСК,
вдыхается через специальное распыляющее
устройство –
ДИСКХАЛЕР.
При использовании этого устройства
необходим активный вдох, только при
таком условии препарат попадет в легкие.
Существует форма вентолина
в таблетках, выпускаемая под названием
ВОЛЬМАКС,
для детей в дозе 4 мг, а для взрослых 8
мг. Применяется 2 раза в день.
Продленного
действия лекарственный препарат
САЛЬМЕТЕРОЛ
выпускается как в виде ингалятора, так
и в виде порошка – дискхалера. ФОРМОТЕРОЛ
или ФОРАДИЛ
—
бронхолитик длительного действия,
применяется в виде порошка, доставка
которого осуществляется с помощью
АЭРОЛАЙЗЕРА.
Двукратный прием в течение суток помогает
успешно контролировать бронхиальную
астму.
В
конце занятия пациентам рассказывается
о принципах более интенсивной терапии
бронхоспастического синдрома с помощью
небулайзерного ингалятора, о понятии
небулизации (способ превращения жидкой
лекарственной формы с помощью струи
воздуха или ультразвука в туманообразное
состояние). Представляются жидкие
лекарственные формы для небулайзерной
терапии: БЕРОДУАЛ,
АТРОВЕНТ, БЕРОТЕК, ВЕНТОЛИН – НЕБУЛЫ.
ЗАНЯТИЕ
№ 4
ЛЕЧЕНИЕ
ХРОНИЧЕСКОГО ВОСПАЛЕНИЯ ПРИ БРОНХИАЛЬНОЙ
АСТМЕ
План
занятия:
-
Бронхиальная
астма – хроническое воспалительное
заболевание. -
Базисное
лечение бронхиальной астмы. -
Интал,
тайлед, дитек – механизмы действия,
правила приема, применяемые дозы. -
Необходимость
и обоснованность глюкокортикостероидов
при бронхиальной астме. -
Показания
для использования таблетированных и
внутривенных стероидов. -
Показания
и необходимость использования
ингаляционных стероидных препаратов.
Реквизит:
спинхалер, интал, тайлед, турбухалеры,
дискхалеры, изихейлеры; ингаляторы
«легкое дыхание», активируемые вдохом,
мультидиск.
Бронхиальная
астма
– это хроническое воспалительное
заболевание бронхиального дерева. В
отличие от других хронических заболеваний
воспаление при бронхиальной астме
аллергическое.
Каждый больной, прошедший обучение,
должен это четко понимать. Также как и
при любом другом хроническом заболевании
(сахарный диабет, гипертоническая
болезнь), обязательно соблюдение
определенных мероприятий практически
постоянно.
Базисное
лечение астмы включает использование
двух групп препаратов:
-
ДИНАТРИЯ
КРОМОГЛИКАТ (ИНТАЛ), НЕДОКРОМИЛ НАТРИЯ
(ТАЙЛЕД), ДИТЭК
– комбинированный препарат динатрия
кромогликата и фенотерола, а также
ингибиторы лейкотриеновых рецепторов:
МОНТЕЛУКАСТ
И ЗАФИРЛУКАСТ. -
ингаляционные
и таблетированные глюкокортикостероиды.
Натрия
кромогликат
– препарат, применяемый для базисного
лечения бронхиальной астмы. Он обладает
мембраностабилизирующим действием
(стабилизирует мембраны тучных клеток).
Препарат выпускается в виде капсул,
содержащих порошок интала, дозированного
аэрозоля, глазных капель и капсул для
перорального применения. Для ингаляций
используют порошковую форму с помощью
устройства СПИНХАЛЕР
и ингаляторы с дозированными аэрозолями.
Препарат эффективен при атопической
астме и астме физического усилия. Если
больной не находится в состоянии стойкой
ремиссии, за 15-20 минут до приема интала
необходимо сделать вдох бронходилятатора.
Больным необходимо объяснять, что ИНТАЛ
не применяется для снятия бронхоспазма.
Дитек
(фенотерола
гидробромид + динатрия кромогликат)
комбинированный препарат, обладающий
одновременно бронхолитическим и
противовоспалительным действием.
Применяется как для купирования приступа
удушья, так и для профилактического
лечения. Используется по 2 дозы 4 раза в
день.
Тайлед
(недокромил
натрия) – препарат близкий по своей
структуре к динатрию кромогликату, но
обладающий более высокой противовоспалительной
активностью. Выпускается в форме
аэрозоля. Применяется по 2 дозы 2 раза в
сутки.
Препараты
зафирлукаст (АКОЛАТ)
и монтелукаст (СИНГУЛЯР)
выпускаются в таблетках и применяются
в зависимости от степени тяжести течения
бронхиальной астмы, чаще по 1 таблетке
2 раза в день. Они не являются гормональными
препаратами.
По
вопросам назначения гормональных
препаратов всегда возникает множество
вопросов. Часто назначение
глюкокортикостероидов вызывает
противодействие со стороны пациентов.
Наиболее частые причины, которые
называютпациенты: «Если я начну применять
гормоны, то
-
окажусь
привязанным к ним на всю жизнь и без
них обходиться не смогу; -
растолстею;
-
возможно
развитие различных осложнений; -
не
смогу оставаться нормальной женщиной,
родить полноценного здорового ребенка; -
их
прием скажется на моих мужских
способностях».
И
вытекающее из всего этого заблуждение
– «Моя болезнь еще не так тяжела, и я
вполне могу обходиться без гормонов».
В основе подобного страха лежит незнание.
Прежде
чем говорить о гормональных препаратах,
необходимо рассказать больным о том,
что гормоны вырабатываются в организме
человека железами внутренней секреции
и регулируют нормальное течение всех
жизненных процессов. Избыток или
недостаток разных гормонов приводит к
тяжелым заболеваниям. Недостаток
инсулина ведет к сахарному диабету, при
избытке гормонов щитовидной железы
развивается одна из форм зоба.
Из
всех многочисленных видов гормонов,
вырабатываемых организмом, для лечения
бронхиальной астмы используется только
одна группа – синтезируемые в надпочечниках
КОРТИКОСТЕРОИДЫ.
Глюкокортикоидные гормоны являются
важнейшим средством лечения бронхиальной
астмы, поскольку обладают мощным
противовоспалительным действием.
Здесь важно напомнить слушателям, что
в основе астмы лежит воспаление.
Необходимо продемонстрировать плакат
и показать, что происходит с бронхами
во время приступа бронхиальной астмы:
сужение просвета за счет спазма, отека
и образования секрета. На все компоненты
воспаления гормоны оказывают влияние,
поэтому их широко применяют в лечении
астмы. В настоящее время рекомендуют
использовать гормональные препараты
уже на самых ранних стадиях заболевания,
так как на поздних стадиях, несмотря на
высокие дозы препаратов, не удается
достичь желаемого результата. Причиной
этого является гипертрофия мышц стенок
бронхов на поздних стадиях течения
бронхиальной астмы. Следовательно,
целью лечения является предупреждение
развития этих процессов путем длительного
и эффективного снижения интенсивности
воспаления в бронхах.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Ингаляционная терапия является краеугольным камнем лечения астмы, а доставка лекарства непосредственно в бронхи обеспечивает оптимальную эффективность и безопасность. Тем не менее, по данным разных исследований более половины пациентов с астмой неправильно используют свои ингаляторы и им требуется специальное обучение, чтобы поддерживать свою технику.
Ниже мы приводим информацию об основных типах ингаляторов и доставочных устройств, которые используются для лечения астмы и особенности их применения:
ДАИ – дозированный аэрозольный ингалятор – самый распространенный и популярный тип доставочного устройства для аэрозоля. Достоинствами ДАИ являются их удобство, портативность, быстрота обращения с ними, низкая стоимость. Для высвобождения дозы препарата необходимо нажатие на дно аэрозольной канистры, в результате чего происходит декомпрессия субстанции внутри клапана дозирующей камеры. Это требует одновременной активации устройства и вдоха, то есть координации «больной-ингалятор». Оптимальной ингаляционной техникой является медленный вдох с последующей задержкой дыхания до 10 с.
Правильная техника ингаляции и ошибки, допускаемые пациентами при использовании ДАИ.
| Встряхнуть ингалятор (в случае суспензии) | Выполнить одну активацию ингалятора во время вдоха |
| Произвести полный выдох перед активацией ингалятора | Вдыхать глубоко и медленно (не прерывать вдох сразу после активации ингалятора) |
| Держать ингалятор вертикально донышком вверх | Вдыхать через рот |
| Разместить загубник между губами, поверх языка, не перекрывая просвет | Задержать дыхание на 10 с на высоте вдоха |
У детей (особенно до 6-7 летнего возраста) и ослабленных пациентов ДАИ нужно использовать со спейсером.
Cпейсер – представляет собой объемную камеру, которая соединяет дозированный ингалятор и дыхательные пути больного. Спейсеры позволяют решать проблемы координации вдоха пациента и высвобождения лекарственного препарата, а также уменьшать оседание препарата на задней стенке глотки из-за высокой скорости потока, с которым препарат попадает в дыхательные пути, и связанные с ней местные побочные эффекты. делает возможным их применение у пациентов практически всех возрастных категорий, включая и детей. Оптимальной техникой ингаляции аэрозоля через спейсер является глубокий медленный вдох, или два спокойных глубоких вдоха после высвобождения одной дозы в камеру небулайзера, или даже обычное спокойное дыхание (для детей).
ДПИ – дозированный порошковый ингалятор – более современное устройство доставки препаратов от астмы. В ДПИ лекарство используются в виде порошка. Для оптимальной ингаляции при использовании ДПИ необходим максимально мощный и быстрый вдох, чтобы преодолеть внутреннее (создаваемое устройством) сопротивление потоку и генерировать турбулентные потоки для формирования мелких лекарственных частиц. К преимуществам ДПИ относятся их портативность, компактность, удобство и относительная простота использования. Большой плюс при использовании ДПИ – отсутствие необходимости координировать вдох с нажатием на устройство.
ДПИ бывают однодозовые и мультидозовые. В однодозовых ДПИ активный препарат находится внутри желатиновой капсулы, которая перед каждой ингаляцией перфорируется специальными иглами. В резервуарных мультидозовых ДПИ препарат находится в едином контейнере, а каждая ингаляционная доза отмеряется с помощью специального дозирующего устройства. Данный тип ДПИ отличается максимальным удобством для больного: ингалятор содержит до 60–200 доз, требует минимальной подготовки для использования и может применяться в экстренных ситуациях.. В мультидозовых блистерных ДПИ используется несколько запакованных в блистеры доз. Но ошибки при использовании всех типов ДПИ похожи и представлены в таблице.
Техника ингаляции и ошибки, допускаемые пациентами при использовании ДПИ
| Удалить / повернуть крышку | Разместить загубник между губами |
| Вставить капсулу | Вдыхать глубоко (не прерывать вдох сразу после активации ингалятора) |
| Проколоть капсулу | Вдыхать быстро (форсированный вдох) |
| Правильно загрузить дозу | Вдыхать через рот (не через нос) |
| Держать ингалятор вертикально | Задержать дыхание на высоте вдоха |
| Произвести полный выдох (не в ингалятор | Выдохнуть не через загубник ингалятора |
При назначении ингаляционной терапии в нашем центре врачи учитывают возраст, индивидуальные особенности течения заболевания и обязательно рассказывают об особенностях применения каждого препарата и доставочного устройства. Если вы сомневаетесь в правильности использования вашего препарата при астме – врачи нашего центра помогут вам. Ведь с правильной техники ингаляции начинается успех в лечении астмы и контроль над заболеванием.
Подробнее о еще одном ультранеобходимом девайсе при астме, особенно в остром периоде астмы – небулайзере – можно познакомиться в статье «Для чего нужен небулайзер». Использование небулайзеров является более простым методом терапии, не требует обучения пациента дыхательному маневру и контроля врача за техникой ингаляции.
Используются изображения от Freepik
Tags: Бронхиальная астмаингалятор