Л.А.Горячкина, О.С.Дробик, М.Ю.Передельская
Кафедра клинической аллергологии РМАПО, Москва
В настоящее время бронхиальная астма (БА) является одной из важных проблем здравоохранения, решение которой вынуждает государство идти на большие экономические затраты, обусловленные в первую очередь длительной и дорогостоящей медикаментозной терапией, а также оказанием экстренной и стационарной помощи, мероприятиями по реабилитации инвалидов и пр. [10]. Кроме того, астма ассоциирована с существенным снижением качества жизни пациента, членов его семьи и родственников, что делает изучение истинной распространенности болезни актуальной задачей современной медицины. БА отличается многообразием клиники и функциональных проявлений, особенностями течения и нередко сочетается с другими заболеваниями легких. В последние годы отмечен значительный прогресс в диагностике и лечении данного заболевания. В тоже время известно, что дифференциальная диагностика бронхиальной астмы иногда вызывает у практических врачей трудности и приводит к ошибкам как в постановке диагноза БА, так и в тактике ведения больных. Наиболее часто приходится сталкиваться с проблемой гиподиагностики данного заболевания, которая является повсеместной: заболевание не выявляется вовсе или подменяется другим диагнозом, и, как следствие, пациенты не получают своевременно базисной терапии, заболевание прогрессирует, что приводит к хронизации и развитию тяжелых осложнений, инвалидности. Тем не менее, во врачебной практике также имеет место и гипердиагностика бронхиальной астмы. Наиболее часто ошибочный диагноз БА устанавливается больным с ХОБЛ, трахеобронхиальной дискинезией, бронхоэктатической болезнью, гипервентиляционным синдромом, наследственным дефицитом a1-антитрипсина, карциноидным синдромом, опухолями дыхательного аппарата и пр. Не стоит так же забывать о том, что пациенты, страдающие БА, часто отягощены и другой соматической патологией и могут предъявлять жалобы на дыхательный дискомфорт, не связанный с основным заболеванием [10, 11].
Бронхиальная астма – хроническое воспалительное заболевание дыхательных путей, в котором принимают участие многие клетки и клеточные элементы. Хроническое воспаление приводит к гиперреактивности дыхательных путей, что, в свою очередь, вызывает повторные эпизоды свистящих хрипов, одышки, чувства стеснения в груди и кашля, особенно ночью и/или ранним утром. Эти эпизоды обычно связаны с распространенной, но вариабельной бронхиальной обструкцией, которая нередко обратима спонтанно или под влиянием лечения (Глобальная стратегия лечения и профилактики бронхиальной астмы, 2007).
При диагностике бронхиальной астмы необходим в первую очередь подробный сбор жалоб и анамнеза больного. Чаще всего имеют место жалобы на эпизодические приступы удушья, одышки, появление свистящих хрипов, ощущение тяжести в грудной клетке, а также кашель. Необходимо уточнить триггеры, запускающие приступ удушья. Весьма характерно волнообразное течение болезни, нередко сезонность обострений. При сборе анамнеза обязательным является выявление атопии у пациента и его родственников, наличие у больного сопутствующего аллергического ринита, атопического дерматита, профессиональных вредностей, климатической зоны проживания пациента. При физикальном обследовании следует помнить, что в связи c приступообразностью течения болезни врач на осмотре не всегда может выявить симптомы. Чаще всего при обострении регистрируется экспираторная одышка, раздутие крыльев носа при вдохе, прерывистая речь, возбуждение, включение вспомогательной дыхательной мускулатуры, положение ортопноэ, постоянный или прерывающийся кашель, сухие свистящие хрипы в легких при аускультации. Важным диагностическим маркером бронхиальной астмы является исчезновение симптомов спонтанно или после применения бронходилататоров и противовоспалительных противоастматических препаратов. Обязательным в диагностике является исследование функции внешнего дыхания, и определения ее колебания, в том числе в течение суток (пикфлуометрия). Основными оцениваемыми показателями для диагностики и дифференциальной диагностики БА являются определение объема форсированного выдоха за 1 секунду (ОФВ1) и связанной с ним форсированной жизненной емкости легких (ФЖЕЛ), а также измерение форсированной (пиковой) скорости выдоха (ПСВ). Важным диагностическим критерием является тест для определения обратимости бронхиальной обструкции, который используется для исследования реактивности дыхательной системы: прирост показателей бронхиальной проходимости считается достоверным при увеличении ОФВ1 на 12% или 200 мл после ингаляции b2-агонистов короткого действия [3]. Вспомогательным методом диагностики БА, к сожалению, доступным на сегодняшний момент только в специализированных отделениях является неинвазивное измерение маркеров воспаления дыхательных путей. Неинвазивными маркерами воспаления при БА являются уровни выделяемого оксида азота (NO) или окиси углерода (СО). Оценка воспаления дыхательных путей также может быть выполнена путем исследования мокроты на наличие эозинофилов и метахроматических клеток. Безусловно, важна для определения атопического фенотипа БА оценка аллергологического статуса пациента путем проведения кожных скарификационных проб или измерение уровня специфических IgE крови.
При дифференциальной диагностике наибольшую сложность представляют больные с ХОБЛ. Для пациентов данной группы характерна постоянная, мало меняющаяся симптоматика. Мокрота выделяется в небольшом количестве (редко более 60 мл/сут) утром, имеет слизистый характер. Хронический кашель и продукция мокроты часто на много лет предшествуют развитию ограничения воздушного потока, хотя не у всех пациентов с продуктивным кашлем развивается ХОБЛ [2]. Диагноз ХОБЛ должен быть заподозрен у всех пациентов с наличием кашля, продукции мокроты, одышки, воздействием факторов риска в анамнезе. Клиническое обследование обнаруживает приступообразность симптоматики при БА, нередко в сочетании с экстрапульмональными признаками аллергии (риниты, конъюнктивиты, кожные проявления, пищевая аллергия). Для больных ХОБЛ характерна постоянная, мало меняющаяся симптоматика. Диагноз подтверждается с помощью спирометрических методов. Функция внешнего дыхания характеризуется обструктивным типом вентиляционных нарушений, проявляющихся прогрессирующим снижением максимальной скорости выдоха из-за возрастающего сопротивления в дыхательных путях, и постепенным ухудшением газообменной функции легких, что указывает на необратимый характер обструкции дыхательных путей. Величина постбронходилатационного ОФВ1 менее 80% от должных величин в сочетании с отношением ОФВ1/ФЖЕЛ (форсированная жизненная емкость легких) менее 70% подтверждает наличие частично необратимых обструктивных изменений. Важным элементом дифференциальной диагностики является снижение ОФВ1 на 50 мл и более в год у больных ХОБЛ, чего не наблюдается при БА.
При БА обычны высокие приросты воздушных объемов, демонстрируется положительный бронхолитический тест, а при ХОБЛ этого не наблюдается. Эта проба входит в критерии дифференциальной диагностики ХОБЛ, так как бронхиальная обструкция при ХОБЛ неуклонно прогрессирует и обратима лишь частично [6, 9].
Гипервентиляционный синдром проявляется развитием целого ряда вегетативных признаков, среди которых головокружение и ощущение приближающего обморока; болезненное ощущение сердцебиения и страх смерти; затруднение дыхания и страх удушья. Гипервентиляционный синдром всегда протекает с ярко выраженной эмоциональной окрашенностью. Одышка при гипервентиляционном синдроме, воспринимаемая самим пациентом как крайне тяжелая, может не соответствовать объективным данным и показателям функции внешнего дыхания. Диагностическое значение приобретает факт, что этот синдром может быть воспроизведен или в развернутой клинической картине, или же частично при проведении произвольного теста на гипервентиляцию. Основным критерием постановки диагноза является установление самого факта гипервентиляции, что возможно осуществить при исследовании функции внешнего дыхания [4]. Второй классический признак гипервентиляционного синдрома – пониженная концентрация углекислоты в крови, т.е. феномен гипокапнии [15]. Бронхиальную астму может симулировать одышка психогенного патогенеза. Такие псевдоастматические приступы возможны у больных с неврозами и психическими заболеваниями (шизофрения). Подобные состояния при дыхательном неврозе характеризуются чувством нехватки воздуха, невозможности сделать глубокий вдох [13]. Дыхание периодически становится частым, форсированным, т. е. выражены признаки гипервентиляционного синдрома. В отличие от бронхиальной астмы у больных отсутствуют характерно физикальные изменения в легких, функциональные признаки бронхиальной обструкции, а бронхолитические препараты не приносят облегчения. Дыхательные неврозы иногда развиваются после перенесенных ранее заболеваний органов дыхания.
Трахеобронхиальная дискенезия. Кашель является главным симптомом при данном заболевании. Он имеет свои клинические особенности: резистентный к терапии, приступообразный, «лающий», «дребезжащий» или «трубный», звонкий, иногда битонального тембра, практически без выделения мокроты – сухой. Кашель провоцируется изменением позы (резкими наклонами или поворотами головы), положением на животе, форсированием дыхания как на выдохе, так и на вдохе, смехом, напряжением, поступлением в верхние дыхательные пути холодного воздуха, газов-ирритантов, глотанием грубой пищи, жидкости (особенно холодной) или большого пищевого комка. Часто на высоте кашлевого пароксизма появляются головокружение, удушье с затруднением вдоха (чаще) или выдоха (реже), недержание мочи. При тяжелом течении болезни может развиться так называемый кашле-обморочный синдром [12, 14].
Дефицит a1-антитрипсина. a1-антитрипсин – низкомолекулярный протеазный ингибитор, подавляющий активность многих протеолитических знзимов: трипсина, химотрипсина, плазмина, тромбина, эластазы, гиалуронидазы, протеаз лейкоцитов, макрофагов, микроорганизмов и др. Дефицит его приводит к повышенному накоплению протеолитических энзимов и последующему повреждению тканей. В отношении патогенеза поражения легких наиболее признанной является теория нарушения протеазно-антипротеазного равновесия. Эксперименты показали, что a1-антитрипсин защищает легочную ткань от протеаз, высвобождаемых лейкоцитами, и тем самым сохраняет структурную целостность эластина. Можно предположить, что к эмфиземе легких приводит хроническое воспаление (вследствие инфекции или загрязнения воздуха), поскольку при данном заболевании легочная ткань ничем не защищена от протеаз лейкоцитов, привлеченных в воспалительный очаг. Замещаясь соединительной тканью, паренхима легких со временем теряет свою эластичность; развиваются обструктивные явления; формируется эмфизема, которая возникает первично, на фоне хронического бронхита или другого хронического неспецифического заболевания легких. Чаще всего расширяется весь ацинус, и эмфизема характеризуется как панацинарная. Заболевание начинается в молодом возрасте и характеризуется прогрессирующей эмфиземой, однако могут наблюдаться рецидивирующий обструктивный синдром, рецидивирующий бронхит, повторные пневмонии. Симптомы a1-антитрипсинзависимой эмфиземы легких обычно не появляются до третьего десятилетия жизни [8, 16].
Гастроэзофагеальная рефлюксная болезнь (ГЭРБ) может как имитировать симптомы бронхиальной астмы (особенно ночные), так и встречаться у больных БА [7]. ГЭРБ может играть роль в формировании картины бронхиальной астмы как за счет прямой аспирации желудочного содержимого, так и по механизму рефлекторных связей. Присоединение гастроэзофагеального рефлюкса ухудшает течение бронхиальной астмы, по данным некоторых авторов, в 25% случаев [7]. По ряду сообщений, у пациентов с ночными симптомами астмы данная болезнь встречается в 60% случаев.
Гастроэзофагеальный рефлюкс сопровождается кашлем, рвотой, нередко одышкой, что напоминает картину бронхиальной астмы. Для верификации диагноза требуется эндоскопическое исследование. Фиброгастроскопия и типичный анамнез поражения желудка и пищевода позволяют исключить бронхиальную астму, несмотря на заброс пищи в дыхательные пути [5].
Среди заболеваний, напоминающих бронхиальную астму, описаны поражения трахеи, гортани и бронхов, в частности папиллома гортани, бронхов, аденома бронхов. Различные пороки развития бронхов, сосудов, сдавливая дыхательные пути могут вызвать бронхиальную обструкцию, что ошибочно принимают за бронхиальную астму. Симулировать картину бронхиальной астмы может туберкулез легких и бронхов (туморозный бронхоаденит, туберкулез бронха), а также желудочно-пищеводной рефлюкс, инородное тело бронхов. Для исключения вышеперечисленной патологии необходим тщательный сбор анамнеза заболевания и обследование пациента с применением современных диагностических методов.
Учитывая сложность диагностического процесса при БА, необходимости использования современных средств диагностики, считаем небезынтересным представить описание случаев диагностической ошибки, основой которой был первично поверхностно собранный анамнез, не подтвержденный клинико-функциональными методами обследования.
Клинический пример 1
Больная Л., 55 лет, находилась на лечении в аллергологическом отделении ГКБ№ 52 весной 2010 г.
Поступила с жалобами на одышку, сухой приступообразный кашель без отхождения мокроты. Из анамнеза: с раннего детского возраста беспокоят часто рецидивирующие затяжные бронхиты, неоднократно переносила пневмонии. С 2003 г. пациентка стала отмечать появления приступов одышки, в 2006 г. установлен диагноз бронхиальная астма. В качестве базисной терапии получала ИГКС в средних и высоких дозах без клинического улучшения, в 2009 г. назначен Симбикорт 4,5/160 мкг по 2 вдоха 2 раза в день, на фоне чего сохраняются симптомы заболевания. Обострение заболевания 3-4 раза в год на фоне ОРВИ. Отмечает затяжной характер простудных заболеваний, длительный период кашля, субфебриллитет, сохраняющийся после ОРВИ до 1 мес. Неоднократное стационарное лечение с диагнозом бронхиальная астма, неатопическая форма, тяжелое неконтролируемое течение. Настоящее обострение также на фоне ОРВИ, когда появился подъем температуры до 38°С, усилился кашель. Самостоятельно принимала азитромицин 500 мг в течение 3-х дней с положительным эффектом. Однако сохранялся приступоообразный кашель, одышка, в связи с чем пациентка госпитализирована.
Аллергологичекий анамнез не отягощен. Пациентка не курит и никогда не курила. Работу на вредных производствах и неблагоприятных климатических условиях отрицает.
При поступлении: состояние относительно удовлетворительное. Эмоционально лабильна. Кожные покровы обычной окраски и влажности. В легких дыхание жесткое, хрипов нет, XL 16 в мин. Тоны сердца приглушены, ритм правильный, ЧСС – 84 уд/мин, АД – 120/80 мм рт.ст.
При обследовании: Нb – 138,0/л, эритроциты – 4,34¥1012/л, цветовой показатель – 0,91 лейкоциты – 8,0¥109/л, СОЭ – 5 мм/ч. С-реактивный белок – отрицательно.
ФВД: ЖЭЛ – 96%, ОФВ1 – 80%, Индекс Тиффно – 77, ПСВ – 61%, МОС25 – 57%, МОС50 – 36%, МОС75 – 23%. После игаляции бронхолитика прирост ОФВ1 2%.
Рентгенография органов грудной клетки: легочная ткань эмфизематозна. Легочный рисунок избыточен. Междолевая плевра несколько утолщена. Корни с признаками фиброза. Синусы свободны. Сердце и аорта без особенностей.
При анализе истории болезни пациентки обращало на себя внимание раннее начало заболевания, частые пневмонии и рецидивирующие бронхиты в раннем детском и подростковом возрасте, многочисленные простудные заболевания, приводящие к ухудшению состояния пациентки, длительному кашлю, прогрессирующее течение заболевания, несмотря на постоянную базисную терапию ИГКС. Тем не менее, у пациентки сохранялись даже при обострении заболевания нормальные показатели ФВД и отсутствие положительного бронхолитического теста. На рентгенограмме органов грудной клетки признаки эмфиземы, в то же время не имелось данных о внешних неблагоприятных факторах (курение, профессиональные вредности, переохлаждения, плохие условия быта).
Учитывая имеющийся анамнез заболевания, было решено провести анализ крови на уровень a1-антитрипсина. Было выявлено снижение данного показателя: 0,61 мг/мл (норма 0,8-1,5 мг/мл).
Был выставлен диагноз: Дефицит a1-антитрипсина. Эмифзема легких. ДН1. Пациентка направлена к пульмонологу для дальнейшей терапии.
Клинический пример 2
Пациентка З., 42 года, проходила стационарное лечение в аллергологическом отделении ГКБ №52 летом 2010 г.
Поступила с жалобами на периодически возникающее затруднение дыхания, сухой навязчивый кашель, першение в горле, осиплость голоса.
Из анамнеза: Диагноз бронхиальная астма установлен 6 лет назад. Получала терапию высокими дозами ИГКС, однако должного контроля над симптомами заболевания достигнуто не было, пациентка постоянно предъявляла вышеуказанные жалобы. В связи с неконтролируемым течением заболевания 3 года назад пульмонолог назначил пациентке системные ГКС на постоянный прием (метипред 2 таблетки в сутки). Неоднократное стационарное лечение, в том числе с парентеральным введением СГКС. С 2008 г. получает базисную ингаляционную терапию: Серетид 25/250 мкг по 2 вдоха 2 раза в день, метипред в суточной дозе от 4 до 1 таблетки в сутки (регулирует самостоятельно), однако данная терапия без должного эффекта, сохраняются вышеуказанные жалобы. В отделение поступила в неотложном порядке в связи с некупирумым приступом удушья.
Аллергоанамнез: отмечает явления ринита, конъюнктивита в сезон паллинации злаковых и сорных трав.
При поступлении: объективно: состояние удовлетворительное. Эмоционально лабильна, фиксирована на своих ощущениях. Кожные покровы обычной окраски. Лицо лунообразное. На нижних конечностях геморрагические высыпания. Дыхание в легких жесткое, хрипов нет. ЧДД – 21 уд/мин. Тоны сердца приглушены, ритм правильный АД – 130/80 мм рт.ст. ЧСС – 105 в минуту. Живот мягкий, безболезненный.
При обследовании: в общем анализе крови, мочи, биохимическом анализе крови патологических изменений не выявлено. Отмечаются изменения в коагулограмме, сдвиг показателей в сторону нарушения свертываемости крови. Консультация гематолога: тромбоцитопатия неясной этиологии.
ФВД: ЖЭЛ – 136%, ОФВ1 – 114%. Показатели ФВД без патологических изменений. Проба с бронхолтиком отрицательна. Уровень оксида азота – 11 ppb (норма -до 20 ppb). Уровень кортизола – 50 нмоль/л.
При дополнительном расспросе были выявлены жалобы на ощущение комка в горле, частую изжогу и отрыжку, особенно в ночное время. Проведена ЭГДС выявлена ГЭРБ, эзофагит.
За период нахождения в стационаре обращало на себя внимание неоднократное развитие «приступов удушья», сопровождавшихся выраженной эмоциональной окраской, расширением зрачков, обильной жестикуляцией. Данные приступы развивались всегда в присутствии медицинского персонала или пациентов клиники. Было заподозрено наличие гипервентиляционного синдрома, в связи пациентке было введено замаскированное плацебо (внутривенное введение физиологического раствора) с целью купировать приступы удушья. Затрудненное дыхание купировалось в течение 5 мин после инфузии. При сборе анамнеза и оценке психо-эмоционального статуса пациентки обращало на себя внимание, что в течение последних 5 лет пациентка не работает, ссылаясь на тяжелое течение заболевания. Любые попытки снизить дозу СГКС, провести какие-либо диагностические мероприятия для уточнения диагноза, в том числе и с привлечением врачей смежных специальностей встречают активное противодействие со стороны пациентки. При анализе истории болезни выявлено четкое несоответствие жалоб больной к предполагаемому диагнозу. Клинически: отсутствие хрипов в легких даже при «приступах удушья», постоянный характер жалоб, отсутствие эффекта от проводимой противоастматической терапии. Функционально: отсутствие изменений показателей функции внешнего дыхания, отрицательный бронхолитический тест, нормальные показатели оксида азота в выдыхаемом воздухе.
Несмотря на имеющийся у пациентки отягощенный аллергологический анамнез клинико-функциональных данных за наличие у нее бронхиальной астмы нет. Вероятно, данный клинический случай может рассматриваться как сочетание сразу нескольких патологий у данной пациентки: ГЭРБ и гипервентиляционного синдрома. На данный момент у пациентки также имеются осложнения длительной системной стероидной терапии в виде синдрома Иценко-Кушинга, осиплость голоса как побочный эффект лечения высокими дозами ИГКС.
С пациенткой проведены неоднократные беседы и начато снижение дозы СКГС с целью их полной отмены, и в дальнейшем коррекции дозы ИГКС. Рекомендовано лечение блокаторами протоновой помпы, консультация психотерапевта.
Гипердиагностика бронхиальной астмы, по нашему мнению, связана с тем, что не учитываются характерные для аллергических заболеваний анамнестические сведения, не берется во внимание отсутствие указаний на особенности течения болезни, в частности, не типичный для бронхиальной астмы бронхообструктивный синдром, отсутствие характерной для бронхиальной астмы клинико-функциональной картины, в том числе изменений на ФВД. В связи с ошибочным диагнозом больных не подвергают подробному бронхологическому обследованию, отсутствие которого может повлечь за собой дальнейшие диагностические и терапевтические ошибки, и как следствие ухудшение состояния пациента.
Литература
1. Глобальная стратегия лечения и профилактики бронхиальной астмы (GINA), Пересмотр 2006 г., пер. с английского, М.: Атмосфера, 2007.
2. Глобальная стратегия диагностики, лечения и профилактики хронической обструктивной болезни легких. Пересмотр 2004 г. / Под редакцией Чучалина А.Г., М.: Атмосфера, 2007.
3. Клиническая аллергология и иммунология. Руководство для практических врачей / Под общей редакцией Горячкиной Л.А, Кашкина К.П., М.: Миклош, 2009.
4. Абросимов В.Н., Гипервентиляционный синдром и дисфункциональное дыхание. Лечащий врач. 2007;8.
5. Васильев Ю.В. Бронхиальная астма, сочетающаяся с гастроэзофагеальной рефлюксной болезнью. Лечащий врач. 2004; 9.
6. Зарембо И.А. Ведение больных хронической обструктивной болезнью легких. Российский медицинский журнал. 2004; 12: 24.
7. Княжеская Н.П., Современные аспекты диагностики бронхиальной астмы . Клиническая аллергология, иммунология, инфектология. 2006; 2.
8. Моногарова Н.Е., Мороз Т.В., Минаев А.А., Донецкий национальный медицинский университет им. М. Горького, Кафедра внутренней медицины им. А.Я. Губергрица. Недостаточность альфа-1-антитрипсина. Гастроэнтерология. 2009.
9. Ноников В.Е. Хроническая обструктивная болезнь легких: диагностика и лечение. Consilium Medicum. 2004; 6: 5.
10. Почивалов А.В., Блинова А.С., Погорелова Е.И. и др. Ошибки в диагностике бронхиальной астмы у детей и подростков. Научно-Медицинской вестник Центрального Черноземья. 2004; 12.
11. Рожжев М.Е., Современные показатель распространенности бронхиальной астмы среди детей. Пульмонология. 2002; 1: 42-46.
12. Серебряков Д.Ю., Терапевтический подход к диагностике и лечению больных с трахеобронхиальной дискинезией. Диссертация кандидата медицинских наук, М.: 2004.
13. Токарева Н.А, Гипервентиляционный синдром при соматической патологии (на примере бронхиальной астмы, гипертонической болезни) и органном неврозе – особенности течения и лечения. 2004.
14. Трисветова Е.Л., Ряполов Н.А., Федорович С.Е. Трахеобронхиальная дискинезия: клиника, диагностика, лечение. Здравоохранение. 2009; 1.
15. Чучалин А.Г., Бронхиальная астма и астмоподобные заболевания. Российский медицинский журнал. 2002; 5.
16. Чучалин А.Г., Эмфизема. Лечащий врач. 1998; 4.
УДК 616.24-036.12-07
Р.Ф. ХАМИТОВ1, Л.А. ДОРОНИНА2, Е.В. ДЕМЬЯНОВА3
1Казанский государственный медицинский университет, 420012, г. Казань, ул. Бутлерова, д. 49
2Казанская государственная медицинская академия, 420012, г. Казань, ул. Бутлерова, д. 36
3Территориальный Фонд Обязательного Медицинского Страхования Республики Татарстан, 420097, г. Казань, ул. Ветеринарная, д. 6
Хамитов Рустэм Фидагиевич ― доктор медицинских наук, профессор, заведующий кафедрой внутренних болезней №2, тел. +7-917-272-96-72, e-mail: rhamitov@mail.ru
Доронина Людмила Александровна ― кандидат медицинских наук, доцент кафедры общественного здоровья, экономики и управления здравоохранением, тел. (843) 291-77-41, e-mail: mila.doronina.1962@mail.ru
Демьянова Елена Владимировна ― начальник отдела контроля качества медицинской помощи управления организации защиты прав застрахованных ТФОМС Республики Татарстан, тел.: (843) 291 77 48, +7-917-277-86-26, e-mail: Demyanova.EV@fomsrt.ru
В статье обсуждаются результаты ретроспективного сплошного анализа историй болезни пациентов с летальными исходами обострений ХОБЛ, госпитализированных в стационары Республики Татарстан и г. Казани в течение первых 6 месяцев календарного года. Изучены клинико-анамнестические и лабораторно-инструментальные диагностические подходы, выделены дефекты качества медицинской помощи, которые могли оказать влияние на летальные исходы заболевания. На основании полученных результатов оптимизированы диагностические подходы к своевременной верификации тяжелых обострений ХОБЛ в Республике Татарстан, требующие своевременной коррекции терапии в условиях стационара и последующей минимизации угрозы неблагоприятных исходов.
Ключевые слова: хроническая обструктивная болезнь легких, диагностика, ошибки, летальные исходы
R.F. KHAMITOV1, L.A. DORONINA2, E.V. DEMYANOVA3
1Kazan State Medical University, 49 Butlerov Str., Kazan, Russian Federation, 420012
2Kazan State Medical Academy, 36 Butlerov Str., Kazan, Russian Federation, 420012
3Territorial Fund of Obligate Medical Insurance of Tatarstan Republic, 6 Veterinarnaya Str., Kazan, Russian Federation, 420097
Diagnostic mistakes at chronic obstructive pulmonary disease: significance for the treatment outcomes
Khamitov R.F. ― D. Med. Sc., Professor, Head of the Department of Inner Diseases № 2, tel. +7-917-272-96-72, e-mail: rhamitov@mail.ru
Doronina L.A. ― Cand. Med. Sc., Associate Professor of the Department of Public Health, Economics and Management in Healthcare, tel. (843) 291-77-41, e-mail: mila.doronina.1962@mail.ru
Demyanova E.V. ― Head of the Department of Quality Control of Medical Aid Services of the Agency for the Rights’ Protection of the Insured Citizens of Tatarstan Republic, tel.: (843) 291-77-48, +7-917-277-86-26, e-mail: Demyanova.EV@fomsrt.ru
The article presents the results of a retrospective analysis of in-patients medical charts with fatal outcomes of COPD exacerbations during the first 6 months of the year. We have analyzed diagnostic approaches, both clinic and laboratory and instrumental findings. The obtained results allow to optimize the diagnostic approaches to quick verification of severe COPD exacerbations in Tatarstan Republic, which require the hospital therapy correction and minimization of subsequent threats of adverse outcomes.
Key words: chronic obstructive pulmonary disease, diagnostics, mistakes, fatal outcomes.
Хроническая обструктивная болезнь легких (ХОБЛ) ― прогрессирующая инвалидизирующая патология, характеризующаяся высоким уровнем заболеваемости и смертности. Пациенты отмечают уменьшение толерантности к физической нагрузке вследствие прогрессирующей одышки и связанное с этим снижение качества жизни. В настоящее время около 600 миллионов человек в мире страдают ХОБЛ. Частота клинически значимой ХОБЛ в Европе варьирует от 4 до 10% взрослого населения. Примерно 2,75 миллионов смертей ежегодно связывают с ХОБЛ, что позволяет расценивать ХОБЛ как второе по распространенности неинфекционное заболевание в мире [1]. Болезнь чаще встречается у мужчин, хотя смертность от ХОБЛ среди женщин увеличивается в промышленно развитых странах, в первую очередь, вследствие увеличения числа курящих женщин. Ожидается, что рост распространенности курения в мире продолжится, и в результате резко увеличится распространенность ХОБЛ. ВОЗ прогнозирует, что к 2030 году смертность от этого заболевания в мире переместится на 4-е место в структуре наиболее значимых причин смерти населения [2]. ХОБЛ часто диагностируется неправильно или длительно остается нераспознанной, так как на ранних стадиях заболевания пациенты могут и не предъявлять жалоб. Поэтому диагноз нередко выставляется уже на этапе среднетяжелых обструктивных нарушений (GOLD II) [3].
В развитых странах общие расходы, связанные с ХОБЛ, в структуре легочных заболеваний занимают 2-е место после рака легких и 1-е место по прямым затратам. Немногочисленные сообщения о прямых медицинских расходах при ХОБЛ свидетельствуют о том, что более 80% материальных средств приходится на стационарную помощь больным. При этом 73% расходов приходится на 10% больных с тяжелым течением заболевания. Наибольший экономический ущерб приносит лечение обострений ХОБЛ [4]. ХОБЛ представляет собой заболевание, которое можно предупредить и лечить, характеризуется персистирующим ограничением скорости воздушного потока, которое обычно прогрессирует и связано с выраженным хроническим воспалительным ответом легких на действие патогенных частиц или газов. У ряда пациентов обострения и сопутствующие заболевания могут влиять на общую тяжесть ХОБЛ. Для диагностики ХОБЛ важное значение имеет оценка симптомов заболевания, таких как хронический продуктивный кашель, одышка, а также выявление значимых факторов риска (курения, профессиональных ингаляционных воздействий вследствие различных форм воздушных загрязнений на рабочем месте, включая газы и аэрозоли, а также воздействие дыма от органического топлива). У пациентов с указанным симптомокомплексом диагноз ХОБЛ всегда должен быть подтвержден данными спирометрии (постбронходилатационными значениями ОФВ1/ФЖЕЛ < 0,7) [4].
В связи с большой социально-экономической значимостью заболевания, необходимо изучение возможных региональных особенностей ХОБЛ с позиций качества оказания медицинской помощи госпитализированным пациентам, как наиболее тяжелой категории больных с наибольшими финансовыми затратами здравоохранения. В первую очередь, это относится к пациентам с летальным исходом. Исходя из этого, была поставлена цель ― провести сплошной, комплексный ретроспективный анализ летальных исходов пациентов, госпитализированных с обострением ХОБЛ в стационары Республики Татарстан, в том числе с выявлением дефектов диагностики на различных этапах ведения пациентов.
Материалом для исследования послужили 33 истории болезни пациентов с обострением ХОБЛ, умерших в стационарах г. Казани и РТ в первом полугодии 2015 г. (сплошной анализ): 3 женщин (9%) и 30 мужчин (91%) в возрасте от 40 до 86 лет (в среднем, 65,12±1,63 лет).
Результаты исследования
Были сельскими жителями 27% пациентов, 73% ― горожанами; 20 больных имели группу инвалидности, из них 3 гр. ― 24%, 2 гр. ― 30%, 1 гр. ― 6%.
Можно выделить основные ошибки, допускаемые врачами при диагностике ХОБЛ:
- дефекты сбора анамнеза и (в меньшей степени) объективного осмотра;
- нечеткое понимание обострения ХОБЛ;
- недоучет имеющихся клинико-лабораторных, инструментальных признаков бронхиальной астмы (БА);
- неполный клинический анализ крови (недооценка эозинофилии);
- попытки микробиологических исследований мокроты в амбулаторно-поликлинических условиях, нерациональные с точки зрения фармакоэкономики;
- отсутствие данных исследования функции внешнего дыхания (ФВД), ошибки выполнения и интерпретации процедуры;
- отсутствие данных рентгенографии легких;
- недоучет актуальных осложнений (респираторных и внелегочных) и клинически значимого коморбида;
- гипероценка актуальности дополнительных исследований (в частности, в ряде случаев, бронхологических и т.д.).
Как уже было указано выше, наибольшее клинико-экономическое значение имеет адекватное ведение пациентов с обострением ХОБЛ. Начиная с 2011 г., комитет экспертов GOLD рекомендовал учитывать частоту и тяжесть обострений для верификации тяжести течения заболевания. Пациенты, имеющие в течение года более двух обострений или более одного, но потребовавшего госпитализации, трактуются как пациенты с тяжелой ХОБЛ. Клиническое понимание обострения заболевания не является простым, как может показаться на первый взгляд. При обострении больные также предъявляют жалобы на продуктивный кашель и одышку, как и при стабильном состоянии, тогда как ведение пациента с обострением значимо отличается от ведения при стабильном состоянии. Под обострением ХОБЛ на сегодняшний день понимается острое событие в течении заболевания, характеризующееся ухудшением имеющихся у больного респираторных симптомов (одышки, кашля и/или отделения мокроты) по сравнению с обычным уровнем, которое выходит за рамки ежедневных колебаний и требует изменения поддерживающей медикаментозной терапии. Таким образом, понятие обострения является очень индивидуальным и то, что для одного пациента является привычным состоянием, для другого уже может трактоваться как обострение.
Принципы адекватной диагностики обострения заболевания напрямую связаны с вопросом определения места дальнейшего лечения пациента: кого-то можно будет вести амбулаторно, для кого-то потребуется госпитализация, а кто-то будет госпитализирован сразу в отделение реанимации и интенсивной терапии.
Признаками тяжести обострений ХОБЛ являются:
- использование вспомогательных дыхательных мышц;
- парадоксальные движения грудной клетки;
- усугубление или появление центрального цианоза;
- развитие периферических отеков;
- гемодинамическая нестабильность;
- ухудшение психического состояния [2].
Показания к госпитализации для лечения обострений включают:
- значительное увеличение интенсивности симптомов, таких как внезапное развитие одышки в покое;
- тяжелые формы ХОБЛ;
- возникновение новых клинических проявлений (например, цианоза, периферических отеков);
- невозможность купировать обострение первоначально используемыми лекарственными средствами;
- серьезные сопутствующие заболевания (например, сердечная недостаточность или недавно развившиеся аритмии);
- частые обострения;
- пожилой возраст;
- недостаточная помощь дома.
Совпадение направительного и клинического диагнозов в изученных историях болезни имело место лишь в 58%, что еще раз подчеркивает сложность своевременной адекватной верификации тяжелого обострения ХОБЛ.
Предикторами среднетяжелых и тяжелых обострений, требующих своевременной госпитализации, считают пожилой возраст, низкий индекс массы тела (ИМТ), низкий ОФВ1, анамнез (фенотип) частых обострений, женский пол, выраженность одышки (по шкале MRC).
В исследуемой когорте пациентов превалировал мужской пол, средний возраст соответствовал прогнозу тяжести обострения (79% пациентов были старше 60 лет).
ИМТ ниже 18,5 имели лишь 8%, тогда как 42% ― выше 25. Данное обстоятельство можно отнести к региональным признакам ХОБЛ, возможно связанным с особенностями питания населения. Также не исключено, что сохранный ИМТ у большинства пациентов обусловлен относительно невысокой распространенностью курения (27%, при этом в 45% приверженность табакокурению врачами в анамнезе не была указана).
Средний ОФВ1 32,7±7,4% от д.в. соответствовал тяжелым обструктивным нарушениям (GOLD III). Тяжесть вентиляционных нарушений при ХОБЛ напрямую коррелирует не только с тяжестью, но и частотой обострений, а значит, оказывает непосредственное влияние на выживаемость пациентов. Данные спирометрии пациентов (n=7) представлены в таблице.
Таблица.
Данные спирометрии при госпитализации (M±m, % от должных величин)
| Параметры | Значение |
| ОФВ1 | 32,7±7,4 |
| ЖЕЛ | 39,41±5,61 |
| ФЖЕЛ | 39,98±6,91 |
| ОФВ1/ФЖЕЛ | 0,63±0,06 (абс. зн.) |
| ПСВ | 37,55±12,69 |
В связи с тяжестью состояния 79% больных были госпитализированы сразу же в первый день обращения за медицинской помощью. Таким образом, была исключена попытка адекватной амбулаторной терапии. Возможно, данное обстоятельство обусловлено поздним обращением пациентов с обострением ХОБЛ за медицинской помощью.
Жалобы на одышку предъявляли 94% больных, но объективизация оценки тяжести клинических симптомов (в первую очередь, одышки) и их влияния на пациента (MRC, CAT), а также оценка годичной частоты обострений ни у кого в истории болезни отражена не была.
Структура жалоб пациентов представлена на рисунке 1.
Рисунок 1.
Структура жалоб пациентов при госпитализации, %
67% имели при госпитализации нормальную температуру тела, 70% ― тахипноэ в покое со средней частотой дыхания 27,94±1,07 в мин. Средние цифры артериального давления были в пределах нормы, но 36% имели некоторую склонность к гипотензии. В большинстве случаев отмечалась тахикардия (79%), при этом среднее число сердечных сокращений составило 108,88±3,61 в мин. Уровень сатурации кислорода в крови был снижен в 96% случаев, при этом в 24% этот важнейший показатель не был измерен.
В общем анализе крови было увеличено содержание лейкоцитов (12,79±0,91×109/л), отмечались палочкоядерный сдвиг влево (11,71±2,67%) и ускорение СОЭ (27,34±3,35 мм/ч), средний уровень эозинофилов был в пределах нормы.
В биохимическом анализе крови было повышено содержание С-реактивного протеина (42,16±20,89 мг/л), отражающего остроту воспаления, и глюкозы (8,3±0,85 ммоль/л). Основные маркеры печеночно-почечной недостаточности были в пределах нормы.
Клинический анализ мокроты, являющийся скрининговым обоснованием показаний к антимикробной терапии, был проведен лишь в 39%. Рентгенологическое исследование органов грудной клетки было сделано лишь в 64%, из них только в 48% исследование проводилось в первые сутки госпитализации. Учитывая высокую угрозу пневмоний у пациентов с тяжелой ХОБЛ, эти показатели следует признать явно недостаточными.
Факторами риска неблагоприятного исхода обострений ХОБЛ (самый крайний вариант ― летальный исход) признаны наличие сопутствующих заболеваний (в 78% изученных историй болезни была задокументирована сопутствующая сердечно-сосудистая патология), тяжелая форма ХОБЛ, фенотип с частыми обострениями, применение антибактериальных препаратов в последние 3 месяца перед обострением [2]. Исходя из имеющихся в историях болезни сведениях, объективизировать тяжесть пациентов представлялось возможным только по тяжести обструктивных нарушенй. При этом адекватность данных исследования ФВД (n=7), проведенных на пике обострения (что соответствует периоду госпитализации умерших пациентов) вызывает законные сомнения. Таким образом, в историях болезни практически не было объективных оснований (отсутствие объективизации тяжести симптомов, в первую очередь, одышки, отсутствие сведений о частоте предшествующих обострений, сомнительные данные ФВД) для объективизации тяжести течения ХОБЛ. Остается предполагать, что оценка тяжести ХОБЛ, представленная на рисунке 2, производилась лечащими врачами на субъективной основе, что, конечно же не могло не сказаться на последующей адекватности лечебных мероприятий.
Рисунок 2.
Структура первичной оценки тяжести ХОБЛ, %
Проведенный анализ позволяет выявить дефекты качества медицинской помощи, относящиеся к диагностическим подходам и сделать следующие выводы:
- Имеет место полное игнорирование практикующими врачами, как стационаров, так и поликлиник, объективизации одышки и прочих клинических симптомов посредством рекомендованных инструментов в виде шкалы MRC и теста CAT. Данное обстоятельство усугубляется еще и тем, что в соответствии с федеральными рекомендациями по ведению больных ХОБЛ, это является нарушением адекватности формулирования клинического диагноза пациентов с ХОБЛ.
- Выявлена неадекватность рентгенологической диагностики у больных с обострением ХОБЛ, проявляющаяся, в первую очередь, высокой угрозой осложнения фатальной пневмонией. Данное исследование должно проводиться всем пациентам, госпитализированным с обострением ХОБЛ, особенно имеющим тяжелые и крайне-тяжелые обструктивные нарушения в стабильном периоде заболевания.
- Результаты исследования вентиляционной функции легких у больных с обострением ХОБЛ будут более адекватными, если их проводить в период стихания обострения, уже перед выпиской из стационара для объективизации объемов базисной терапии, рекомендуемой для амбулаторного этапа.
- Исследование сатурации кислорода в крови необходимо проводить всем пациентам с обострением ХОБЛ в рамках первичного осмотра при госпитализации в связи с высокой скрининговой значимостью данного показателя для уточнения потребности и режимов кислородотерапии у данной категории больных.
- Весьма важным является выявленное недостаточное исследование мокроты у пациентов, госпитализированных с обострением ХОБЛ, уменьшающее возможности объективизации показаний к антимикробной терапии, что в последующем неминуемо отражается на успешности этой терапии.
ЛИТЕРАТУРА
- Хамитов Р.Ф., Кудрявцева Э.З., Пальмова Л.Ю., Сулбаева К.Р. Хроническая обструктивная болезнь легких: клинические рекомендации и реальная врачебная практика. Сборник статей XXI научно-практической конференции, посвященной памяти академика Н.Н. Бурденко /Под ред. С.В. Евстигнеева. ― Пенза: ИП Соколов А.Ю., 2016. ― С. 165-172.
- Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease (GOLD). ― Updated, 2016. ― 91 p.
- Шмелев Е.И., Жестков А.В., Визель А.А. и др. Оптимизация лечения хронической обструктивной болезни легких: путь к двойной бронходилатации (заключение совета экспертов Приволжского федерального округа России) // Вестник современной клинической медицины. ― 2016. ― Т. 9, вып. 3. ― С. 82-89.
- Чучалин А.Г., Айсанов З.Р., Авдеев С.Н. и др. Федеральные клинические рекомендации по диагностике и лечению хронической обструктивной болезни легких. ― Российское респираторное общество, М.: 2014. ― 41 с.
REFERENCES
- Khamitov R.F., Kudryavtseva E.Z., Pal’mova L.Yu., Sulbaeva K.R. Khronicheskaya obstruktivnaya bolezn’ legkikh: klinicheskie rekomendatsii i real’naya vrachebnaya praktika. Sbornik statey XXI nauchno-prakticheskoy konferentsii, posvyashchennoy pamyati akademika N.N. Burdenko [Chronic obstructive pulmonary disease: clinical recommendations and real medical practice. Collection of articles of the XXI scientific and practical conference dedicated to the memory of Academician N.N. Burdenko]. Penza: IP Sokolov A.Yu., 2016. Pp. 165-172.
- Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease (GOLD). Updated, 2016. 91 p.
- Shmelev E.I., Zhestkov A.V., Vizel’ A.A. et al. Optimization of the treatment of chronic obstructive pulmonary disease: the path to double bronchodilation (opinion of the expert council of the Volga Federal District of Russia). Vestnik sovremennoy klinicheskoy meditsiny, 2016, vol. 9, iss. 3, pp. 82-89 (in Russ.).
- Chuchalin A.G., Aysanov Z.R., Avdeev S.N. et al. Federal’nye klinicheskie rekomendatsii po diagnostike i lecheniyu khronicheskoy obstruktivnoy bolezni legkikh. Rossiyskoe respiratornoe obshchestvo [Federal clinical guidelines for the diagnosis and treatment of chronic obstructive pulmonary disease]. Moscow, 2014. 41 p.
Обсуждение закрыто.

Однако немногие люди понимают, что результаты этого исследования могут быть искажены из-за неправильной подготовки пациента или недостаточных усилий, приложенных пациентом при проведении спирометрического теста. Помимо правильного выполнения теста и соблюдения пациентом установленных требований, также чрезвычайно важно контролировать измерительное оборудование и выполнять необходимые действия для обеспечения его точности.
Ошибки при выполнении теста
К наиболее частым ошибкам, возникающим при выполнении спирометрического теста, относятся:
- Предоставление ложных данных, касающихся возраста, пола, веса пациента, влияющих на нормы;
- Неверный инструктаж пациента, из-за которого он во время текста не прилагает максимальных усилий для выдыхания;
- Неправильная осанка обследуемого, слишком наклоненная или опущенная голова, или неверная поддержка рук во время обследования;
- Плохое прилегание губ к мундштуку, неверный захват мундштука пациентом, или, наоборот, чрезмерное прилегание с закрытием необходимых для теста отверстий;
- Слишком поздний выдох после начала теста;
- Частичный выдох пациента перед тем, как положить мундштук в рот;
- Слишком медленное начало выдоха испытуемым.
Плохая подготовка пациента к обследованию
Неправильная подготовка пациента к анализу также может повлиять на результаты. Однако, поскольку интерес пациента состоит не в том, чтобы перехитрить прибор, а в том, чтобы получить точную оценку состояния здоровья, каждый пациент, который хочет выяснить состояние своего здоровья, не будет придумывать способы, как обмануть спирометрию, но узнает об особенностях обследования и изучит его правила. Для этого очень важно, чтобы правильные измерения соответствовали следующим требованиям:
- Пациент не может приступать к тесту сразу после еды.
- Пациенту настоятельно рекомендуется следовать указанию в отношении питания: последний прием пищи должен быть за 2 часа до обследования. Во время измерения спирометрии для дыхания потребуется физическая нагрузка, и полный желудок может повлиять на результаты индивидуальных анализов.
- Пациенту необходимо воздерживаться от курения.
- Рекомендуется воздержаться от курения за 24 часа до спирометрии, однако для заядлых курильщиков, которые не могут выдерживать такое длительное время, минимальный период отказа от курения составляет 2 часа до процедуры.
- Пациент не может употреблять алкоголь.
- Медицинские рекомендации указывают на необходимость воздержаться от употребления алкоголя за 4 часа до обследования. Однако лучше не проводить тест, если пациент употреблял его накануне.
- Пациент должен быть одет в удобную одежду.
- Чтобы дыхательные мышцы могли свободно двигаться, и человек был способен правильно дышать, необходимо подобрать одежду, которая не давит на грудь или живот.
Пациенту следует воздерживаться от физических нагрузок
Чтобы результат теста был достоверным, необходимо начать его выполнять после достаточного отдыха и отказаться от интенсивных физических нагрузок за 30 минут до теста. К таким нагрузкам можно отнести, например, прогулку быстрым шагом, и бег к месту проведения теста. Также подъем по лестнице значительно увеличивает потребность организма в кислороде и влияет на активность дыхательной системы. Поэтому пациенту лучше до проведения теста отдохнуть и отказаться от физической нагрузки.
Пациенту необходимо временно прекратить прием некоторых лекарств

Как правило, человеку рекомендуется отказаться от приема препаратов за определенное количество часов до исследования:
- За 8 часов — ингаляционные бета-амиметики короткого действия,
- 12 часов — короткого действия: теофиллин и пероральные бетамиметики,
- 24 часа — пероральные бета-амиметики длительного действия, теофиллин с антилейкотриеновыми препаратами длительного действия,
- 48 часов — бетамиметики пролонгированного действия, теофиллин пролонгированного действия,
- 7 дней — тиотропий.
Пациент должен сотрудничать со специалистом
Многие научные исследования показывают, что результаты спирометрии могут значительно различаться в зависимости от приверженности пациента инструкциям персонала. Поэтому при проведении спирометрии необходимо в точности следовать рекомендациям, когда говорят, что нужно сделать, например, втянуть или выдуть как можно больше воздуха, и т.д.
Правильный контроль оборудования
Помимо метрологических требований, которым должны соответствовать спирометры, проверка их работоспособности должна проводиться регулярно, поэтому необходимо проводить некоторые контрольные мероприятия. Это:
- Проверка внешних условий, таких как барометрическое давление, температура, влажность, которые способствуют обеспечению соответствующего преобразования объемных значений в условия BTPS, а также важны для благополучия пациента.
- Контроль исправности аппаратных модулей. В устройствах, подключенных к компьютеру, такие функции выполняются соответствующим диагностическим программным обеспечением, и такие проверки должны выполняться каждый день.
- Проверка герметичности системы подключения. Несмотря на визуальную оценку состояния соединительных труб, также рекомендуется использовать постоянное давление, которое должно составлять 3 см H2O (3 гПа) в течение 1 минуты, и это давление не должно изменяться в течение этого времени. Проверку герметичности следует проводить ежедневно.
- Правильная калибровка оборудования. Его следует проводить трехлитровым калибровочным шприцем с разной скоростью плунжера — так, чтобы это делалось для разных расходов газа. Калибровку объема также следует выполнять ежедневно.
- Проверка характеристической линейности, которая также может быть выполнена калибровочным шприцем при разном расходе. Проверки линейности следует проводить ежеквартально.
При замене программного обеспечения поддержки тестирования всегда необходимо выполнять дополнительную повторную калибровку прибора и проверки линейности.
Сегодняшние требования к умениям и навыкам врача общей практики (ВОП) продиктованы как экономической целесообразностью распределения ресурсов в системе здравоохранения, так и развитием медицинских технологий. Современное развитие медицинской техники предоставляет ВОП расширить свои диагностические возможности, в том числе самостоятельно оценить функцию внешнего дыхания (ФВД) при помощи спирометрии – базового метода исследования вентиляционной способности легких. Спирометрия является наиболее простым, неинвазивным и диагностически значимым методом выявления вентиляционных нарушений легких, часто встречающихся в работе ВОП.
Проведение спирометрии заложено в рамках приказа Министерства здравоохранения Республики Беларусь № 177 от 27.02.2018 г. «Об организации работы врача общей практики». С целью реализации поставленной задачи учреждения здравоохранения амбулаторно-поликлинического типа Республики Беларусь оснащаются портативными спирометрами, а также проводится целевое обучение ВОП по работе с ними. Наиболее широкое распространение в общей врачебной практике получил портативный спирометр отечественного (ООО «БЕЛИНТЕЛМЕД», г. Минск) производства МАС2-БМ, в дальнейшем Спирометр, обеспечивающий полноценное исследование вентиляционной функции лёгких как на приёме, так и при выезде к пациенту.
Спирометр также поддерживает выполнение Pre/Post тестов с бронхолитиками и физической нагрузкой, неограниченное архивирование результатов тестирования, организует динамическое наблюдение при рутинной спирометрии, в т.ч. режимы ХОБЛ-мониторирования и детского мониторирования. В приборе реализован контроль качества и воспроизводимости тестов в соответствии с рекомендациями ATS-1994 и ATS/ERS-2005 по предпочтению исследователя с выдачей сообщений (в т.ч. звуковых) и рекомендаций в процессе тестирования. Спирометр имеет возможность проведения скрининга ФВД с заключением по принципу «с одного взгляда», а также возможность подключения режима пульсоксиметрии.
Прибор адаптирован к проведению массовых исследований ФВД (например, при профосмотрах), допускает использование как многоразовых, так и одноразовых мундштуков, а также антибактериальных пульмонологических фильтров. Так как Спирометр оснащён встроенными аккумуляторами, то он допускает работу как в условиях кабинета, так и на выезде вплоть до полевых условий. Простую и удобную навигацию в меню прибора обеспечивает встроенный цветной сенсорный экран.
Поскольку базовые сведения о спирометрии как о методе исследования ФВД были изложены в статье «Спирометрия в общей врачебной практике» в журнале «Семейный доктор», № 3, сентябрь 2019 года, настоящая статья посвящена последовательности действий – алгоритму работы ВОП при проведении исследования.
ШАГ 1. ПОДГОТОВКА.
- Необходимо включить Спирометр и проверить его калибровку при наличии калибровочного шприца в соответствии с Руководством по эксплуатации. Соответствующее меню Спирометра приводится на Рис. 1
Рисунок 1. Главное меню спирометра МАС2- БМ
2) Следует задать пациенту вопросы о недавнем курении, имеющихся заболеваниях, использовании лекарственных препаратов, которые могут повлиять на результаты исследования;
3) Обязательно нужно внести следующие данные о пациенте по запросу прибора: Ф.И.О., дату рождения в формате день-месяц-год, рост, вес, расовый фактор, а также провести опрос о курении – в случае, если пациент курит, внести количество выкуриваемых сигарет в день и продолжительность курения в годах;
! Все данные должны быть точны, особенно при первом вводе данных пациента; рост пациента следует измерить – даже 2-3 см несовпадения реального роста пациента с тем, что он думает про себя, могут привести к недостоверному результату тестирования!
! Если пациент ранее уже обследовался на Спирометре, то его следует загрузить из архива, при необходимости откорректировав его рост, вес, фактор курения. При этом Вы сэкономите время на ввод данных пациента и не допустите ошибок, поскольку данные пациента уже были введены точно ранее!
4) Следует правильно расположить пациента перед спирометром – с прямой спиной и слегка приподнятой головой, отвернув от него экран прибора (см. Рис. 2);
Рисунок 2. Правильное положение пациента при спирометрии
5) Далее надо объяснить пациенту, как правильно использовать мундштук (см. Рис. 3).
Рисунок 3. Расположение мундштука во рту пациента
Зубы должны лежать на мундштуке, а губы – его плотно обхватывать, чтобы весь воздух как при вдохах, так и при выдохах проходил только через мундштук, а не мимо его. При этом не следует держать мундштук слишком глубоко – это может создать препятствие для свободного дыхания!
! Обращайте внимание на то, как пациент использует мундштук. Это очень важно! Никто, кроме исследователя, это не проконтролирует, а пациенты, особенно при первом для них проведении спирометрии часто допускают ошибки при использовании мундштука!
6) Необходимо объяснить пациенту порядок выполнения дыхательных манёвров для 2-х тестов: исследование жизненной емкости легких (тест ЖЕЛ – см Рис. 4),
Рисунок 4. Проведение теста ЖЕЛ
исследование форсированной жизненной емкости легких (тест ФЖЕЛ – см. Рис. 5).
Рисунок 5. Проведение теста ФЖЕЛ
Важно подчеркнуть, что дыхательные манёвры строго регламентированы в соответствии с рекомендациями ATS-1994 и ATS/ERS-2005, проводятся по командам и инструкциям исследователя. Главный принцип спирометрии информирование, контроль выполнения и сотрудничество с пациентом.
! Самостоятельно, без указаний исследователя выполнить достоверно спирометрию пациент не сможет!
7) Помогите пациенту надеть носовой зажим. Предложите ему попробовать подышать носом при надетом зажиме. Если воздух всё же проходит, то следует более тщательно укрепить носовой зажим до тех пор, пока нозальный поток не прекратится. После этого предложите пациенту попробовать подышать через мундштук до начала тестирования, укажите ему на ошибки при их наличии – это поможет ему при выполнении тестирования!
ШАГ 2. ПРОВЕДЕНИЕ.1) Начинаем исследование ФВД с проведения теста ЖЕЛ,
как менее сложного и нагрузочного для пациента. Порядок действий – в соответствии с Руководством по эксплуатации Спирометра. Обращаем внимание на то, чтобы сенсор дыхания находился в покое и пациент не пытался брать его в рот до гудка прибора – сигнала для начала тестирования. Требуемый манёвр при тесте ЖЕЛ представлен на Рис. 4.
После гудка Спирометра исследователь предлагает пациенту дышать спокойно 4-5 дыхательных циклов, затем переводит прибор в измерение ЖЕЛ нажатием клавиши и в такт дыханию пациента командует ему сделать самый глубокий вдох и затем максимально полный и продолжительный выдох.
! При выполнении спокойного дыхания не следует задавать ритм дыхания пациента командами «Раз, два, три..» или «Вдох, выдох…» – это приведёт к искажению паттерна дыхания обследуемого! На протяжении всего спокойного дыхания инструктируйте его: «Дышите спокойно, дышите спокойно…», позволяя тем самым пациенту записать свой паттерн дыхания в покое!
В процессе выполнения полного выдоха следует постоянно инструктировать пациента «Выдыхайте, выдыхайте, продолжайте выдох…», тем самым побуждая пациента корректно выполнить манёвр – сделать самый полный и продолжительный выдох, на который испытуемый способен, что и означает правильное завершение теста ЖЕЛ.
! При корректном выполнении выдоха Спирометр выдаст звуковой сигнал, информирующий исследователя о достижении приемлемой точности измерения показателя ЖЕЛ (~ 3-5%). Однако этот гудок не означает автоматическое завершение манёвра – решение о прекращении тестирования принимает исследователь, увидев как по показаниям прибора, так и наблюдая непосредственно пациента, что он более не в состоянии продолжать выдох.
Чем дольше после гудка выдыхает пациент, тем точнее Вы измерите его жизненную ёмкость лёгких!
Затем пациент возвращается к спокойному дыханию. Тест следует повторять до появления всех знаков «+» в таблице критериев качества тестов (см. Рис. 6), что означает достижение пациентом как технической приемлемости манёвров, так и воспроизводимости его дыхания. Для достижения технической приемлемости каждой попытки, а также воспроизводимости дыхания пациента исследование в тесте ЖЕЛ следует повторять не менее 2 – 3 раз, а если требуется, то и до 5 попыток, после чего рекомендуется предоставить отдых пациенту.
! Спирометр поддерживает также измерение ЖЕЛвд, когда манёвр начинается с полного выдоха, а измерение ЖЕЛ проводится на последующем максимально глубоком вдохе.
Рисунок 6. Критерии качества тестов
! Проведение только одной попытки в тесте ЖЕЛ даже при достижении нормы показателей НЕПРИЕМЛЕМО!
2) После достижения всех знаков «+» в таблице критериев качества тестов ЖЕЛ, либо после выдачи Спирометром сообщения «Исследования в тесте ЖЕЛ выполнены достоверно. Переходите к проведению следующего теста.» запускаем тест ФЖЕЛ в соответствии с Руководством по эксплуатации Спирометра. Обращаем внимание на то, чтобы сенсор дыхания находился в покое и пациент не пытался брать его в рот до гудка прибора – сигнала для начала тестирования.
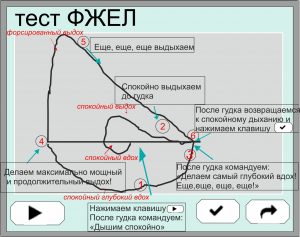
Схема выполнения манёвра в тесте ФЖЕЛ представлена на Рис. 5. Исследователь дает пациенту команду «Дышите спокойно», затем предлагает ему спокойно полностью выдохнуть (с выдохом резервного объёма выдоха РОвыд), сделать максимально полный вдох и далее без задержки самый мощный и продолжительный (форсированный) выдох. Отсюда и название этого манёвра и измеряемого показателя – Форсированная жизненная ёмкость лёгких – жизненная ёмкость лёгких, определяемая при форсированном выдохе.
При выполнении форсированного выдоха следует постоянно инструктировать пациента «Выдыхайте, выдыхайте, продолжайте выдох…», тем самым побуждая пациента корректно выполнить манёвр – сделать самый мощный и продолжительный выдох, на который испытуемый способен, что и означает правильное выполнение теста ФЖЕЛ.
! При корректном выполнении выдоха Спирометр выдаст звуковой сигнал, информирующий исследователя о достижении приемлемой точности измерения показателя ФЖЕЛ (~ 3-5%). Однако этот гудок не означает автоматическое завершение манёвра – решение о прекращении тестирования принимает исследователь, увидев как по показаниям прибора, так и наблюдая непосредственно пациента, что он более не в состоянии продолжать выдох.
Этот манёвр является самым сложным по исполнению для пациента, но, с другой стороны, наиболее информативным из всего спирометрического тестирования. Если с пациентами молодого возраста с нормальной бронхиальной проходимостью бывает сложно добиться приемлемой продолжительности выдоха, то, наоборот, пациенты старшего и пожилого возраста, особенно с наличием выраженной бронхообструкции, могут ещё долго выдыхать после гудка прибора!
! Без Вашей помощи сам пациент манёвр ФЖЕЛ корректно не выполнит!
Чем дольше пациент выдыхает, даже после гудка прибора (зачастую такой выдох сопровождается хорошо слышимыми характерными свистящими звуками), тем точнее Вы измерите его ФЖЕЛ, тем раньше Вы зарегистрируете начальные обструктивные нарушения ФВД!
! Не торопитесь завершать тестирование сразу же после того, как услышали гудок прибора!
Затем пациент возвращается к спокойному дыханию. Аналогично тесту ЖЕЛ, форсированный выдох следует повторять до появления всех знаков «+» в таблице критериев качества тестов (см. Рис. 6), что означает достижение пациентом как технической приемлемости манёвров, так и воспроизводимости его дыхания. Для достижения технической приемлемости каждой попытки, а также воспроизводимости дыхания пациента исследование в тесте ФЖЕЛ следует повторять не менее 2 – 3 раз, а если требуется, то и до 8 попыток, после чего рекомендуется предоставить отдых пациенту .
! Проведение только одной попытки в тесте ФЖЕЛ даже при достижении нормы показателей НЕПРИЕМЛЕМО!
На Рис. 7 схематически представлены возможные варианты выполнения теста ФЖЕЛ [8].
Рисунок 7. Корректное – а; технически неприемлемое выполнение манёвра ФЖЕЛ: б – кашель при первой секунде форсированного выдоха; в – преждевременное завершение манёвра; г, д – недостаточное усилие в начале манёвра.

Получение диагностически значимых результатов спирометрии – это большой труд, причём как пациента, так и исследователя! Но адекватный диагноз того стоит!
ШАГ 3. ИНТЕРПРЕТАЦИЯ
После выполнения тестов, компьютерная программа Спирометра рассчитывает ряд параметров ФВД и интерпретирует их с выдачей автоматического заключения. Результаты проведенного исследования доступны как на экране Спирометра – следует войти в меню «ЗАКЛЮЧЕНИЕ» (см. Рис. 9),
Рисунок 9. Заключение и печать спирометрического исследования.
так и в виде печатного протокола – следует войти в меню «ПЕЧАТЬ» (см. Рис. 9). Результаты исследования включают в себя как цифры – значения измеренных показателей ФВД, так и графики в спирометрическом (объём – время) и пневмотахометрическом (поток – объём) представлениях.
Протокол исследования ФВД Спирометра (см. Рис. 10)
Рисунок 10. Печатный протокол исследования с расшифровкой.
содержит следующие основные модули: данные прибора и медицинского учреждения; данные пациента; вид исследования с хронологией; таблицы измеренных значений базовых показателей спирометрии и контроля качества выполненных тестов; сводная графическая диаграмма параметров ФВД для оценки результатов по принципу «с одного взгляда»; досье респираторных рисков по данным Pre/Post тестов и динамического наблюдения; автоматическое заключение.
При анализе результатов ВОП должен оценить:
- правильность выполнения исследования. В протоколе в разделе «Критерии качества тестов» (см. Рис. 6) в соответствии с ATS/ERS-2005 следует обратить внимание на знаки «+» и «-». Знаки «+» говорят о том, что в данном исследовании были записаны технически приемлемые и воспроизводимые манёвры. Знаки «-», наоборот, свидетельствуют о недостоверности исследования – недостаточном количестве попыток, об их технической неприемлемости или недостаточной воспроизводимости.
! Не следует интерпретировать недостоверные исследования ФВД! Выбросьте их в корзину! И тогда повторное исследование будет записано качественно!
2) значения показателей объема форсированного выдоха за 1-ю секунду (ОФВ1), ЖЕЛ, ФЖЕЛ и индекс Генслара – отношение ОФВ1 к ФЖЕЛ (ОФВ1/ФЖЕЛ) для выявления отсутствия/наличия вентиляционных нарушений, а в случае наличия – их типа, уточнения степени их тяжести, мониторирования течения заболевания и оценки адекватности терапии. В протоколе исследования Вы всегда найдёте возрастные нормы в соответствии с используемым стандартом должных величин, а также абсолютные (в л и л/с) и относительные (в процентах от нормы) значения вышеуказанных показателей.
Описание показателей, предназначенных для скрининговой диагностики респираторных нарушений, представлены в таблице 1.
Таблица 1. Описание показателей «базовой» спирометрии
| № п/п | Показатель | Расшифровка | Значение |
| 1 | ЖЕЛвд | Жизненная емкость легких, измеренная на вдохе | Максимальный объем воздуха, который может вдохнуть пациент в легкие при проведении спокойного вдоха после полного выдоха |
| 2 | ФЖЕЛ | Форсированная жизненная емкость легких | Максимальный объем воздуха,
который человек может форсированно выдохнуть после максимально глубокого вдоха. |
| 3 | ОФВ1 | Объем форсированного выдоха за 1- ю секунду | Самый информативный показатель. Отражает интегральную бронхиальную проходимость дыхательных путей. |
| 4 | (ОФВ1/ФЖЕЛ) х 100% | Отношение объема форсированного выдоха за 1- ю секунду к форсированной жизненной ёмкости легких | Индекс Генслара |
| 5 | (ОФВ1/ЖЕЛ) х 100% | Отношение объема форсированного выдоха за 1- ю секунду к жизненной емкости легких | Индекс Тиффно |
Программное обеспечение Спирометра адаптировано для проведения респираторного скрининга. Сводная диаграмма параметров (см. Рис. 11)
Рисунок 11. Оценка ФВД с «одного взгляда».позволяет оценить ФВД по принципу «с одного взгляда» без анализа числовых значений. С её помощью Вы сможете достоверно оценить отсутствие/наличие вентиляционных нарушений, а в случае наличия вентиляционных нарушений – определить их тип и уточнить выраженность этих нарушений. Качественная оценка вида вентиляционных нарушений производится по цвету столбцов, относящихся к объёмным или скоростным показателям. Так зеленый цвет столбца означает нормальное значение показателя, зеленый с менее плотной штриховкой – условную норму, желтый цвет соответствует умеренному снижению, розовый – значительному снижению, красный – резкому снижению значения показателя (см. Рис. 11).
Качественное определение типа и степени нарушения вентиляционной функции лёгких может также производится с помощью визуальной оценки кривой «поток-объем», полученной при выполнении теста ФЖЕЛ (см. Рис. 12 [8])
Рисунок 12. Корректное – а; Синдром изолированной обструкции мелких бронхов (дистальные нарушения)- б; Синдром генерализованной обструкции (преходящей и стойкой) – в; Ограничительный синдром (рестрикция) – г; Синдром гипотонической дискинезии трахеи и крупных бронхов -д.
Алгоритм оценки спирометрических показателей стартует с определения типа нарушения вентиляции (обструкция/возможно рестрикция). Количественной оценке результатов исследования в первую очередь подлежат показатели ОФВ1, ФЖЕЛ и соотношение ОФВ1/ФЖЕЛ.
При снижении соотношения ОФВ1/ФЖЕЛ менее 70% фиксируют обструктивные нарушения ФВД и оценивают выраженность обструкции по показателю ОФВ1 (Таблица 2).
Таблица 2. Классификация степени тяжести бронхиальной обструкции по ОФВ1 (градация ERS/ATS, 2005)
| Степень тяжести | ОФВ1, от должной величины |
| Легкая (mild) | >70 |
| Умеренная (moderate) | 60-69 |
| Средней тяжести (moderate severe) | 50-59 |
| Тяжелая (severe) | 35-49 |
| Крайне тяжелая (very severe) | <35 |
При снижении ФЖЕЛ и нормальном соотношении ОФВ1/ФЖЕЛ предполагают рестриктивный тип нарушений с последующей оценкой структуры общей емкости легких – ОЕЛ [6].
Для углублённого понимания клинической ситуации пациента следует также обратить внимание на содержащиеся в протоколе исследования автоматическое заключение с оценкой состояния ФВД, досье рисков хронической обструктивной болезни легких (ХОБЛ) по данным Pre/Post тестов и динамического наблюдения. Последняя функция активируется при условии, что пациент неоднократно проходил исследование на одном и том же приборе либо при наличии сетевой базы данных, в которой накапливаются все спирометрические исследования учреждения здравоохранения, района, города и т.д. в соответствии с концепцией электронного здравоохранения Республики Беларусь.
Таким образом, спирометрия в ОВП сегодня является доступным, хорошо стандартизированным и высокоинформативным методом диагностики вентиляционных нарушений легких. Выполнение этого исследования является стандартом в обследовании и лечении пациентов не только с бронхолегочными заболеваниями, но и возможностью поиска ответов на целый ряд вопросов в терапевтической практике. Особое значение в организации работы ВОП приобретают электронные портативные устройства с программным обеспечением, которые позволяют проводить как скрининг, так и качественную диагностику заболеваний, тем самым улучшая доступность медицинской помощи населению. Следует отдельно подчеркнуть, что клиническая значимость спирометрии зависит от правильного выполнения маневров и адекватной интерпретации показателей, что будет требовать от ВОП, использующего данную функционально-диагностическую методику, непрерывного совершенствования профессиональных компетенций.
Спирометрия относится к инструментальным методам диагностики легких, которые делятся на три большие группы: используемые для морфологической визуализации, для оценки функции и позволяющие оценить оба этих показателя.
Для исследования морфологических изменений в бронхолегочной системе используют рентгенографию, КТ и МРТ. Эти методы широко распространены, но они не позволяют судить о том, как функционирует дыхательная система.
Лучшим способом оценить функцию внешнего дыхания является спирометрия, позволяющая не только подтвердить диагноз, но и определить тяжесть состояния пациента.
Спирометрия – что это
Справочно. Спирометрия – это исследование воздушного потока, позволяющее оценить функцию внешнего дыхания (ФВД) по многим показателям.
Проводят спирометрию с помощью специального аппарата, представленного компьютером с программным обеспечением и функциональной частью. Последняя состоит из мундштука, воздухопроводящей части и датчиков воздушного потока.
Пациент зажимает во рту мундштук и дышит в него так, как говорит врач. Воздух проходит через проводящую часть и попадает на датчик. Последний регистрирует силу, скорость и объем потока, преобразуя эти данные в различные показатели. Компьютер записывает все результаты, чертит графики и таблицы.
С помощью полученных данных строится общее представление о ФВД.
Справочно. Функцией внешнего дыхания называют способность дыхательной системы проводить воздух из внешней среды в ткань легких и в обратном направлении, а также возможность диффузии газов через ткань легких.
Оценка ФВД является важным диагностическим и прогностическим критерием, потому спирометрия часто проводится пациентам с заболеваниями легких.
Когда назначают исследование
Спирометрия показана тогда, когда необходимо подтвердить наличие заболевания дыхательной системы, узнать степень его выраженности и установить эффективность проводимого лечения.
Показаниями к назначению исследования являются:
- Наличие симптомов поражения бронхиального дерева, подозрение на возникновение бронхита;
- Необходимость подтвердить или опровергнуть диагноз бронхиальная астма, определить ее выраженность, стадию, степень контроля;
- Дифференциальная диагностика между бронхиальной астмой и хроническим бронхитом;
- Определение ФВД после перенесенных заболеваний легких;
- Определение наличия обструкции дыхательных путей и ее выраженности;
- Определение нарушения ФВД при рестриктивных патологиях (плевриты, альвеолиты, пневмонии);
- Оценка степени нанесенного вреда здоровью у работников, входящих в группу риска по дыхательной патологии (пекари, кондитеры, шахтеры, строители);
- Профессиональный осмотр спортсменов перед тяжелыми физическими нагрузками;
- Мониторирование изменений у пациентов, проходящих курс терапии в связи с бронхолегочной патологией.
Методы оценки ФВД
Справочно. На данный момент существует не так много методик, позволяющих узнать функцию внешнего дыхания. Сейчас применяются только самые точные и малоинвазивные тесты, минимизирующие возможность ошибки и риск возникновения инфекционных осложнений.
Самыми распространенными из этих методов являются:
- Спирометрия и спирография. Позволяют оценить все показатели функции внешнего дыхания, но не исключают возможность ошибки вследствие погрешности в проведении методики.
- Бодиплетизмография. Технически схожа со спирографией, но имеет большую точность. Отличие ее состоит в том, что пациент во время исследования помещается в герметичную камеру. Компьютер регистрирует не только показатели в трубке, но и давление внутри камеры. Пациент должен вдыхать воздух из камеры и выдыхать его в трубку. При этом вероятность возникновения погрешности минимальная.
- Пневмотахография. Технически метод похож на спирографию, но измеряет только один показатель – объемную скорость дыхания. В настоящее время применяется реже других методов из-за малой информативности.
- Пикфлоуметрия. Очень простой и доступный способ, позволяющий определить ФВД в любом месте, даже у себя дома. Механический прибор, обладающий мундштуком и измерителем скорости воздушного потока, показывает пиковую скорость выдоха за 1 секунду. Другие показатели прибор не определяет. Его часто используют пациенты с хроническим бронхитом и бронхиальной астмой, чтобы определить у себя начало обострения.
Подготовка к исследованию
Справочно. Данная методика не требует специальной подготовки пациента. Единственное условие ее выполнения – исключение всех факторов, которые могут повлиять на результат.
В день проведения спирометрии нельзя:
- Курить;
- Употреблять алкоголь;
- Съедать большой объем пищи, лучше вовсе отказаться от еды до проведения теста;
- Выполнять физические упражнения, даже после подъема по лестнице необходимо подождать полчаса;
- Принимать лекарственные препараты, способные повлиять на функцию дыхания, лучше вовсе отказаться от приема любых препаратов до проведения теста.
Кроме того, на пациенте должна быть свободная одежда, не сдавливающая грудную клетку и живот. Корсеты и бандажи перед процедурой следует снять.
Методика проведения
Перед спирометрией врач измеряет массу тела пациента и его рост, заносит показатели в компьютер, также в программу вносятся данные пациента, его возраст, пол и полное имя.
Справочно. После этого обследуемый садится на стул, сохраняя максимально ровную осанку. Лишние движения во время проведения методики запрещены из-за возможных искажений результатов.
На аппарат надевают одноразовый мундштук, после чего врач учит пациента правильно дышать. Ему заранее объясняют, что значит спокойное дыхание, глубокое дыхание, форсированный выдох и вдох. Затем на нос пациента надевают зажим, а мундштук помещают в рот и просят плотно прижать его губами.
Врач запускает программу и дает пациенту инструкции. Вначале его просят дышать в спокойном привычном темпе. Затем – сделать максимально глубокий вдох и выдох. После этого пациент дышит максимально быстро и поверхностно. Инструкции могут быть изменены в соответствие с поставленными целями.
Все это время программа записывать полученную информацию, чертит графики, подсчитывает показатели спирометрии. После этого все результаты выводятся на экран компьютера врача. Как правило, методику повторяют дважды или трижды, чтобы убедиться в отсутствии погрешности в технике выполнения.
Справочно. При необходимости отличить обратимые изменения бронхиального дерева от необратимых, пациенту вводят сальбутамол. Спирометрию проводят до пробы с препаратом и через 15 минут после его введения.
Спирометрия с бронхолитиком позволяет провести дифференциальную диагностику между бронхиальной астмой и ХОБЛ, потому применяют его не всегда.
Спирометрия – норма
Спирометрия позволяет определить множество показателей внешнего дыхания и сравнить их с нормативными значениями. Последние могут значительно отличаться у лиц разного пола и возраста.
Внимание. В каждом конкретном случае показатель нормы задает программа согласно введенных исходных данных. Нормы рассчитываются в процентах от показателя нормы.
В ходе проведения методики определяются следующие показатели спирометрии:
- Жизненная емкость легких. Это объем газов, который могут вместить в себя легкие при максимальном наполнении. Как правило, средний показатель ЖЕЛ около 3,5л, но он может значительно отличаться у спортсменов, стариков и подростков. Нормальным считается уменьшение ЖЕЛ не более чем на 20% от долженствующей.
- Форсированная жизненная емкость. Показывает объем максимального выдоха. Он должен быть равен 80% от измеренной ЖЕЛ.
- Объем резервного вдоха и выдоха. Является разницей между максимальным и спокойным вдохом, максимальным и спокойным выдохом. В норме равен примерно 1,5л 30-40% ЖЕЛ);
- Общая емкость легких. Отличается от жизненной емкости тем, что учитывает так называемое “мертвое пространство” – ту часть дыхательной системы, которая не участвует в газообмене. Сюда входят все воздухоносные пути от полости носа до бронхиол. В норме ОЕЛ примерно в 2 раза больше ЖЕЛ.
- Объема форсированного выдоха за 1 секунду. Показывает величину выдоха, совершаемого пациентом за первую секунду с максимальной скоростью. Нормой считают уменьшение показателя не более, чем на 25%, долженствующая величина рассчитывается в процентах от ЖЕЛ.
- Индекс Тиффно. Является отношением ОФВ1 к ЖЕЛ. В норме индекс равен 0,7 или более.
Справочно. Это наиболее информативные показатели спирометрии, которые позволяют определить основные виды патологии дыхательную системы. В зависимости от поставленных задач количество показателей может быть увеличено.
Особенности исследования у детей
Детям сложно объяснить, как именно необходимо дышать во время проведения спирометрии. Они часто допускают ошибки, могут капризничать или отказываться выполнять тест.
Справочно. До 5 лет проводить исследование бессмысленно, поскольку до этого возраста дети не могут сделать правильный выдох. Любое повышение нагрузки – плачь, крик, излишняя подвижность – искажают результаты теста. Потому его делают детям школьного возраста, находящимся в спокойном состоянии.
Рекомендуется проведение методики в детском кабинете функциональной диагностики, где есть игрушки, отвлекающие картинки и доброжелательная атмосфера. Детский врач-диагност умеет находить подход к детям и объяснять им, что требуется делать.
До 9 лет желательно использовать вспомогательные картинки. Например, показывать ребенку праздничный торт со свечой, которую он сможет задуть, если правильно выдохнет воздух в трубку. Во время спирометрии важно следить за тем, чтобы мундштук был плотно охвачен губами и воздух не проходил мимо него.
Следует несколько раз повторить методику, а затем сравнить показатели. Если два полученных один за другим результата отличаются незначительно, спирометрию можно считать информативной. В противном случае исследование стоит повторить еще раз или отложить на некоторое время.
Интерпретация полученных данных у детей также имеет свои особенности.
Справочно. Существуют специальные формулы, которые переводят нормативные показатели взрослых, пересчитывая их с учетом детского возраста. Как правило, пользуются программами, которые автоматически выдают результаты, учитывая возраст обследуемого.
Спирометрия – расшифровка
Во время интерпретации результатов отвечают на два вопроса: есть ли изменения ФВД и по какому типу происходят изменения, если они есть.
Существует три типа нарушения функции внешнего дыхания:
- Обструктивный. Обусловлен перекрытием воздухоносных путей на любом уровне. Характеризуется снижение ОФВ1 и индекса Тиффно. Встречается чаще всего при бронхитах, ХОБЛ и бронхиальной астме.
- Рестриктивный. Обусловлен уменьшением функционирующей ткани легких. Характеризуется Одновременным снижением ОФВ1, ЖЕЛ и ФЖЕЛ. Индекс Тиффно остается в пределах нормальных значений. Встречается при пневмофиброзе, саркоидозе, пневмокониозе, воспалительных заболеваниях легочной ткани.
- Смешанный. Снижаются все показатели, что указывается на одновременное наличие обструктивного и рестриктивного компонента. Встречается при ателектазе.
Более подробная расшифровка всех показателей и графиков, нарисованных компьютером, позволяет заподозрить конкретную патологию.
К какому врачу обратиться
Заболеваниями легких занимается пульмонолог, который дает направление на исследование. В том случае, если соответствующий аппарат есть в поликлинике, направление может дать участковый терапевт. Для детей существуют соответствующие детские специалисты – детский пульмонолог и участковый педиатр.
В случае, если исследование проводят с целью выявления бронхиальной астмы, назначить спирометрию может врач-аллерголог. Любой специалист, которому необходимо проверить функцию внешнего дыхания пациента может сделать такое назначение.
Справочно. Проводят исследование в кабинете функциональной диагностики. Там работает врач-диагност, который имеет сертификат, позволяющий работать со спирометром.
Диагност следит за правильностью выполнения методики, дает указания пациенту, после чего пишет заключение на основании полученных данных. Расшифровку результата, чаще всего, делает врач, назначивший исследование.
Пациенты с хроническими заболеваниями бронхолегочной системы могут выполнять альтернативную методику самостоятельно. Для этого у них есть карманные пикфлоуметры, показывающие пиковую скорость выдоха.
Справочно. Пикфлоуметрия менее информативна, чем спирометрия, но позволяет в общих чертах определить функцию внешнего дыхания за несколько секунд. Приобрести такой прибор можно в магазине медицинской техники.
Противопоказания
Спирометрия является неинвазивным методом, риски развития осложнений при ее проведении минимальны.
Внимание. Однако стоит учитывать, что во время исследования из-за особой методики дыхания головной мозг кратковременно испытывает гипоксию. Кроме того, повышается давление в легких, в грудной клетке и в сосудах малого круга кровообращения, увеличивается нагрузка на дыхательную мускулатуру и мышцы брюшного пресса.
Отсюда следует ряд противопоказаний к проведению спирометрии:
- Детский возраст. Дети до 5 лет не могут четко соблюдать инструкцию во время проведения исследования, потому дошкольникам спирометрию не назначают.
- Старческий возраст. Люди старше 75 лет, как правило, имеют сразу несколько заболеваний сердечно-сосудистой системы, вследствие чего риск возникновения осложнений увеличивается. К тому же в этом возрасте методика менее информативна в связи с физиологическим старением легочной ткани.
- Оперативные вмешательства менее, чем за 2 месяца до исследования. Прежде всего, операции на грудной клетке и брюшной полости. Повышение давления и нагрузка на мышцы могут привести к тому, что послеоперационные швы разойдутся.
- Прием антиагрегантов и антикоагулянтов. В этом случае повышение давления в малом круге кровообращения может вызвать кровотечение.
- Пневмоторакс в анамнезе. Особенно ограничение касается спонтанных пневмотораксов, которые могут рецидивировать при повышении нагрузки на легкие.
- Перелом ребер. В этом случае грудную клетку следует максимально щадить. Спирометрию рекомендуется отложить до полного заживления перелома.
- Сердечно-сосудистая патология в стадии декомпенсации. В эту группу противопоказаний входят сердечная недостаточность высокой степени и артериальная гипертензия.
- Глаукома. Повышение внутриглазного давления также является противопоказанием к проведению исследования.
- Острый инсульт или инфаркт. В случае возникновения этих состояний исследование необходимо отложить как минимум на месяц.
Отличие спирометрии от спирографии
Разница между двумя понятиями заключается в словообразовании согласно правилам греческой терминологии. Медицинские названия, обозначенные латинским и греческим языками, переводятся по частям, их образующим.
Термин “Спирометрия” состоит из двух частиц: “спиро-” и “-метрия”. Первая переводится как дыхание, дышать, а вторая – измерение. Термин “Спирография” имеет ту же первую часть, а вторая часть “-графия” означает записывать.
Справочно. Отсюда следует, что спирометрией обозначают сам процесс измерения функции внешнего дыхания. Спирография же – изображение или запись полученных результатов на бумаге. Как правило, термины считают синонимами, поскольку во время проведения исследования результат всегда записывают на бумаге.