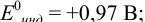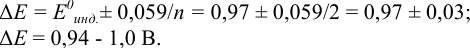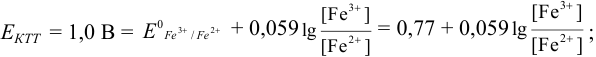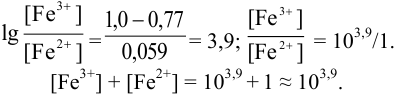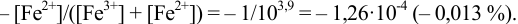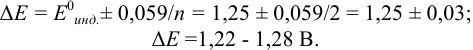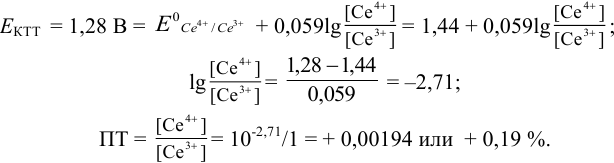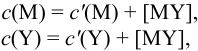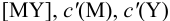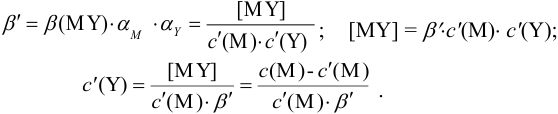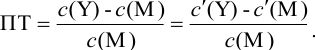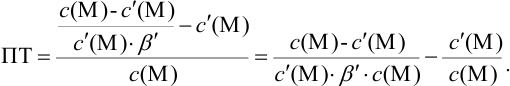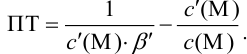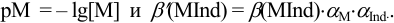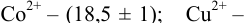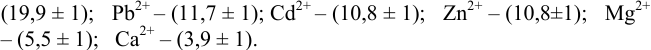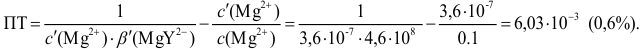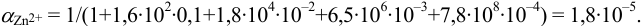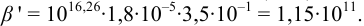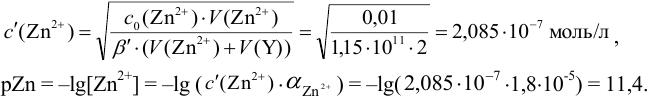Кривые титрования. Индикаторные ошибки титрования
Для
того чтобы иметь возможность выбрать
индикатор для титрования, кроме
качественных показателей, необходимо
использовать методы, дающие количественную
характеристику этого процесса. К таким
методам относятся метод построения
“кривых титрования”, метод вычисления
индикаторной ошибки, совершаемой при
титровании.
Метод “кривых
титрования”
При
прибавлении к 0,1 н. раствору кислоты
раствора щелочи такой же нормальности
происходит изменение реакции среды из
кислой в нейтральную, а затем в щелочную.
Количество прилитого раствора щелочи
будет соответствовать определенной
величине рН и цвету индикатора.
Чтобы
иметь возможность точно изучить этот
процесс и выбрать нужный индикатор,
используют графический метод. Для этого
на оси ординат откладывают величину
рН, а на оси абсцисс – количество раствора
NaOH
(в мл).
При этом образуется кривая, которая
будет характеризовать изменение рН в
зависимости от количества миллилитров
прилитого рабочего раствора. Различают
три случая: А, Б и В.
Кривая титрования
сильной кислоты (НС1) сильным основанием
Для
построения кривой в коническую колбу
наливают 20 мл
0,1 н. раствора
соляной кислоты и из бюретки добавляют
постепенно 20 мл
0,1 н. раствора натрия гидроксида.
Рассчитывают величины рН, получающиеся
в зависимости от прилитого количества
миллилитров гидроксида, и по точкам
строят кривую.
Сначала
находят начальную (исходную) точку
кривой Сhci
= 0,1 н. = 0,1
М,
поэтому концентрация [Н+]=0,1=10ˉ1
г-ион/л
и рН = 1, поскольку степень диссоциации
соляной кислоты при С = 0,1 н. будет равна
1. VNaOH
= 0, начальная точка кривой будет иметь
координаты: х1
= 0, y1
= 1. Затем определяют конечную точку
кривой (точку эквивалентности).
Концентрация растворов равна 0,1 н.,
поэтому на 20 мл
соляной кислоты будет израсходовано
20 мл
раствора натрия гидроксида и [H+]=
[OH—]
= 10ˉ7,
а рН = 7.
В
растворе будет находиться соль, натрия
хлорид, которая не будет подвергаться
гидролизу, и координаты точки
эквивалентности будут хn
= 20, рН = 7 (точка «2»), Зная координаты
начальной и конечной точек, приступают
к расчету промежуточных точек. Допустим,
что в точке «3» к 20 мл
0,1 н. раствора соляной кислоты прибавили
18,00 мл
0,1 н. раствора натрия гидроксида NaOH,
тогда в растворе осталось 2 мл
0,1 н, раствора соляной кислоты, т. е. в 10
раз меньше, и поэтому С3
=
и рН = –lg
[Н+]
=
–lg (10ˉ2)
= 2. В точке «4» прилили 19,80 мл
NaOH, поэтому chci
=
0,001 М,
[Н+]
= 10ˉ3
и рН = 3.
Таким же способом
рассчитывают и другие промежуточные
точки. По данным таблицы 10.1 строим кривую
титрования сильной кислоты сильным
гидроксидом.
Таблица 1
Изменение рН при титровании 20 мл 0,1 н. Раствора соляной кислоты раствором натрия гидроксида
|
Прибавление |
Остаток НС1 |
рН |
||
|
% |
мл |
% |
г-экв/л |
|
|
0 90 99 99,9 100,0 100,1 101 110 200 |
0 18 19,8 19,98 20,00 20,02 20,2 22 40 |
100 10 1,0 0.1 0 0,1 1,0 10,0 100 |
0,1 0,01 0,001 0,0001 10ˉ7 Избыток 0,0001 0,001 0,01 0,1 |
1 2 3 4 7 10 11 12 13 |
П
кривой титрования (рис. 1) видно, что к
концу этого титрования происходит
сильное изменение величины рН раствора
и наблюдается резкий скачок. Если за
время нейтрализации 99,9% кислоты рН
изменяется постепенно от 1,0 до 4,0, то при
добавлении весьма небольшого количества
раствора натрия гидроксида (0,1 % до точки
нейтрализации и 0,1% избыточных) рН
повышается с 4,0 до 10,0. Последняя капля
добавленной щелочи вызывает изменение
рН на 6 единиц, а [Н+]
в 1.000.000 раз, поэтому кривая на этом
отрезке занимает вертикальное положение
– этот вертикальный участок кривой
называют скачком рН на кривой титрования.
Если после достижения точки эквивалентности
продолжать добавлять раствор гидроксида
NaOH,
то [Н+]
будет уменьшаться и кривая во второй
половине будет такой же пологой, как и
в первой.
Рис.12
Кривая титрования сильной кислоты
сильной щелочью
Такая
кривая характеризуется такими
особенностями:
а) точка эквивалентности
лежит на линии нейтральности:
б) скачок рН на
кривой титрования (при 0,1 н. растворах)
имеет большой интервал – от рН = 4,0 до
рН = 10;
в)
при титровании раствора щелочи кислотой
начальная точка располагалась бы при
рН = 13 – в нижней области графика.
На
основании кривой титрования (для 0,1 н.
растворов НС1 и NaOH) можно сделать вывод,
что в этом случае применимы следующие
индикаторы: метиловый оранжевый,
метиловый красный, нейтральный красный
и фенолфталеин, т.е. такие индикаторы,
показатели титрования – рН которых
находятся в области скачка рН на кривой.
Для того чтобы не
усложнять расчеты, увеличение объема
раствора при титровании не учитывают.
Соседние файлы в папке Лекции
- #
- #
- #
- #
- #
- #
- #
Расчет индикаторных погрешностей кислотно-основного титрования
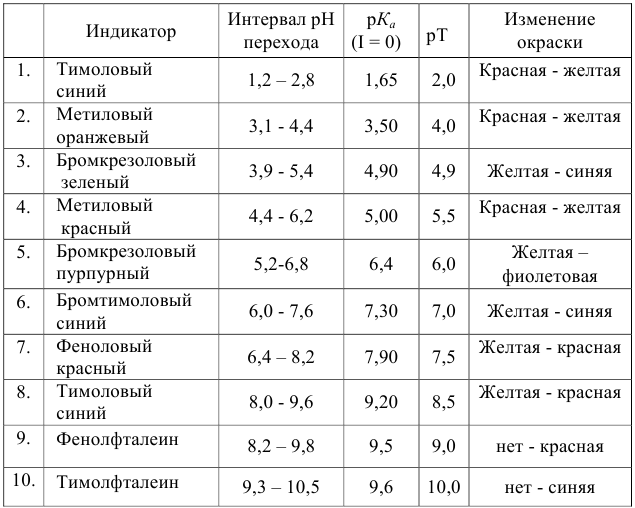
Согласно ионно-хромофорной теории индикаторов, интервал перехода окраски индикатора 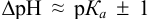
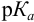
Таблица 8.12
Важнейшие кислотно-основные индикаторы
При правильно выбранном индикаторе индикаторная ПТ не должна превышать заданную погрешность измерения объема раствора в титриметрии. Типы (виды) индикаторных ПТ кислотно-осиовиого титрования и названия, встречающиеся в разных учебниках и сборниках задач, происхождение погрешностей и формулы для расчета приведены в табл. 8.13. Формулы легко выводятся из определения погрешности титрования как отношения недотитро-ванного или перетитрованного количества кислоты или основания к первоначально взятому для титрования (то есть к произведению 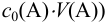
Таблица 8.13
Индикаторные погрешности кислотно-основного титрования
Пример 8.28.
Выберите подходящие индикаторы, определите тип индикаторных погрешностей и рассчитайте ПТ при титровании а) 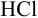
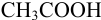
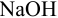
Решение:
а). Как следует из табл. 8.4 и рис. 8.1(1), для случая титрования 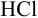

Однако используемые для расчета ПТ формулы показывают, что чем ближе рТ и 

Рассчитаем величину ПТ с двумя индикаторами: с рТ < 

С индикатором метиловым красным (рТ 5,5 < 
С индикатором фенолфталеином (рТ 9,0 > 
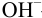
В данном случае оба индикатора пригодны, поскольку вычисленные значения ПТ не превышают заданную погрешность титрования (0,4%), но с метиловым красным систематическая индикаторная погрешность меньше.
б). При титровании 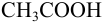



Например, при выборе фенолфталеина (рТ = 9,0):
а при выборе тимолфталеина (рТ = 10,0) погрешность возрастает в 10 раз:
Выбор фенолфталеина приводит к меньшей индикаторной погрешности титрования 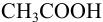
При титровании с индикаторами, для которых рТ < рНтэ, в растворе остается неоттитрованная слабая кислота, т. е. присутствует НА-ошибка (кислотная) со знаком «-» (см. табл. 8.13). Если использовать индикатор бромтимоловый синий (рТ 7,0), то вычисленная ПТ не удовлетворяет заданной точности, индикатор не пригоден:
или при проведении расчета по приближенной формуле:
Пример 8.29.
Какой индикатор позволяет оттитровать 0,1000 М гидразин 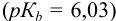
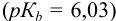
Решение:
Реакция титрования:
приводит к образованию слабой сопряженной кислоты 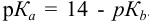
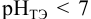
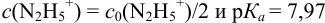
Сравнивая рТ индикаторов и 
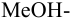
и с метиловым красным (рТ 5,5):
Из предложенных индикаторов метиловый красный позволяет провести титрование гидразина с меньшей погрешностью.
Расчет индикаторных погрешностей окислительно-восстановительного титрования
При использовании окислительно-восстановительных (редокс) индикаторов потенциал в ТЭ 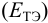

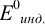
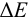
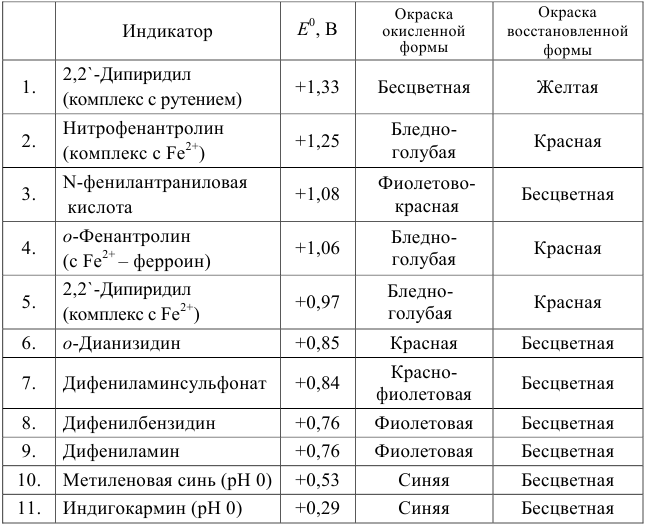
Таблица 8.14
Примеры распространенных окислительно-восстановительных индикаторов
Полуреакция восстановления и интервал перехода индикатора:
Наиболее часто в полуреакции восстановления (окисления) индикатора участвуют 2 электрона. Для индикаторов №1 — №6 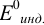
- сравнить
для выбора редокс-пары участников реакции титрования и уравнения Нернста для расчета ПТ.
Например, если 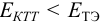
Сумма числителя и знаменателя здесь составляет 100 % титруемого вещества. Индикатор считается пригодным, если ПТ не превышает 0,1 -0,2%.
Пример 8.30.
Выберите подходящие индикаторы, определите тип индикаторных погрешностей и рассчитайте ПТ при титровании раствора соли 
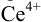
Решение:
Как следует из табл. 8.8 и рис. 8.3 (кривая 1, пример 8.25), область скачка (при относительной погрешности измерения объема 0,1 %) на кривой титрования 0,95 — 1,26 В, а 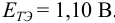
Выберем для рассмотрения порядка расчета два индикатора:
а) с 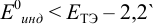
б) с 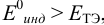
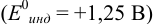
В случае а) интервал перехода индикатора:
Изменение окраски заканчивается при 
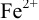
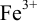
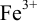

Тогда: ПТ =
В случае б) интервал перехода индикатора нитрофенантролина в виде комплекса с 
Изменение окраски заканчивается при 
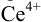
Тогда количество 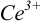
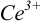
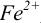
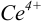
Таким образом, оба выбранных индикатора оказались приемлемыми.
Расчет индикаторных погрешностей комплексонометрического титрования
В конечной точке титрования общие концентрации определяемого иона с(М) и титранта c(Y) можно представить выражениями {для упрощения записи в общем виде упустим заряды ионов):
где 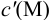
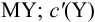
Условные константы устойчивости (см. выражение 8.16) связывают
Отсюда относительная погрешность титрования (ПТ) определяется выражением (с учетом (8.18) и (8.19)):
Подставляем в это уравнение выражение для 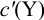
Вблизи ТЭ 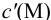
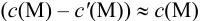
следовательно:
Выражение (8.21) тождественно выражению: 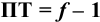
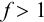
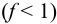
Конечная точка титрования определяется интервалом перехода окраски индикатора (интервалом рМ, в котором индикатор меняет свою окраску):
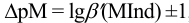
Интервал перехода окраски 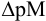
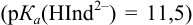
Пример 8.31.
Рассчитайте погрешность титрования 0,1 ОМ раствора 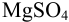

Решение:
В данных условиях 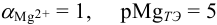
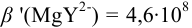
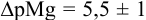
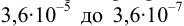
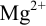
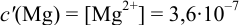
Погрешность титрования 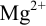
Пример 8.32.
Докажите возможность использования индикатора эриохром черный Т для титрования 0,010 М раствора 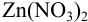

Решение:
1. Рассчитаем условную константу 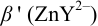
Общие константы устойчивости для аммиачных комплексов 
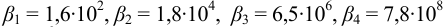

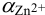
По табл. 7 и табл. 4 приложения находим 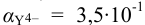
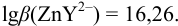

В точке эквивалентности:
Интервал перехода окраски индикатора эриохром черный Т в случае титрования ионов цинка при pH 10: 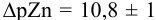
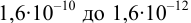

2. Конечная точка титрования наступает при [
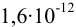

Эти примеры взяты со страницы примеров решения задач по аналитической химии:
Решение задач по аналитической химии
Возможны вам будут полезны эти страницы:
1.
Индикаторные ошибки
кислотно-основного титрования
1
2.
Водородная ошибка возникает, когда
недотитрована сильная кислота,
перетитровано сильное или слабое основание
Водородная ошибка – отношение количества
ионов водорода n(H+) в конце титрования к
первоначально взятому количеству вещества
n(X)
n
(H+)к.т.
X(H+) = ———— · 100%
n(X)
2
3.
n(X) = Сэкв(Х) · V(X)
Сэкв(Х) – молярная концентрация эквивалента
первоначально взятого вещества
V(X) – объем первоначально взятого вещества
n(H+)к.т. = [H+]к.т.· Vк.т.
Vк.т. – объем в конце титрования
Vк.т. = V(X) + V(Т)
3
4.
+] · (V(X) + V(Т))
[H
к.т.
+
X(H ) = ——————————— · 100%
С(1/z Х) · V(X)
рНк.т. = рТInd
[H+]к.т = 10–рН = 10–рТ
–рТ · (V(X) + V(Т))
10
X(H+) = ————————— · 100%
Сэкв(Х) · V(X)
4
5.
Гидроксильная ошибка обусловлена наличием
гидроксид-ионов в конце титрования и возникает, когда недотитровано сильное основание,
перетитрована сильная или слабая кислота
n(OH–)к.т.
X(OH–) = ———— · 100%
n(X)
n(OH–)к.т = [OH–]к.т. · (V(X) + V(Т))
n(X) = Сэкв(Х) · V(X)
–]
[OH
·
(V
(X) + V(Т))
к.т.
X(OH–) = —————————— · 100%
Сэкв(Х) · V(X)
5
6.
рНк.т. = рТInd
т.к. рН + рОН = 14
рОН = 14 – рН = 14 – рТ
[OH–] = 10–(14 – рТ) = 10рТ–14
рТ–14 · (V(X) + V(Т))
10
X(OH–) = —————————— · 100%
Сэкв(Х) · V(X)
6
7.
Кислотная ошибка возникает, когда остается
недотитрованной слабая кислота
Кислотная ошибка – отношение концентрации
недотитрованной кислоты в конце титрования
к ее оттитрованной части
HA + KOH H2O + KA
[HA]к.т.
X(HA) = ———— · 100%
[A–]к.т.
Оттитрованная часть кислоты будет
определяться анионами соли
7
8.
HAк.т. H+к.т. + A–к.т.
[H+]к.т. · [A–]к.т.
Kк-ты = ———————
[HA]к.т.
[HA]к.т. [H+]к.т.
———=
———
[A–]к.т.
Kк-ты
[H+]к.т.
X(HA) = ———— · 100%
Kк-ты
8
9.
рНк.т. = рТInd
[H+]к.т = 10–рН = 10–рТ
Kк-ты = 10–рК
10–рТ
X(HA) = ———— · 100%
10–рКк-ты
X(HA) =10рКк-ты–рТ · 100%
9
10.
Основная ошибка возникает, когда остается
недотитрованным слабое основание
Основная ошибка – отношение концентрации
неоттитрованного основания в конце
титрования к его оттитрованной части
[BOH]к.т.
X(BOH) = ———— · 100%
[B+]к.т.
10
11.
Аналогично с кислотной ошибкой можно
показать
[BOH]к.т.
[OH–]к.т.
—————
=
—————
[B+]к.т.
Kосн
[OH–]к.т.
X(BOH) = ———— · 100%
Kосн
Т.к. [OH–]к.т. = 10рТ–14
Kосн = 10–рКосн
11
12.
10рТ–14
X(BOH) = ———— · 100%
10–рКосн
X(BOH) =10рКосн + рТ–14 · 100%
12
13.
Вычислить ошибку титрования 0,2 н. раствора
HCl 0,2 н. раствором NaOH с индикатором
метиловым оранжевым.
рТ(м/о) = 4
ошибка водородная
–рТ · (V(X) + V(Т))
10
X(H+) = ————————— · 100%
Сэкв(Х) · V(X)
–4 · (10 + 10)
10
X(H+) = ——————— · 100 = 0,1%
0,2 · 10
Индикаторная ошибка должна быть 0,1%
13
14.
Вычислить индикаторную ошибку титрования
0,2 н. раствора HCl 0,2 н. раствором NaOH с
индикатором фенолфталеином
рТ(ф/ф) = 9
ошибка гидроксильная
рТ–14 · (V(X) + V(Т))
10
X(OH–) = —————————— · 100%
Сэкв(Х) · V(X)
9–14 · (10 + 10)
10
X(OH–) = ——————— · 100 = 0,01 %
0,2 · 10
14
15.
Вычислить ошибку титрования 0,1 н. раствора
муравьиной кислоты 0,1 н. раствором сильного основания с индикатором метиловым
красным
рТ(м/к) = 5
рК(HCOOH) = 3,76
рНт.э. = 7 + ½ рКк-ты + ½ lg Cсоли = 8,38
Раствор недотитрован ошибка кислотная
15
16.
X(HA) =10рКк-ты–рТ · 100%
X(HA) =103,76–5 · 100 = 5,7 %
Индикатор использовать нельзя.
16
17.
Чему равна ошибка титрования 0,1 н. раствора
аммиака 0,1 н. раствором HCl с индикатором
крезоловым пурпуровым
рТ(к/п) = 8
рК(NH4OH) = 4,75
рНт.э. = 7 – ½ рКосн – ½ lg Cсоли = 5,10
Раствор недотитрован ошибка основная
X(BOH) =10рКосн + рТ–14 · 100%
X(BOH) =104,75 + 8–14 · 100 = 5,6%
17


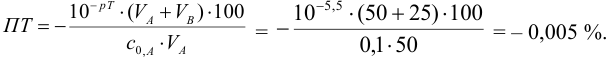
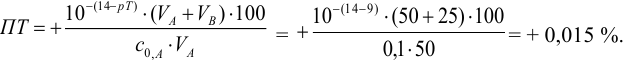
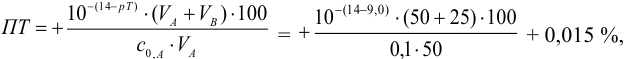
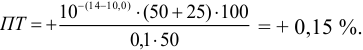
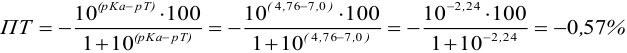
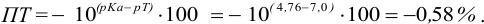
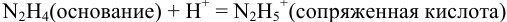
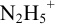
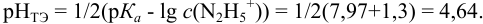
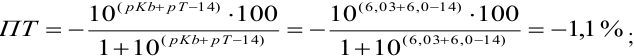
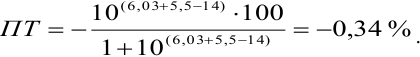

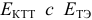 для выбора редокс-пары участников реакции титрования и уравнения Нернста для расчета ПТ.
для выбора редокс-пары участников реакции титрования и уравнения Нернста для расчета ПТ.